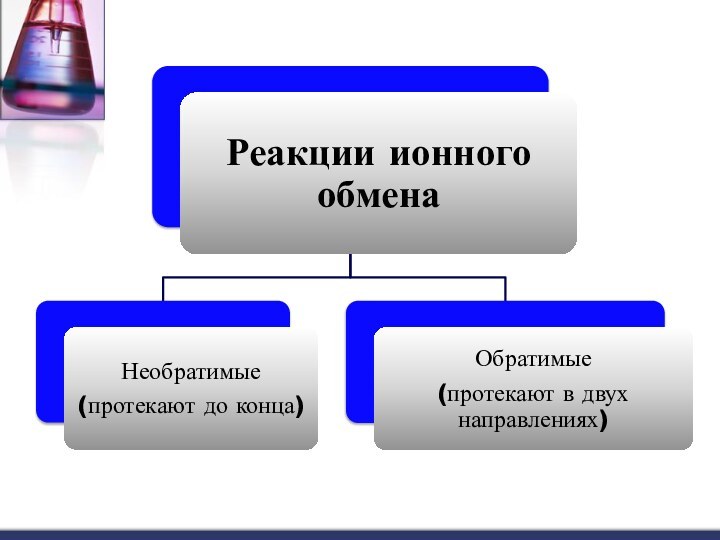
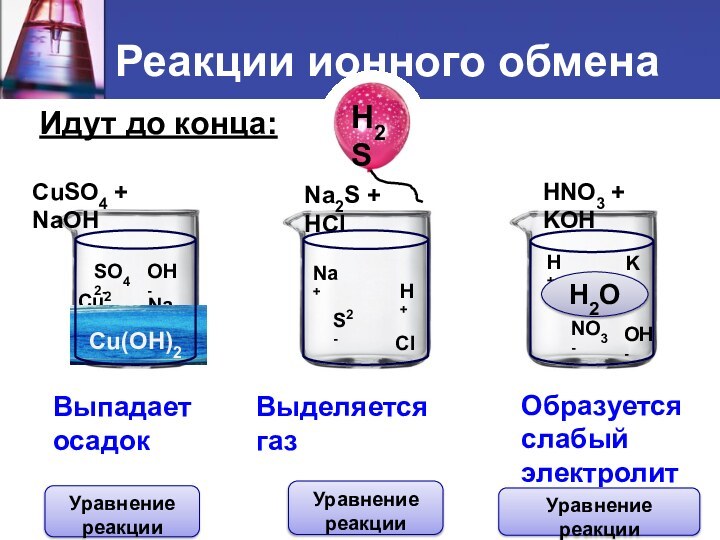
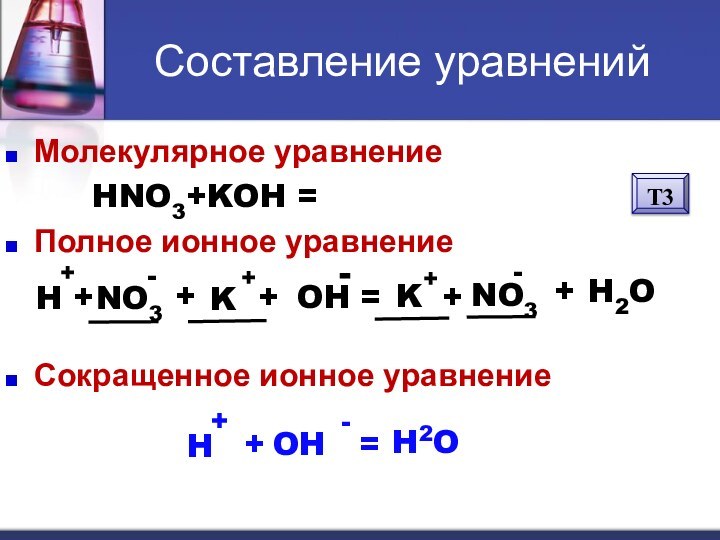
протекания реакций ионного обмена до конца;
формировать системный подход и
способность предсказывать результат реакций на основе полученных знаний;раскрыть значение реакций ионного обмена.
Презентация может быть использована для дистанционного обучения.