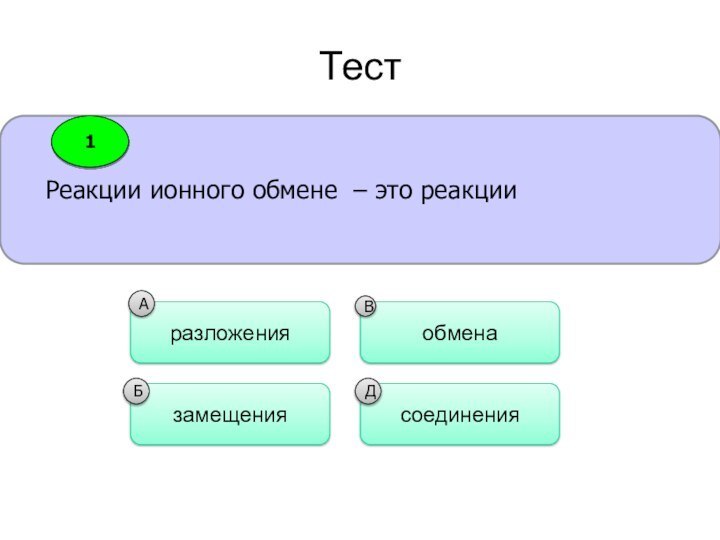
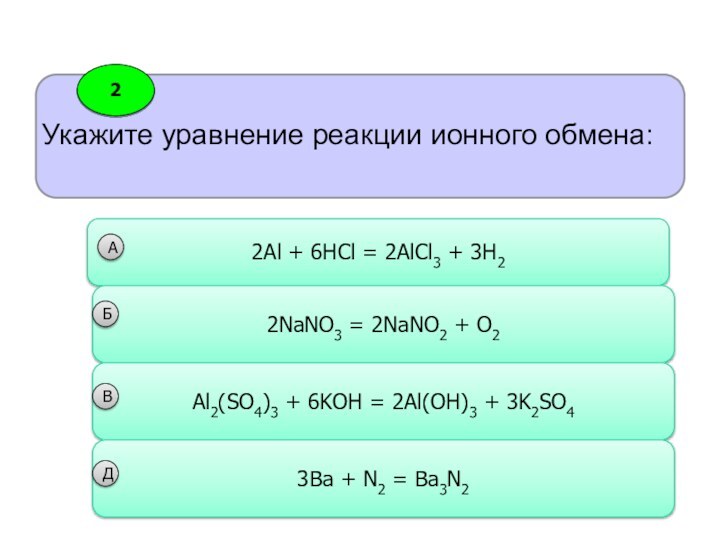
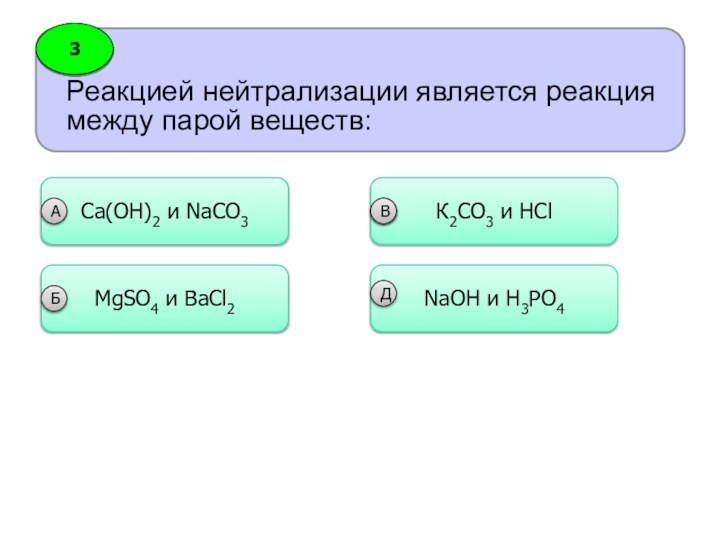
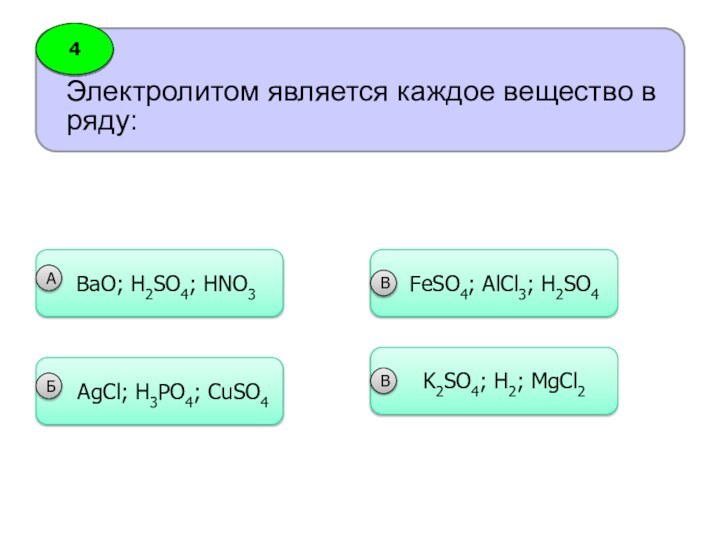
реакции протекающие
между электролитами.
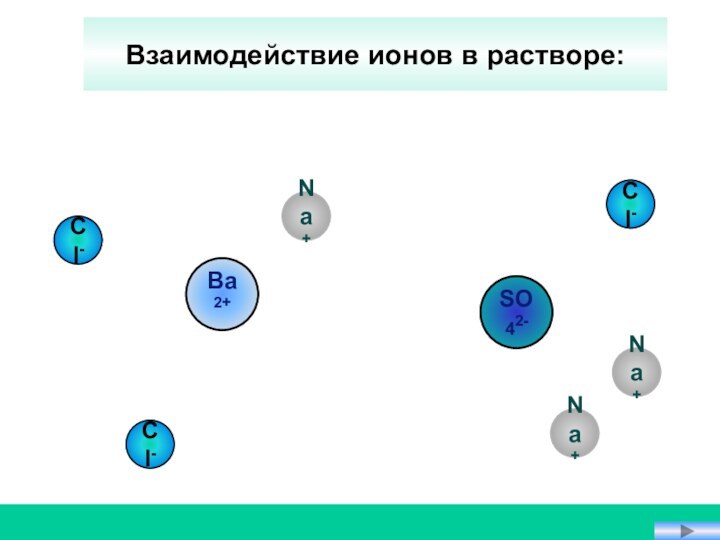
Пример: Взаимодействие хлорида бария
с сульфатом натрия.
Порядок действий:
1. Записать уравнение реакции в молекулярном виде.
BaCl2 + Na2SO4 = BaSO4 + NaCl