- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Реакции ионного обмена
Содержание
- 2. 1. Простые вещества, газы, оксиды, нерастворимые соединения
- 3. 2. Малорастворимые вещества в левой части уравнения
- 4. 3. Общая сумма зарядов ионов в левой
- 5. 4. Реакции ионного обмена идут до конца,
- 6. Последовательность действийВыполнение действий1. Записать уравнение реакции в молекулярном виде, выставить коэффициентыАlСl3+3КОНКСl3+Аl(ОН)3
- 7. Последовательность действийВыполнение действий2. Используя таблицу растворимости определить
- 8. Последовательность действийВыполнение действий3. Составить полное ионное уравнение, записав электролиты в виде ионов, неэлектролиты в молекулярном видеАl+3+Сl3-+К3++3+ОН-Аl(ОН)3↓+3К++3Сl-
- 9. Последовательность действийВыполнение действий4. Сократив ионы правой и левой части уравнения, запишем сокращённое ионное уравнениеАl+3+Сl3-+К3++3+ОН-Аl(ОН)3↓+3К++3Сl-Аl+3+3ОН-Аl(ОН)3↓
- 10. Реакций, характеризующих общие химические свойства кислот. 1.
- 11. Последовательность действийВыполнение действий1. Молекулярное уравнениеZn+Н2SО4ZnSО4+Н22. Полное ионное уравнениеZn+SО4SО4+Н2↑Н+2Zn++-2+2-23. Сокращённое ионное уравнениеZn++Н2↑Н2Zn++2
- 12. 2. Кислоты взаимодействуют с оксидами металлов.Молекулярное уравнениеСuO+Н2ОН2SО4CuSО4+Полное ионное уравнениеSО4CuО+H+SО4Cu++H2O+-2+2-22
- 13. Сокращённое ионное уравнениеCuО+HCu+H2O++223. Кислоты взаимодействуют с основаниями (гидроксидами) – реакции нейтрализации.
- 14. H2SO4+KOHK2SO4+2H2O2SO4+KK+2H2O2H+OHSO4+222++-2+-+-2+2H2O2HOH2++-H2SO4+Cu(OH)2CuSO4+H2O2
- 15. SO4HCu(OH)2++++-2-2+222SO4Cu+H2OHCu(OH)2+++222Cu+H2O3. Кислоты взаимодействуют с солями.
- 16. H2SO4+BaCl2+BaSO4HCl↓2SO4+Ba+BaSO4Cl↓2H+Cl+H222++-2+2--+SO4+BaBaSO4↓-2+2
- 17. H2SO4+K2CO3K2SO4+H2CO3CO2 + H2O+H+KK+CO2 + H2O+SO4+CO3SO4+222+-2+-2+-2H+CO2 + H2OCO32+-2
- 18. Задания для самоконтроля1. Напишите молекулярные, ионное и
- 19. в) карбоната натрия и нитрата свинца(II)г) нитрата
- 20. Скачать презентацию
- 21. Похожие презентации
1. Простые вещества, газы, оксиды, нерастворимые соединения не диссоциируют (в ионных уравнениях их записывают в молекулярном виде).










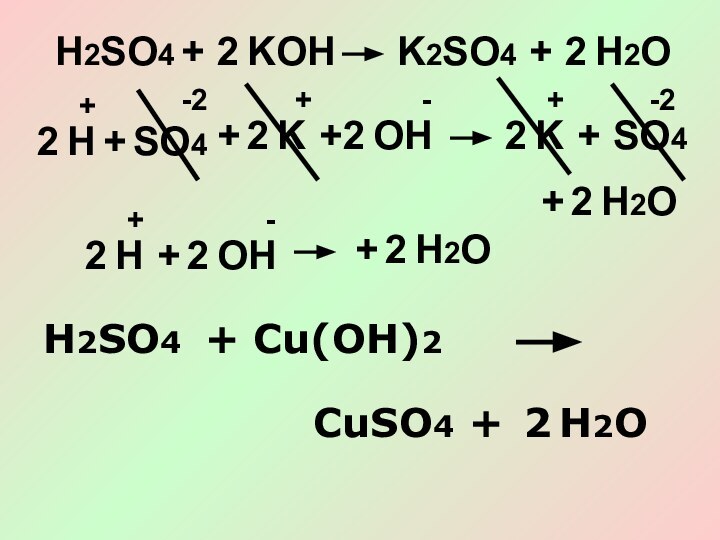


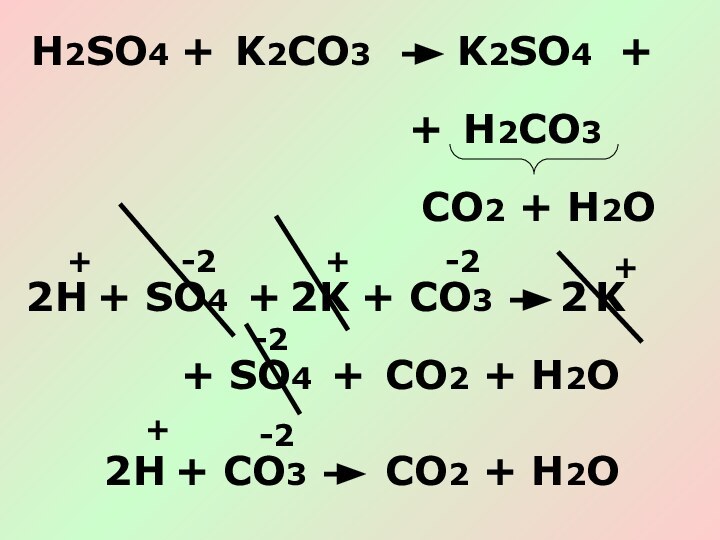



Слайд 3 2. Малорастворимые вещества в левой части уравнения записывают
в виде ионов, а в правой части – в
молекулярном виде (т. е. считают нерастворимыми).Ва
+
SО4
ВаSО4
+2
- 2
Сульфат бария
Слайд 4 3. Общая сумма зарядов ионов в левой части
уравнения должна быть равна общей сумме зарядов ионов в
правой части.Ва
+
SО4
(ВаSО4)
+2
- 2
0
+2·1 + (-2)·1 = 0
Слайд 5 4. Реакции ионного обмена идут до конца, если
образуется: а) осадок (↓); б) газ (↑); в) малодиссоциирующее
вещество (Н.,М.).
Слайд 6
Последовательность действий
Выполнение действий
1. Записать уравнение реакции в молекулярном
виде, выставить коэффициенты
АlСl3
+
3
КОН
КСl
3
+
Аl(ОН)3
Слайд 7
Последовательность действий
Выполнение действий
2. Используя таблицу растворимости определить растворимость
каждого вещества
АlСl3 – р.
КСl – р.
КОН – р.
Аl(ОН)3 –
н.АlСl3
+
3
КОН
КСl
3
+
Аl(ОН)3↓
Слайд 8
Последовательность действий
Выполнение действий
3. Составить полное ионное уравнение, записав
электролиты в виде ионов, неэлектролиты в молекулярном виде
Аl
+3
+
Сl
3
-
+
К
3
+
+
3
+
ОН
-
Аl(ОН)3↓
+
3
К
+
+
3
Сl
-
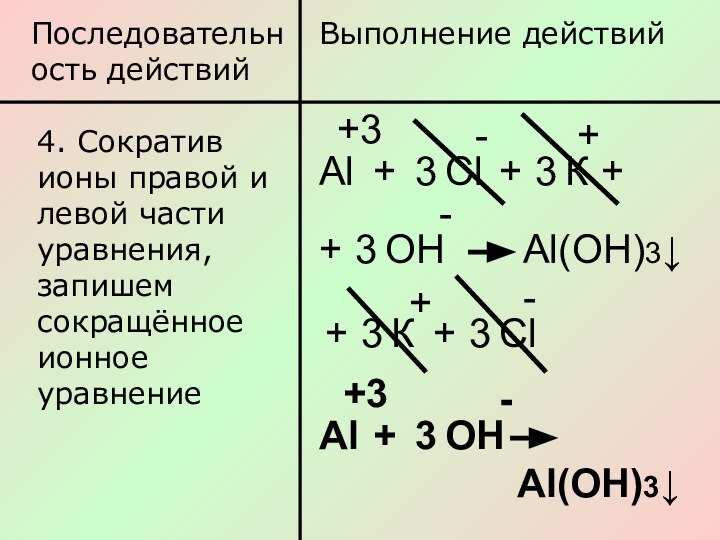
Слайд 9
Последовательность действий
Выполнение действий
4. Сократив ионы правой и левой
части уравнения, запишем сокращённое ионное уравнение
Аl
+3
+
Сl
3
-
+
К
3
+
+
3
+
ОН
-
Аl(ОН)3↓
+
3
К
+
+
3
Сl
-
Аl
+3
+
3
ОН
-
Аl(ОН)3↓
Слайд 10
Реакций, характеризующих общие химические свойства кислот.
1. Кислоты
взаимодействуют с металлами, расположенных в ряду электрохимического ряда напряжения
до водорода.
Слайд 11
Последовательность действий
Выполнение действий
1. Молекулярное уравнение
Zn
+
Н2SО4
ZnSО4
+
Н2
2. Полное ионное уравнение
Zn
+
SО4
SО4
+
Н2↑
Н
+
2
Zn
+
+
-2
+2
-2
3.
Сокращённое ионное уравнение
Zn
+
+
Н2↑
Н
2
Zn
+
+2
Слайд 12
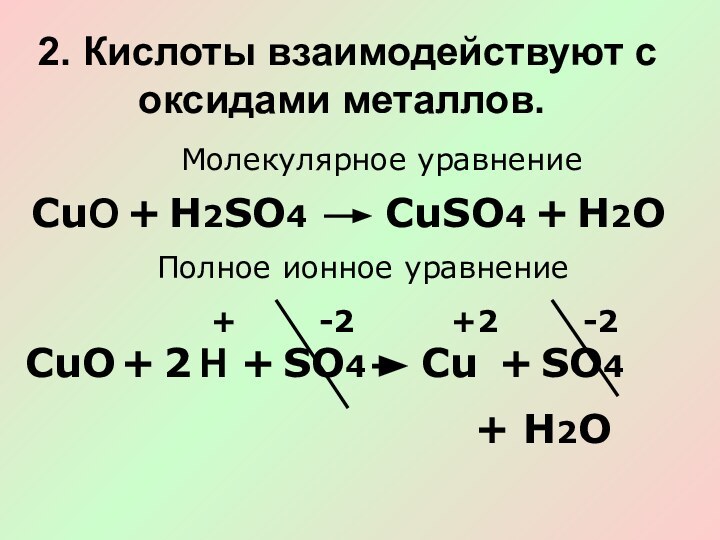
2. Кислоты взаимодействуют с оксидами металлов.
Молекулярное уравнение
СuO
+
Н2О
Н2SО4
CuSО4
+
Полное ионное
уравнение
SО4
CuО
+
H
+
SО4
Cu
+
+
H2O
+
-2
+2
-2
2
Слайд 13
Сокращённое ионное уравнение
CuО
+
H
Cu
+
H2O
+
+2
2
3. Кислоты взаимодействуют с основаниями (гидроксидами)
– реакции нейтрализации.
Слайд 18
Задания для самоконтроля
1. Напишите молекулярные, ионное и сокращенные
ионные уравнения реакций между растворами:
а) серной кислоты и нитрата
бария б) гидроксида калия и фосфорной кислоты