- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Соединения галогенов
Содержание
- 2. Цели урока:Рассмотреть свойства и применение важнейших соединений
- 3. Основное содержаниеПонятие о галогеноводородахГалогеноводородные кислотыОксокислотыГалогениды.(соли)Значение соединений галогенов.
- 4. Соединения галогенов Галогеноводороды, – Это едкие газы
- 5. Получение хлороводорода NaСl(тв) + Н2SО4(конц) = НСl↑ + КНSО4.
- 6. Галогеноводородные кислотыОбразуются при растворении галогеноводородов в воде.
- 7. ОксокислотыХлорная – НСlO4
- 8. СолиФторидыХлоридыБромидыЙодидыГалогениды Na F KClKBrNaI
- 9. Качественная реакция на галогенид - ионыВзаимодействие с
- 10. Фтор F2
- 11. Соединения фтораn(-CF2-CF2-) Тефлон
- 12. Галит (NaCl )ХлорДДТ (дихлородифенилтрихлорэтан)KClO3 - Бертолетова соль.2KClO3 + 3S = 2KСl + 3SO2↑.
- 13. AgBr- фотографияNaBr- дубление кожиKBr- линзы LiBr- используется в кондиционерах.Бром
- 14. Получил Б.Куртуа. (1811 г)2NaI + 2H2SO4 =
- 15. Скачать презентацию
- 16. Похожие презентации
Цели урока:Рассмотреть свойства и применение важнейших соединений галогенов. Изучить качественные реакции на галогенид-ионы. Рассмотреть свойства и применение важнейших соединений галогенов и способы получения галогенов.













Слайд 3
Основное содержание
Понятие о галогеноводородах
Галогеноводородные кислоты
Оксокислоты
Галогениды.(соли)
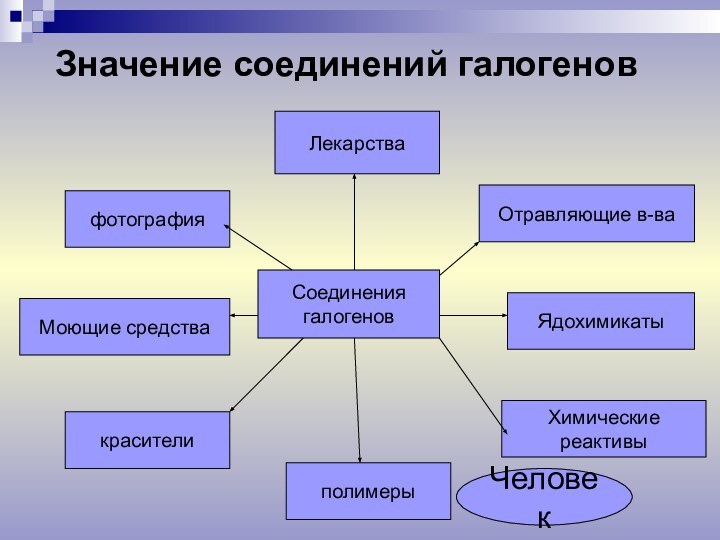
Значение соединений галогенов.
Слайд 4
Соединения галогенов
Галогеноводороды, – Это едкие газы с
резким запахом, хорошо раствормые в воде
HF
HCl HBr HIфтороводород
хлороводород
бромоводород
йодоводород
Слайд 6
Галогеноводородные кислоты
Образуются при растворении галогеноводородов в воде.
HF
HCl HBr HIФтороводородная
кислота
( плавиковая)
хлороводородная
кислота
(соляная)
бромоводородная
кислота
йодоводородная
кислота
Слайд 7
Оксокислоты
Хлорная – НСlO4
Сl2O7
Хлорноватая – НСlO3
Сl2O5 Хлористая – НСlO2 Сl2O3
Хлорноватистая- НСlO Сl2O
Слайд 9
Качественная реакция на галогенид - ионы
Взаимодействие с ионом
серебра: (AgNO3)
AgNO3 + KCl = KNO3 + AgCl (белый
)AgNO3 + KВr = KNO3 + AgBr(Светло-желтый)
AgNO3 + KI = KNO3 + AgI( желтый)
Слайд 10
Фтор F2
Открыт Муассаном в 1886 году электролизом
безводного фторида углерода Плавиковый
шпат
СаF2
Криолит:
Na3AlF6
Слайд 11
Соединения фтора
n(-CF2-CF2-)
Тефлон устойчив
к действию всех известных кислот и их смесей. Он
выдерживает температуры от -269 до +200°С.Плавиковая кислота:
HF
Разъедает стекло
Зарин и зоман-
Боевые отравляющие вещества
Слайд 12
Галит (NaCl )
Хлор
ДДТ (дихлородифенилтрихлорэтан)
KClO3 - Бертолетова соль.
2KClO3 +
3S = 2KСl + 3SO2↑.
Слайд 14
Получил Б.Куртуа. (1811 г)
2NaI + 2H2SO4 = I2
+ SO2↑ + Na2SO4 + 2H2O
3I2 + 5NH3 =
I3N∙NH3↓ + 3NH4↑.моноаммиакат нитрида трииода I3N∙NH3.
Йод





























