Слайд 2
Содержание
Классификация углеводов
Моносахариды
Нахождение в природе
Изомерия
Получение
Физические свойства
Химические свойства
Источники информации
Слайд 3
Классификация углеводов
Углеводы входят в состав клеток и тканей
всех растительных и животных организмов и по массе составляют
основную часть органического вещества на Земле. На долю углеводов приходится около 80% сухого вещества растений и около 20% животных. Растения синтезируют углеводы из неорганических соединений - углекислого газа и воды (СО2 и Н2О).
Углеводы делятся на три группы: моносахариды (монозы), дисахариды(биозы) и полисахариды (полиозы).
Слайд 4
Углеводы
Моносахариды
пентозы – рибоза C5H10O5, дезоксирибоза C5H10O4,
гексозы –
C6H12O6 глюкоза, фруктоза.
Дисахариды
Сахароза, мальтоза C12H22O11 .
Полисахариды
Крахмал, целлюлоза, гликоген, хитин
(C6H10O5 )n
Слайд 5
Моносахариды
Углеводы имеют общую формулу Cn(H2O)m.
Моносахариды являются гетерофункциональными соединениями.
В их молекулах одновременно содержатся и карбонильная (альдегидная или
кетонная) и несколько гидроксильных групп. В зависимости от этого моносахариды подразделяются на альдозы (в моносахариде содержится альдегидная группа) и кетозы (содержится кетогруппа).
Слайд 6
Нахождение в природе
В свободном виде глюкоза содержится почти
во всех органах зеленых растений. Особенно её много в
соке винограда, поэтому глюкозу иногда называют виноградным сахаром. Мёд в основном состоит из смеси глюкозы с фруктозой.
В организме человека глюкоза содержится в мышцах, в крови и в небольших количествах во всех клетках.
Слайд 7
Изомерия
Наиболее часто встречаются два моносахарида:
глюкоза и
фруктоза. Они являются изомерами и имеют
молекулярну
формулу С6H12O6.Глюкоза является альдегидоспиртом, а
фруктоза – кетоноспиртом.
глюкоза – это альдоза фруктоза – это кетоза
Слайд 8
Получение
В свободном виде в природе встречается преимущественно глюкоза.
Она же является структурной единицей многих полисахаридов. Другие моносахариды
в свободном состоянии встречаются редко и в основном известны как компоненты олиго- и полисахаридов. В природе глюкоза получается в результате реакции фотосинтеза:
6CO2 + 6H2O → C6H12O6(глюкоза) + 6O2
Слайд 9
Впервые глюкоза получена в 1811 году русским химиком
Г.Э.Кирхгофом при гидролизе крахмала.
Позже синтез моносахаридов из формальдегида
в щелочной среде предложен А.М.Бутлеровым.
O
|| Ca(OH)2
6 C–H → C6H12O6
|
H
Слайд 10
В промышленности глюкозу получают гидролизом крахмала в присутствии
серной кислоты.
H2SO4,t°
(C6H10O5)n + nH2O → nC6H12O6
крахмал глюкоза
Слайд 11
Физические свойства
Моносахариды – твердые вещества, легко растворимые
в воде, плохо – в спирте и совсем нерастворимые
в эфире. Водные растворы имеют нейтральную реакцию на лакмус. Большинство моносахаридов обладают сладким вкусом, однако меньшим, чем свекловичный сахар.
Слайд 12
Химические свойства
Моносахариды проявляют свойства спиртов и
карбонильных соединений.
Вещества, проявляющие характерные свойства двух
различных классов органических соединений,
имеют двойственную функцию.
Слайд 13
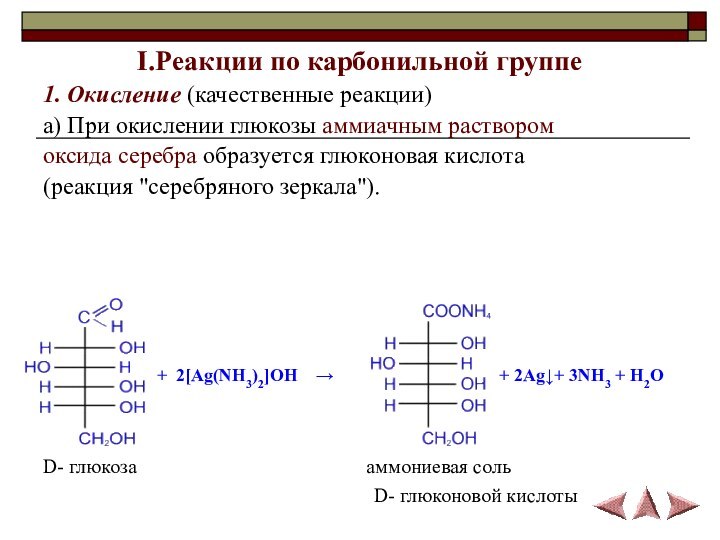
I.Реакции по карбонильной группе
1. Окисление (качественные реакции)
а) При
окислении глюкозы аммиачным раствором
оксида серебра образуется глюконовая кислота
(реакция "серебряного
зеркала").
D- глюкоза аммониевая соль
D- глюконовой кислоты
+ 2[Ag(NH3)2]OH →
+ 2Ag↓+ 3NH3 + H2O
Слайд 14
б) Реакция глюкозы с гидроксидом меди при
нагревании
так же приводит к образованию
глюконовой кислоты.
O O
// t //
CH2OH(CHOH)4 – C + Cu(OH)2 → CH2OH(CHOH)4 – C + CuOH ↓+ H2O
\ \ желтый
H OH
2CuOH → Cu2O↓ + H2O
красный
Слайд 15
2. Восстановление
Восстановление сахаров приводит к многоатомным
спиртам. В
качестве восстановителя используют
водород в присутствии никеля, алюмогидрид лития
и др.
Слайд 16
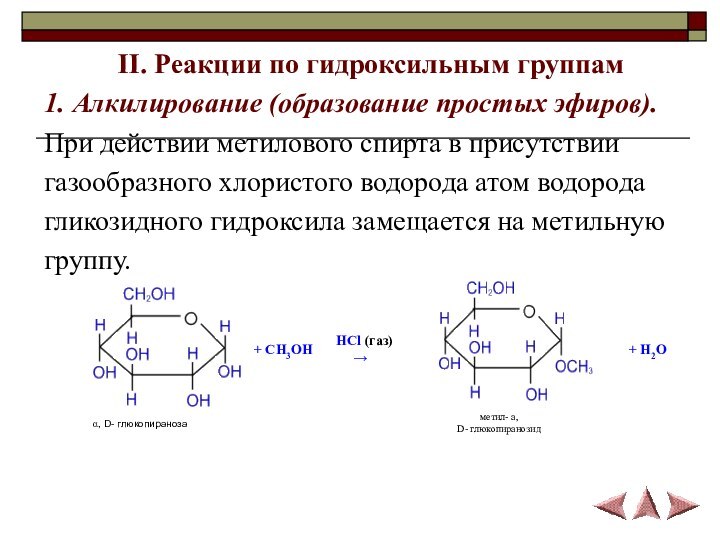
II. Реакции по гидроксильным группам
1. Алкилирование (образование простых эфиров).
При
действии метилового спирта в присутствии
газообразного хлористого водорода атом
водорода
гликозидного гидроксила замещается на метильную
группу.
Слайд 17
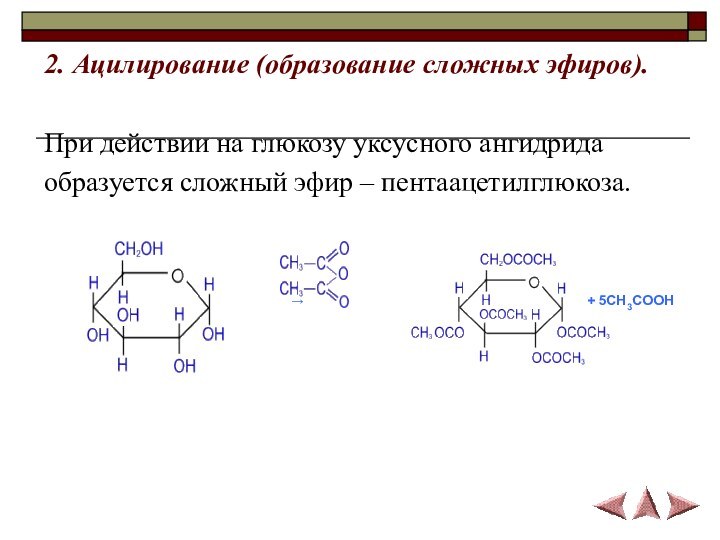
2. Ацилирование (образование сложных эфиров).
При действии на глюкозу
уксусного ангидрида
образуется сложный эфир – пентаацетилглюкоза.
Слайд 18
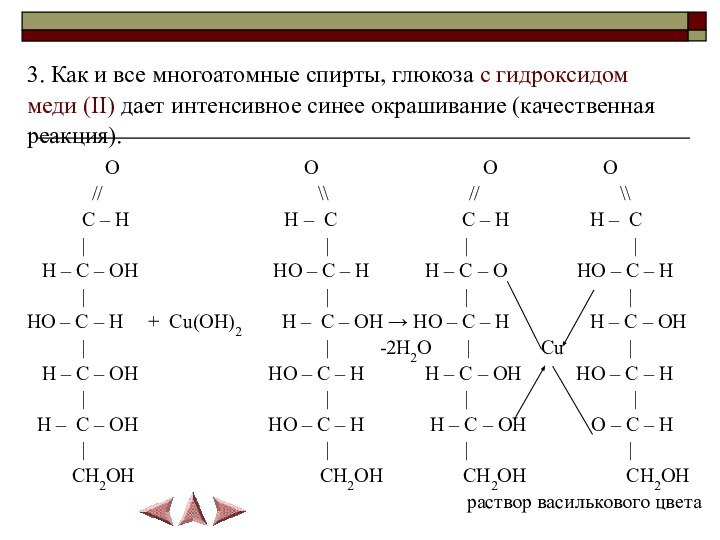
3. Как и все многоатомные спирты, глюкоза с
гидроксидом
меди (II) дает интенсивное синее окрашивание (качественная
реакция).
O O O O
// \\ // \\
C – H H – C C – H H – C
| | | |
H – C – OH HO – C – H H – C – O HO – C – H
| | | |
HO – C – H + Cu(OH)2 H – C – OH → HO – C – H H – C – OH
| | -2H2O | Cu |
H – C – OH HO – C – H H – C – OH HO – C – H
| | | |
H – C – OH HO – C – H H – C – OH O – C – H
| | | |
CH2OH CH2OH CH2OH CH2OH
раствор василькового цвета
Слайд 19
III. Специфические реакции
Глюкоза характеризуется и некоторыми
специфическими свойствами
– процессами
брожения. Брожением называется
расщепление молекул сахаров под воздействием
ферментов
(энзимов).
а) спиртовое брожение
C6H12O6 → 2C2H5OH + 2CO2
глюкоза этиловый спирт
Слайд 20
б) молочнокислое брожение
молочно-кислые
бактерии
C6H12O6 → 2 CH3 – CH – COOH
|
OH
молочная кислота
в) лимоннокислое брожение OH
[O] |
C6H12O6 → HOOC – CH2 – C – CH2 – COOH
грибки |
COOH
лимонная кислота
Слайд 21
г) маслянокислое брожение
масляно-кислые
бактерии
C6H12O6 → CH3 – CH2 – CH2 – COOH + 2H2O +2CO2
масляная кислота
Упомянутые виды брожения, вызываемые
микроорганизмами, имеют широкое практическое
значение. Например, спиртовое – для получения
этилового спирта, в виноделии, пивоварении и т.д.,
а молочнокислое – для получения молочной
кислоты и кисломолочных продуктов, лимоннокислое
- для получения лимонной кислоты.
Слайд 22
IV.Горение и разложение глюкозы.
Как все органические вещества, глюкоза
может гореть и разлагаться при
нагревании:
C6H12O6 + 6O2 → 6H2O + 6CO2
t
C6H12O6 → 6H2O + 6C
Слайд 23
Источники информации
1. Денисов В.Г. Химия. 10 класс. Поурочные
планы. – Волгоград: Учитель, 2004.
2. Аргишева А.И., Задумина
Э.А. Химия:
Подготовка к государственному
централизованному тестированию. – Саратов:
Лицей, 2002.
3. Петров А.А., Бальян Х.В., Трощенко А.Т.
Органическая химия. Учебник для вузов./ Под
ред. Петрова А.А. – М.: Высшая школа, 1981
Слайд 24
4. Хомченко Г.П. Пособие по химии для
поступающих
в вузы. – М.: ООО «Издательство
Новая Волна», 2002.
5. Курмашева К.К. Химия в таблицах и схемах.
Серия «Школа в клеточку». – М.: «Лист», 1997.
6. Потапов В.М., Чертков И.Н. Строение и
свойства органических веществ. Пособие для
учащихся 10 кл. – М.: Просвещение, 1980.
7. Штремплер Г.И. Тесты, вопросы и ответы по
химии: Книга для учащихя 8-11 классов
общеобразовательных учреждений. – М.:
Просвещение, 1999.