Слайд 2
Использование современных методов высококонформной лучевой терапии, в частности,

с модулированной интенсивностью пучка (IMRT) требует целого ряда мероприятий
для обеспечения гарантированной точности подведения дозы к мишени.
Наряду с гарантией качества терапевтических установок, в соответствии с современными представлениями необходима индивидуальная верификация каждого плана IMRT до начала его применения, которая требует целого ряда мероприятий для обеспечения гарантированной точности подведения дозы к мишени.
Методы IMRT значительно более сложны, чем обычное конформное облучение и требуют тесного сотрудничества и экспертных знаний соответственно обученной мультидисциплинарной команды, включающей радиационных онкологов, медицинских физиков, дозиметристов и радиационных технологов.
В рекомендациях МАГАТЭ подчеркивается, что переходить к освоению IMRT следует только тогда, когда имеется достаточный опыт 3-D конформной лучевой терапии с контролем повторяемости положения пациента при укладке, т.е. IGRT.
Введение
Слайд 3
Введение
В 2015 году в РНЦРР была внедрена
технология IMRT на трех терапевтических установках: ускорителе TrueBeam (фотонные
пучки 6, 10FFF и 15 МВ) и двух ускорителях UNIQUE (6 МВ). Оптимизация облучения и расчет дозы проводился с использованием системы планирования лучевой терапии Eclipse, хранение, передача и реализация планов – с помощью компонент радиологической информационной системы Aria.
Для верификации индивидуальных планов пациентов были разработаны, опробованы и внедрены пять различных методов, описываемых ниже. Оценены достоинства и недостатки каждого из них, необходимые ресурсы и временные затраты, особенности использования оборудования.
Слайд 4
Материалы и методы
Основой большинства методов верификации планов
IMRT является создание т.н. верификационного плана путем замены реального
тела пациента моделирующим его фантомом с размещенными внутри дозиметрическими детекторами, позволяющими измерять распределение дозы в точке или плоскости.
Измеренное в процессе реализации верификационного плана распределение дозы сравнивается затем с расчетным с помощью метода гамма-анализа, предложенного в работе [3] и являющимся в настоящее время общемировым стандартом. Для каждой точки измерения дозы с радиус-вектором рассчитывается параметр гамма в виде:
Точка считается прошедшей тест, если и не прошедшей, если . Критерием успешной верификации плана является успешное прохождение теста не менее 95% всех точек измерения.
Слайд 5
Материалы и методы
Для верификации планов использовалась матрица MapCHECK
2 (Sun Neclear Corporation, США), содержащая 1527 диодов, расположенных
на регулярной сетке с программным обеспечением SCN Patient для анализа результатов. Матрица использовалась либо в верификационном водно-эквивалентном фантоме MapPHAN MC2 (рис 1), либо в устройстве изоцентрической центрации IMF с дополнительно установленной сверху пластиной водно-эквивалентного материала Virtual Water толщиной 5 см (рис. 3).
Для непосредственного измерения дозы в пластинчатом твердотельном фантоме Virtual Water использовалась ионизационная камера 31010 (PTW Freiburg, Германия) с клиническим дозиметром SuperMax (Standard Imaging, США) и радиохромная дозиметрическая пленка Gafchromic EBT2. Сканирование пленки осуществлялось на сканере Epson V700, а дальнейшая обработка (расчет оптической плотности, дозы, проведение гамма-анализа) – с помощью программы DoseLab версии 6.50 (Mobius Medical Sysytems, США).
Слайд 6
Метод 1. Верификация с помощью матрицы MapCheck 2

в фантоме MapPHAN.
Предварительно, до проведения верификации плана матрица
должна быть калибрована на пучке соответствующего качества в соответствии с требованиями ее документации [2], а поправочные коэффициенты для каждого детектора и результаты абсолютной калибровки должны быть загружены в управляющую программу SNC Patient.
Для подготовки верификационного плана необходимо заменить набор КТ-сканов пациента, для которого рассчитан рабочий план облучения, набором сканов верификационного фантома с помещенной внутри нее матрицей MapCHECK 2. Далее угол поворота гантри устанавливается в нулевое значение таким образом, чтобы плоскость расположения диодов была всегда перпендикулярна оси пучка, рассчитываются и экспортируются в формате DICOM RT Dose распределения дозы в этой плоскости.
Матрица и фантом устанавливаются на столе ускорителя как показано на рис.1 и подключается к управляющему компьютеру с установленным программным обеспечением SNC Patient через интерфейсный модуль PDI 2.0.
Слайд 7
Метод 1. Верификация с помощью матрицы MapCheck 2
в фантоме MapPHAN.
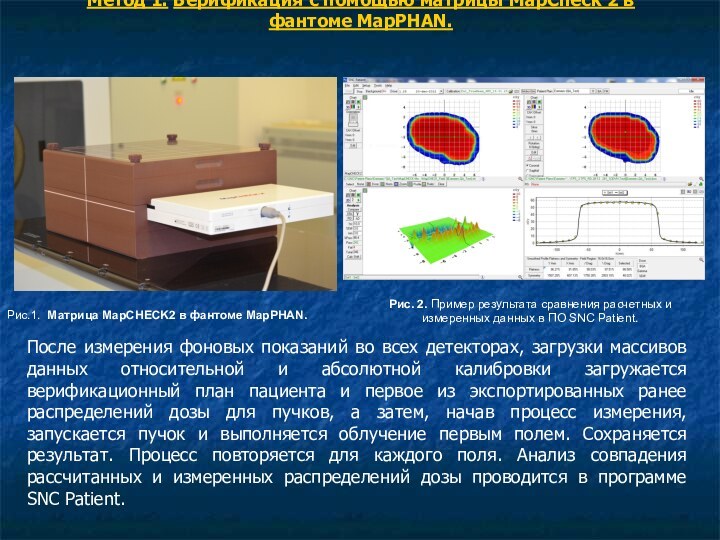
Рис.1. Матрица MapCHECK2 в фантоме MapPHAN.
Рис. 2.
Пример результата сравнения расчетных и измеренных данных в ПО SNC Patient.
После измерения фоновых показаний во всех детекторах, загрузки массивов данных относительной и абсолютной калибровки загружается верификационный план пациента и первое из экспортированных ранее распределений дозы для пучков, а затем, начав процесс измерения, запускается пучок и выполняется облучение первым полем. Сохраняется результат. Процесс повторяется для каждого поля. Анализ совпадения рассчитанных и измеренных распределений дозы проводится в программе SNC Patient.
Слайд 8
Метод 1. Верификация с помощью матрицы MapCheck 2
в фантоме MapPHAN.
Достоинства метода:
оценка соответствия поглощенной дозы в
плоскости, сравнение абсолютных значений;
размер фантома приближается к размеру соответствующей области тела пациента, обеспечивается учет рассеянного излучения, близкий к реальному.
Анализ результатов проводится немедленно после завершения измерения.
Матрица работает также и для пучков в режиме FFF.
Недостатки метода:
Не учитывается влияние гравитации на движение лепестков, поскольку гантри находится в нулевом (вертикальном положении).
Необходимо учитывать температурную зависимость матрицы приблизительно 0,6%/градус, загружать калибровочные значения, полученные для близкой температуры.
Невозможно облучения матрицы при других углах поворота гантри, кроме нулевого, вследствие самоэкранирования внутренних конструктивных элементов матрицы.
Слайд 9
Метод 2. Матрица MapCheck 2 в устройстве IMF.
Измерения
дозы проводятся с помощью матрицы диодов MapCHECK 2, но
она помещается не внутрь верификационного фантома, а устанавливается в устройстве изоцентрической центрации IMF (рис.3). Сверху матрица покрывается пластиной Virtual Water толщиной 5 см для обеспечения рассеяния.
Таким образом, общая толщина пластика до плоскости диодов составляет 7 см воды, а конструкция устройства обеспечивает позиционирование этой плоскости в изоцентре. Матрица с пластиной, таким образом, может вращаться вместе с гантри, а метод включает учет влияния гравитации на движения лепестков.
Рис. 3. Устройство IMF с матрицей MapCHECK 2.
Слайд 10
Метод 2. Матрица MapCheck 2 в устройстве IMF.

Подготовка верификационного плана аналогична предыдущему варианту, но проводится бес
сброса угла поворота гантри в ноль, а КТ-срезы пациента подменяются на данные матрицы с наложенной сверху пластиной Virtual Water.
Также и при проведении измерений единственным отличием является тот факт, что матрица и пластина вращаются вместе с гантри.
Обработка результатов полностью аналогична случаю матрицы в фантоме, проводится в программе SNC Patient на основе гамма-анализа с критерием 3%/3 мм и установленным порогом 10% от максимального значения дозы.
Достоинства метода:
По сравнению с предыдущим методом учтено воздействие гравитации на положения и скорости перемещения лепестков МЛК.
Недостатки метода:
В связи с ограничением нагрузки на гантри полноценный верификационный фантом заменен на водно-эквивалетную пластину толщиной 5 см. Это менее реалистичная модель человеческого тела, имеющая существенно меньший вклад рассеяния.
При горизонтальных положениях гантри (вблизи углов 90 и 270 градусов) наблюдается провис устройства около 1 мм, что вносит дополнительную погрешность в результаты измерений.
Метод более трудоемок и требует больших затрат времени.
Слайд 11
Метод 3. Измерения в фантоме Virtual Water с

помощью ионизационной камеры и пленки Gafchromic EBT2
Для верификации плана
данным методом используется водно-эквивалентный пластинчатый твердотельный фантом из материала Virtual Water в качестве модели тела пациента, для оценки пространственного распределения (относительной дозиметрии) используется самопроявляющаяся пленка Gafchromic EBT2, а для измерения абсолютной дозы в изоцентре – ионизационная камера PTW 31010. До проведения верификации плана самопроявляющаяся пленка Gafchromic из используемой партии должна быть калибрована на пучке соответствующего качества в соответствии с требованиями [8,9].
При создании верификационного плана данные КТ пациента заменяются на полученные предварительно данные КТ для фантома Virtual Water. Лист пленки размещается внутри фантома на 1 см выше изоцентра, непосредственно в изоцентр помещается ионизационная камера. Все углы поворота гантри и коллиматора устанавливаются в ноль.
Полость камеры на данных КТ оконтуривается, оформляется в виде структуры и заполняется водно-эквивалентной средой. В качестве контрольного значения рассчитывается доза, усредненная по объему структуры камеры, поскольку для сильно модулированного поля неточечность объема камеры должна быть учтена.
Слайд 12
Метод 3. Измерения в фантоме Virtual Water с
помощью ионизационной камеры и пленки Gafchromic EBT2
Рис. 4. Размещение
пленки Gafchromic на адаптерной пластине фантома Virtual Water: а – установка фантома и фиксация пленки; б – разметка осей на пленке.
Рис. 5. Фантом Virtual Water в сборе с пленкой Gafchromic и ионизационной камерой: а – установка верхних пластин фантома; б – фантом с камерой в сборке
При проведении измерений для каждого поля между пластинами фиксируется лист пленки Gafchromic EBT2 (рис.4 и 5), по кресту светового поля на краях пленки отмечаются оси координат (рис.4б), покрываются сверху остальными пластинами (рис 5б) и облучаются на ускорителе в соответствии с верификационным планом .
Слайд 13
Метод 3. Измерения в фантоме Virtual Water с

помощью ионизационной камеры и пленки Gafchromic EBT2
Поскольку сразу после
облучения оптическая плотность пленки изменяется и выходит на стабильный уровень только через 48 часов. Калибровка пленки должна также проводиться через этот срок после облучения.
После этого пленку необходимо отсканировать на сканере, обеспечивающим интервал оптических плотностей. В нашем случае использовался сканер Epson V700, обеспечивающий сканирование пленки на просвет в указанном интервале плотностей, для дальнейшей обработки использовалась программа Doselab 6.50 (Mobius Medical Systems).
Важно чтобы сканирование происходило в той же ориентации, что и сканирование калибровочных образцов и в том же положении на стекле сканера, поскольку отклик сканера линейки сканера зависит от этого положения, а также отсканировать необлученную пленку – с нулевой дозой, необходимую для расчета оптической плотности.
Для повышения точности в качестве необлученных образцов желательно использовать эти же листы пленки до проведения облучения – тогда появляется возможность учесть неоднородность эмульсии на пленке.
Полученные данные сохраняются в формате TIFF RGB 48 бит/пиксел, преобразуются к оптической плотности и далее – к распределению поглощенной дозы (рис.6).
Слайд 14
Метод 3. Измерения в фантоме Virtual Water с
помощью ионизационной камеры и пленки Gafchromic EBT2
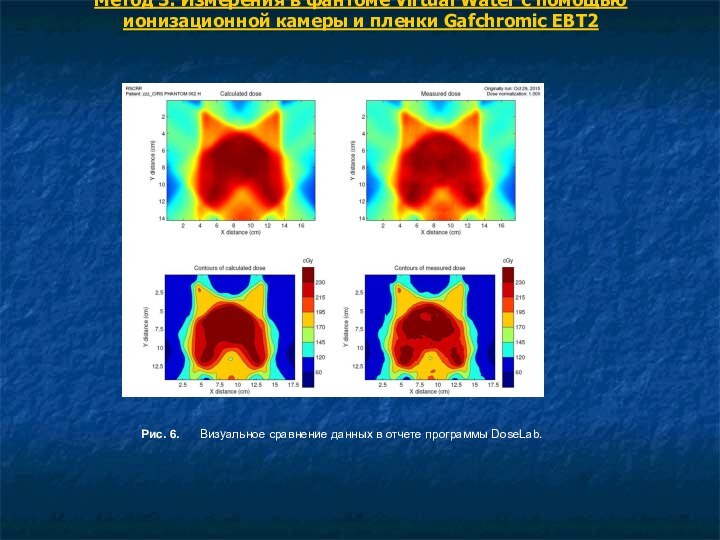
Рис. 6.
Визуальное сравнение данных в отчете программы DoseLab.
Слайд 15
Метод 3. Измерения в фантоме Virtual Water с
помощью ионизационной камеры и пленки Gafchromic EBT2
Рис. 7. Сравнение
результатов расчета и измерений в
ПО DoseLab. Окно Measured Image Rotation.
Сравнение с экспортированным распределением дозы из системы проводится как и ранее с помощью гамма-анализа с критерием 3%/3 мм в относительном режиме, абсолютные значения дозы сравниваются по показаниям ионизационной камеры. Поскольку пленка имеет существенное лучшее пространственное разрешение по сравнению с матрицей диодов, имеется возможность анализа распределений в увеличенном виде (рис.7), анализ профилей дозы (рис.8), расчет распределение гамма-индекса в плоскости измерения (рис.9 ), построение гистограмм гамма-индекса (рис.10).
Рис. 8. Сравнение результатов расчета и измерений в ПО DoseLab. Окно Manual Image Registration.
Слайд 16
Метод 3. Измерения в фантоме Virtual Water с
помощью ионизационной камеры и пленки Gafchromic EBT2
Рис. 9. Сравнение
результатов расчета и измерений в ПО DoseLab. Распределение гамма-индекса в отчете программы DoseLab.
Рис. 10. Сравнение результатов расчета и измерений в ПО DoseLab. Гистограммы гамма-анализа в отчете программы DoseLab.
Рис. 10. Сравнение результатов расчета и измерений в ПО DoseLab. Гистограммы гамма-анализа в отчете программы DoseLab.
Достоинства метода:
Измерение двумерного распределения поглощенной дозы с высоким пространственным разрешением.
Абсолютные измерения поглощенной дозы ионизационной камерой.
Недостатки метода:
Необходимость выдержки пленки после облучения делает метод малопригодным для оперативной верификации планов.
Высокая трудоемкость метода не позволяет обеспечить верификацией сколько-нибудь существенный поток пациентов.
Требуется постоянный расход дорогостоящей пленки Gafchromic ($75-300 на пациента).
Слайд 17
Метод 4. Верификация планов IMRT с помощью средств
портальной визуализации в режиме портальной дозиметрии.
При использовании метода портальной
дозиметрии должен быть в соответствии с требованиями документации [10] калиброван мегавольтный портальный детектор и настроен алгоритм PDIP в системе планирования Eclipse.
Регистрация флюенса модулированного поля проводится с помощью портального детектора, помещенного вблизи изоцентра (как правило, на 5 см ниже изоцентра). Пациент или заменяющий его фантом отсутствует, регистрируется не доза, а флюенс (распределение интенсивности в пучке излучения). Угол вращения гантри соответствует реальному, поэтому влияние гравитации на движение лепестков многолепесткового коллиматора учитывается в полной мере.
Измеренные распределения дозы сравниваются с рассчитанными в системе Eclipse, как и ранее, с помощью гамма-анализа с критерием 3 %/3 мм и порогом 10%. Для обработки данных используется штатная программа Portal Dosimetry из системы Aria.
Слайд 18
Метод 4. Верификация планов IMRT с помощью средств
портальной визуализации в режиме портальной дозиметрии.
Достоинства метода:
Быстрый и простой
метод верификации.
Учитывается влияние гравитации на движение лепестков МЛК.
Недостатки метода:
Не учитывает дозу в пациенте (фантоме), проводится только верификация флюенса.
Необходима покупка лицензии Varian на технологию, калибровка детектора (радиационный выход для прямоугольных полей), настройка расчетного алгоритма в системе Eclipse.
Рис.11. Использование мегавольтного портального детектора для верификации планов IMRT.
Слайд 19
Метод 5. Верификация планов IMRTна основе анализа файлов

Dynalog и лог-файлов траекторий ускорителя TrueBeam.
Ускорители Varian UNIQUE позволяют
сохранять на жестком диске для дальнейшего анализа файлы DynaLog, содержащие протокол реализации плана лечения пациента, включая координаты каждого из лепестков многолесткового коллиматора в контрольных точках. Анализ файлов DynaLog позволяет оценить точность реализации плана и, в частности, погрешности движения лепестков относительно планируемых значений.
Для ускорителей TrueBeam имеются файлы аналогичного назначения, но отличающиеся по формату и названию – лог-файлы траекторий.
Использование файлов DynaLog или файлов траекторий не требует специальной подготовки верификационного плана – достаточно использовать лечебный план в режиме QA – при этом полученные за верификацию дозы не будут добавлены к данным пациента.
Анализ результатов верификации на ускорителе UNIQUE проводится с помощью программы DynalogFileViewer (рис.12,13,14), которая выводит в графическом и табличном виде гистограмму ошибок положения лепестков во время выполнения плана, а также среднекваратичные ошибки для каждого лепестка. Эти данные могут также быть использованы для оценки состояния двигателей лепестков МЛК и ранней диагностики возможной поломки.
Слайд 20
Метод 5. Верификация планов IMRTна основе анализа файлов
Dynalog и лог-файлов траекторий ускорителя TrueBeam.
Рис. 12. Верификация на
основе файлов Dynalog. Таблицы (а) и гистограммы (б) распределения ошибок положения лепестков в контрольных точках.
Рис. 13. Верификация на основе файлов Dynalog. Таблица (а) и график (б) среднеквадратичной ошибки положения каждого лепестка для банков A и B в процессе выполнения плана.
Слайд 21
Метод 5. Верификация планов IMRTна основе анализа файлов
Dynalog и лог-файлов траекторий ускорителя TrueBeam.
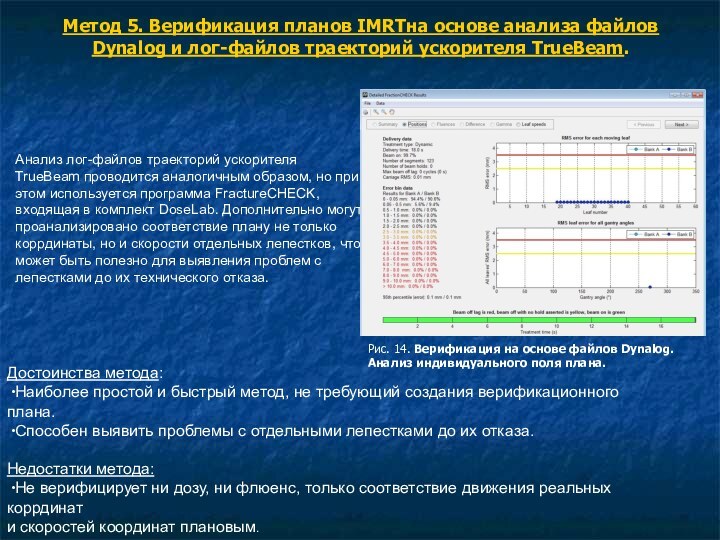
Анализ лог-файлов траекторий ускорителя
TrueBeam проводится аналогичным образом, но при этом используется программа FractureCHECK, входящая в комплект DoseLab. Дополнительно могут проанализировано соответствие плану не только коррдинаты, но и скорости отдельных лепестков, что может быть полезно для выявления проблем с лепестками до их технического отказа.
Достоинства метода:
Наиболее простой и быстрый метод, не требующий создания верификационного плана.
Способен выявить проблемы с отдельными лепестками до их отказа.
Недостатки метода:
Не верифицирует ни дозу, ни флюенс, только соответствие движения реальных коррдинат
и скоростей координат плановым.
Рис. 14. Верификация на основе файлов Dynalog. Анализ индивидуального поля плана.
Слайд 22
Выводы:
Контроль с помощью файлов Dynalog – быстрый, простой,

не требует вообще создания верификационного плана, характеризует состояние ускорителя
и рекомендуется к постоянному применению.
Верификация в фантоме с помощью пленки Gafchomic и ионизационной камеры для постоянного использования практически непригодна: необходимость выдержки двое суток после облучения, трудоемкость, затраты пленки по количеству полей. Наиболее рационально использовать этот метод для end-to-end test – верификации всей цепочки IMRT в антропоморфном фантоме.
Верификация с помощью матрицы MapCHECK 2 в фантоме MapPHAN на наш взгляд является хорошим компромиссом между учитываемыми эффектами и производительностью и наиболее часто используемым методом верификации планов в IMRT.
Метод портальной дозиметрии – второй по применимости в РНЦРР, незаменим при необходимости быстрой и оперативной верификации (за 5-10 минут времени на ускорителе). Может быть комбинирован с записью и последующим анализом файлов Dynalog.
Матрица MapCHEK 2 в устройстве изоцентрической центрации IMF – не имеет существенных преимуществ перед матрицей в фантоме, но более трудоемок и вносит дополнительные геометрические погрешности за счет прогиба устройства. Редко используется для верификации планов IMRT, но является основным методом верификации для внедряемой в РНЦРР технологии RapidArc.
По всем методам верификации разработаны детальные методические рекомендации, пошагово описывающие технологию выполнения процедур. С ними можно ознакомиться по запросу.