- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Клеточный цикл и его регуляция
Содержание
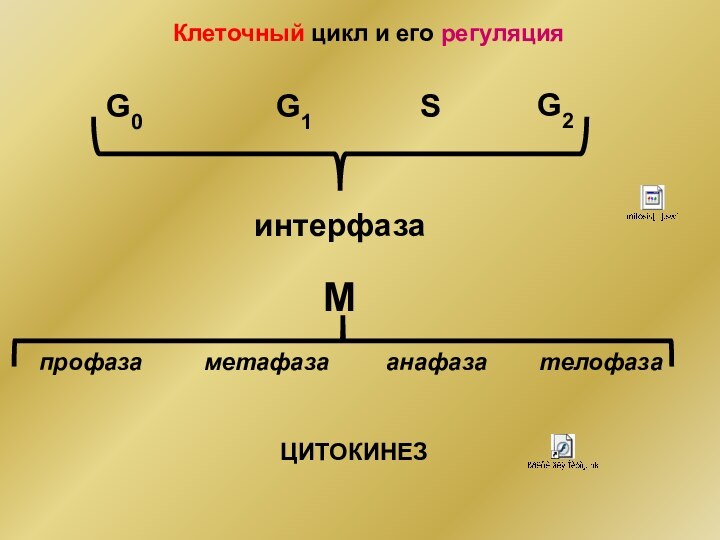
- 2. Клеточный цикл и его регуляцияG0G1SG2Mинтерфаза профаза метафаза анафаза телофаза ЦИТОКИНЕЗ
- 3. G0G1G2SMхарактеризуется экспрессией генов и синтезом белков. Клетка
- 4. прохождение цикла обеспечивается последовательной сменой активированных cyclin-зависимых
- 5. G0G1SMcyclin E Cdk2 пресинтетическаяпостсинтетическаясинтез ДНКмитозcyclin В Cdс2
- 6. В регуляции активности checkpoint задействованы три группы
- 7. Три гена отслеживают повреждение ДНК в checkpoint:регулирует
- 8. Клеточный цикл регулируется не только внутриклеточ- ными,
- 9. КАНЦЕРОГЕНЕЗ многоступенчатый процесс накопления мутаций и других
- 10. химические канцерогены: бензпирен и диметилбензантрацен, нитрозамины; многие
- 11. вирусы - индуцируют опухоли (возникновение лейкозов связана
- 12. ТЕОРИИ КАНЦЕРОГЕНЕЗА Мутационная теория канцерогенеза Развитие опухолевого
- 13. Процесс непосредственного действия канцерогена на клетки, запускающий
- 14. Трансформированные клетки характеризуются:нарушением дифференцировкиклоны клеток, как бы
- 15. ослаблением адгезивных свойствнарушение клеточной адгезии и подвижности
- 16. дефектами апоптозадля опухолевых клеток характерно ослабление обоих
- 17. Иммунологический атипизм - появление в опухолях белков,
- 18. ПРОМОЦИЯ Мутации могут проявляться при воздействии опухолевого
- 19. ОПУХОЛЕВАЯ ПРОГРЕССИЯ процесс малигнизации опухоли, в основе
- 20. Генетическая нестабильность популяций опухолевых клеток складывается из
- 21. качественные изменения в ходе опухолевого роста представляют
- 22. ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТУничтожение трансформированных клеток с помощью клеточных
- 23. Эффекторные механизмы противоопухолевого иммунитетаНеспецифические ФНОα, ИФγ, ИЛ-2 Тh1CD4+NKCD56/CD57 К.-М.перфориныперфориныАЗКЦ NKК.-М.
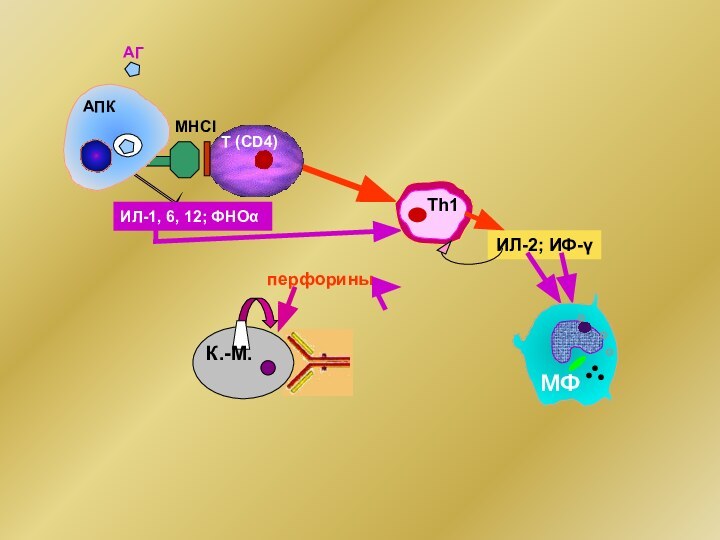
- 24. МНСIАГИЛ-1, 6, 12; ФНОα ИЛ-2; ИФ-γАПКТ (CD4) Тh1перфориныК.-М.МФ
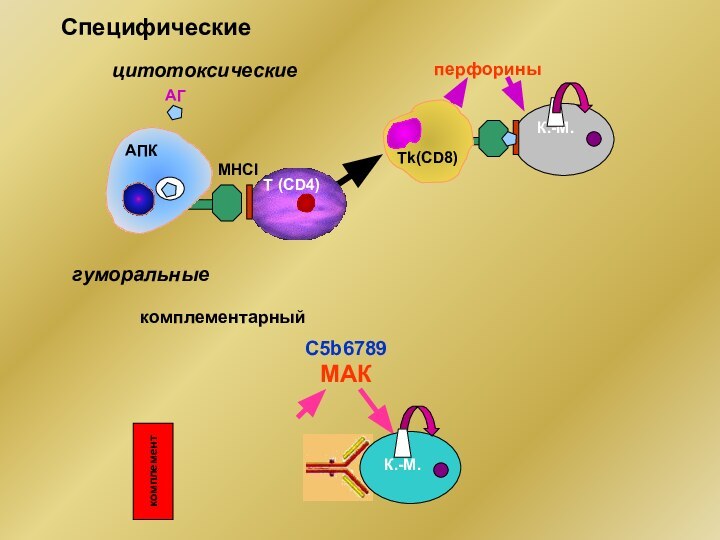
- 25. Специфические МНСIАГК.-М.АПКТ (CD4) Тk(CD8) перфориныцитотоксические гуморальные C5b6789 МАКкомплементарный К.-М.комплемент
- 26. ВЛИЯНИЕ ОПУХОЛИ НА ОРГАНИЗММестные обусловлены характером роста опухолиэкспансивный рост
- 27. инфильтративный рост аппозиционный рост происходит за счет
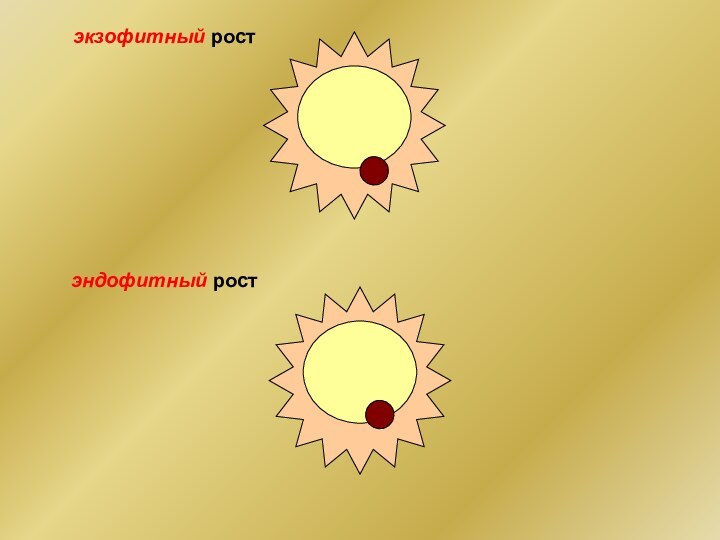
- 28. экзофитный рост эндофитный рост
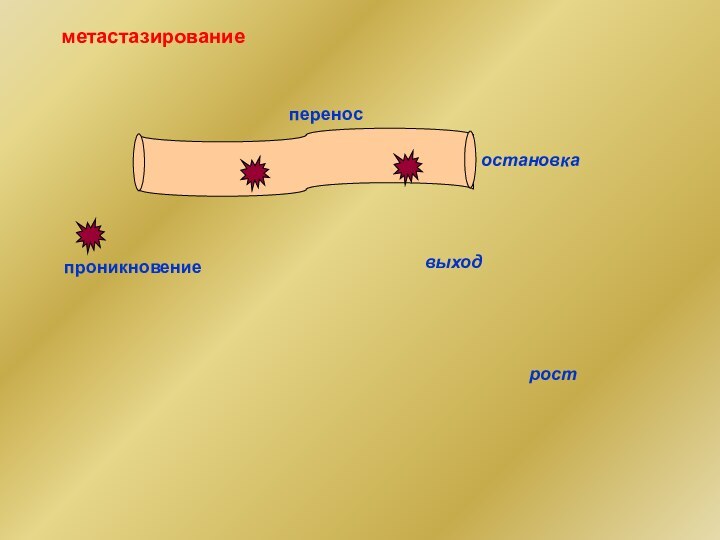
- 29. метастазирование проникновение перенос остановка выход рост
- 30. ПАРАНЕОПЛАСТИЧЕСКИЙ СИНДРОМ дистанционное (системное) воздействие новообразования, не
- 31. Скачать презентацию
- 32. Похожие презентации
























Слайд 3
G0
G1
G2
S
M
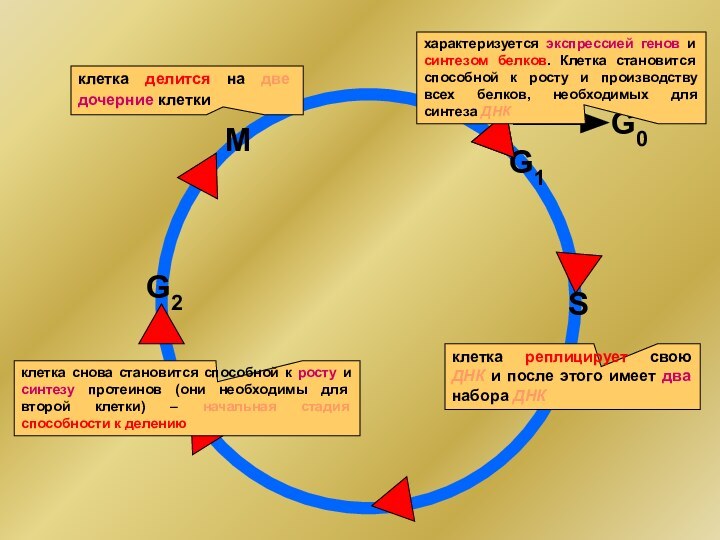
характеризуется экспрессией генов и синтезом белков. Клетка становится
способной к росту и производству всех белков, необходимых для
синтеза ДНКклетка реплицирует свою ДНК и после этого имеет два набора ДНК
клетка снова становится способной к росту и синтезу протеинов (они необходимы для второй клетки) – начальная стадия способности к делению
клетка делится на две дочерние клетки
Слайд 4
прохождение цикла обеспечивается последовательной сменой активированных cyclin-зависимых киназ,
для активации которых необходимо присутствие соответствующей активаторной субъединицы -
циклинаcyclin+Cdk фосфорилируют регуляторные белки, контролирующие протекание данной фазы клеточного цикла. Обратимое фосфорилирование / дефосфорилирование регуляторных белков - основа регуляции клеточного цикла
Слайд 5
G0
G1
S
M
cyclin E
Cdk2
пресинтетическая
постсинтетическая
синтез ДНК
митоз
cyclin В
Cdс2
Точки
контроля checkpoint
G2
G1/S
checkpoint
проверка целостности ДНК
готовность к репликации S
checkpoint
G2/М
checkpoint
проверка завершенности репликации ДНК
cyclin E/S
Cdk
системы передачи внутриклеточ- ных сигналов, с помощью которых клетка контролирует завершение одних событий цикла и готовность инициировать следующие. Определяют те стадии клеточного цикла, на которых осуществляется задержка прохождения по циклу в ответ на нарушение
Точка рестрикции R-point
стадия клеточного цикла, на которой клетка чувствительна к действию ФР
Слайд 6
В регуляции активности checkpoint задействованы три группы генов,
кодирующих:
1) белки-сенсоры, которые контролируют завершение событий клеточного цикла
2) сигналы,
посылаемые этими сенсорами3) эффекторы - ответные элементы, которые принимают сигналы и осуществляют задержку движения клеток по циклу
Сheckpoint репликации ДНК – это переход из S/G2 и/или поздняя часть G2, блокирует переход в М фазу. G2 очень короткая, если репликация ДНК не завершена G2 фаза удлиняется
В этой точке включаются механизмы, реагирующие на повреждение ДНК остановкой клеточного цикла на время, необходимое для репарации и активации транскрипции генов, ответственных за репарацию ДНК. Ключевыми компонентами этой системы являются опухолевые гены-супрессоры
Слайд 7
Три гена отслеживают повреждение ДНК в checkpoint:
регулирует активность
E2F-DP, фактора транскрипции cyclin A, E и Cdk1. Активность
E2F-DP - один из основных механизмов контроля входа в S-фазу и М-фазуопухолевый ген-супрессор - белок BRCA
ген p53 опухоль-супрессирующий ген
p53 - фактор транскрипции. Он регулирует экспрессию более 10 белков, ответственных за активацию различных супрессорных систем. Среди них - индукторы апоптоза, регуляторы клеточного цикла, секретируемые ингибиторы роста
Остановка клеточного цикла при повреждениях ДНК в G1 обеспечивается ингибированием cyclin-Cdk, в G2 - инактивацией комплекса cyclin B-Сdk1
опухолевый ген-супрессор pRb
играет важную роль в системе G1- и G2- checkpoint
Мутации, инактивирующие гены-супрессоры, способствуют тому, что поврежденная ДНК сохраняет способность к репликации. Это ведет к нарушению генетической стабильности клетки
Слайд 8
Клеточный цикл регулируется не только внутриклеточ- ными, но
также и внешними факторами. ФР и состояние внеклеточного матрикса
детерминируют пролиферациюФР связывает с белком-рецептором на клетке, которая должна делиться. Он взаимодействует с рецептором, активизируя его. Активизированный ФР рецептор или является Пк, или активизирует Пк. Запускается киназный каскад. В итоге активизируется фактор транскрипции и экспрессируется один или несколько генов, контролирующих выход из G0-фазы, возвращение в G1-фазу, и переход в S-фазу
Слайд 9
КАНЦЕРОГЕНЕЗ
многоступенчатый процесс накопления мутаций и других генетических
изменений, приводящих к нарушениям регуляции клеточного цикла (гиперактивация стимуляторов
клеточного цикла и инактивация супрессоров), апоптоза, дифференцировки, движения и морфогенетических реакций клетки, а также контроля за целостностью геномаВ число наиболее важных факторов (канцерогенов) онкогенеза включают:
1) химические (приблизительно 90% опухолей)
2) физические
3) онкогенные вирусы
Слайд 10
химические канцерогены: бензпирен и диметилбензантрацен, нитрозамины; многие инсектициды
и гербициды, полициклические ароматические углеводороды; цикламаты и сахарин, азокрасители,
асбест; курение сигарет, жевание бетельного листа и бетельного ореха. Некоторые химические соединения - проканцерогены в организме превращаются в активные формы (например, эпоксиды)КАНЦЕРОГЕННЫЕ ВЕЩЕСТВА
физический канцерогены: действие высокой температуры, механического трения, УФО и космическое излучение радиоактивные изотопы (с длинным периодом полураспада и нейтронным излучением)
экзогенные канцерогены находятся во внешней среде:
Слайд 11
вирусы - индуцируют опухоли (возникновение лейкозов связана с
РНК -содержащими вирусами, а другие опухоли вызываются ДНК-содержащими). Из
ферментов онковирусов важнейшим является РНК-зависимая-ДНК-полимераза (обратная транскриптаза, ревертаза), которая способна синтезировать молекулу ДНК, комплиментарную вирусной РНК. При вирусном канцерогенезе предполагается интеграция ДНК из генома с молекулами ДНК клетки-хозяина. При активации они встраиваются в геном клетки-хозяина и синтезируют ДНК, включающую безудержную пролиферацию клетокэндогенные канцерогены - вещества, выполняющие в организме определенную полезную функцию, но при определенных условиях способны вызывать опухолевую трансформацию. Это стероидные гормоны (особенно эстрогены), холестерин, витамин Д, продукты превращения триптофана, лекарственные препараты (цитостатики, йодконтрастные соединения, искусственные гормональные препараты и многие другие)
Слайд 12
ТЕОРИИ КАНЦЕРОГЕНЕЗА
Мутационная теория канцерогенеза
Развитие опухолевого процесса
- следствие мутации. Химические канцерогенные вещества, излучения вызывают мутационный
процесс - изменяется геном, изменяется структура клеток, идет малигнизацияЭпигеномная теория канцерогенеза
В основе эпигеномного механизма лежит депрессия активных генов и дерепрессия в норме неактивных генов. Основой опухолевого процесса по этой теории является дерепрессия древних генов
Вирусная теория канцерогенеза
Вирус встраивается в клеточный геном, внося дополнительную информацию в клетку, вызывая нарушение генома и нарушение жизнедеятельности клетки
Все эти теории легли в основу современной теории экспрессии онкогенов
Слайд 13
Процесс непосредственного действия канцерогена на клетки, запускающий их
трансформацию, называется инициацией опухолевого роста
Опухолевая трансформация - это изменения
структуры клеточной ДНК, известные как мутации. Мутации изменяют информацию, которую несут гены, вовлеченные в регулирование роста клетки, деления и дифференцированияМутации одного гена (протоонкогены) обычно вызывает только частичную трансформацию. Полная опухолевая трансформация требует сочетанных генных мутаций
Протоонкогены - это нормальные клеточные гены, гиперэкспрессия или модификация функции которых делает их онкогенами. Биологическая роль многих протоонкогенов - стимуляция клеточного цикла. Гиперактивация некоторых из них способна ослаблять работу checkpoint, контролирующих повреждения ДНК
Биологическая роль многих протоонкогенов - стимуляция клеточного цикла. Их белковые продукты повышают активность циклинзависимых киназ, ответственных за начальные этапы пресинтетической фазы G1 и переход из G1 в фазу синтеза ДНК - S. Некоторые протоонкогены регулируют активность комплексов cyclin А+Сdk2 для репликации ДНК и cyclin B+Cdk1 для перехода из G2 в М. Протоонкогены являются компонентами сигнальных путей, передающих в ядро митогенные сигналы от различных ФР.
Слайд 14
Трансформированные клетки характеризуются:
нарушением дифференцировки
клоны клеток, как бы "заморожены"
на той или иной стадии созревания, они происходят из
незрелых клеток, в которых блокированы процессы дальнейшей дифференцировкиотсутствием контактного торможения
нарушается контактная регуляция размножения. клетки, взвешенные в вязкой среде, продолжают размножаться без прикрепления к подложке, все морфогенетические реакции на контакты с другими клетками и подложкой. Трансформированные клетки делают меньше матрикса, хуже прикрепляются к матриксу, подложке и другим клеткам. Крайние изменения способности к морфогенетическим реакциям и построению тканей обусловливают наиболее опасные свойства опухолевых клеток - способность к врастанию в нормальные ткани (инвазия) и к образованию колоний в других органах (метастазирование)
Слайд 15
ослаблением адгезивных свойств
нарушение клеточной адгезии и подвижности играет
фундаментальную роль в инициации канцерогенеза. Нарушения адгезионных сил возникает
между клетками, клеткой и компонентами внеклеточного матрикса. Эти нарушения играют важную роль, когда от опухоли отделяются клетки и начинается процесс метастазированиянеопределенно долгим делением без признаков старения (иммортализация)
отсутствие в опухолевых клетках человека репликативного старения (иммортализация) связано с включением специального механизма. В его основе лежит способность специфического фермента теломеразы достраивать недореплицированные теломерные повторы и поддерживать, таким образом, их постоянную длину. существенный вклад в иммортализацию вносят нарушениями работы охранных механизмов, осуществляющих остановку клеточного цикла при нарушения структуры ДНК
Слайд 16
дефектами апоптоза
для опухолевых клеток характерно ослабление обоих путей
индукции апоптоза. Обнаруживаются:
- потеря экспрессии на поверхности клетки
рецептора смерти Fasнарушения проведения апоптогенного сигнала к МХ
блокирование активации эффекторных каспаз
- резкое уменьшению времени жизни каспаз
АТИПИЗМОМ
Морфологический атипизм. Уменьшается площадь поверхности соприкосновения, уменьшается количество нексусов, меняется состав мембранных гликопротеидов. В клетке начинают синтезироваться, несвойственные зрелым клеткам эмбриональные белки
Биохимический атипизм. В опухолевых клетках преобладает гликолиз, что обуславливает их высокую выживаемость в условиях гипоксии. Опухоль активно поглощает питательные вещества. Наблюдается феномен субстратных ловушек, который заключается в повышении сродства фермента к субстрату (глюкозе), в опухолевых клетках в 1000 раз повышается активность гексокиназ. Преобладание гликолиза приводит к ацидозу
Слайд 17
Иммунологический атипизм - появление в опухолях белков, имеющих
АГ значение для организма - хозяина
Атипизм регуляции роста
и дифференцировки опухолевых клеток. Индукция роста и дифференцировки начинается с взаимодействия ФР с рецептором на клеточной мембране. Затем образуются вторичные посредники - цАМФ и цГМФ. Образование цГМФ сочетается с усилением пролиферации. Далее происходит активация Пк. В опухолевой ткани Пк тирозинзависимые. Характерна гиперреактивность Са-зависимой Пк, которая выполняет роль индуктора пролиферации - усиливает бесконтрольное размножение клеток
Слайд 18
ПРОМОЦИЯ
Мутации могут проявляться при воздействии опухолевого промотора
даже спустя большой промежуток времени. Промотор стимулирует деление клеток,
индуцируя экспрессию онкогенов – происходит манифестация опухолевого фенотипа клетокКлючевым элементом промоции считается активация Пк С
При длительном воздействии происходит закрепление опухолевого фенотипа
Слайд 19
ОПУХОЛЕВАЯ ПРОГРЕССИЯ
процесс малигнизации опухоли, в основе которого
лежит дальнейшая трансформация генетического материала клеток
Изначально опухоль представляет
собой клон клеток, потомков одной мутантной клетки Генетическая нестабильность - увеличение вероятности возникновения и закрепления в ряду клеточных поколений разнообразных изменений генома
происходит накопление в одной клетке сразу нескольких мутаций в онкогенах, опухолевых супрессорах и других генах
Слайд 20
Генетическая нестабильность популяций опухолевых клеток складывается из основных
типов нарушений:
уменьшения точности репликации ДНК и сегрегации хромосом
во время митоза нарушений в системах репарации повреждений ДНК или ошибок, возникших при ее репликации
ослабления функции сheckpoint
ослабления индукции апоптоза
опухолевая прогрессия приводит к увеличению массы опухоли и приобретению все большей автономности от организма; деструктивности роста; инвазивности; способности к метастазированию
Слайд 21
качественные изменения в ходе опухолевого роста представляют микроэволюционный
процесс, в котором генетическая нестабильность клетки обусловливает гено- и
фенотипическую гетерогенность клеточных популяций и создает основу для отбора по признаку набольшей злокачественностиБольшинство опухолей является кариотипически гетерогенными популяциями, проявляющими клональный характер роста
злокачественная опухоль своеобразная «мозаика», состоящая из различных клеточных клонов, отличающихся как по хромосомному набору, так и по генетическому потенциалу
Слайд 22
ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТ
Уничтожение трансформированных клеток с помощью клеточных и
иммунных реакций называется иммунным надзором за клетками в организме
На поверхности опухолевых клеток экспрессируются специфи-ческие АГ, которые распознаются ИС как “чужие”
На специфические для опухоли АГ, в ИО вырабатываюся специфические для данных АГ АТ
IgM и IgG
На фоне опухолевого процесса может формироваться цитокиновая дисрегуляция в виде изменения синтеза и секреции ИЛ
Рост опухолей сопровождается повышением уровней ИЛ-1β, ИЛ-6 и ИЛ-10, что сочетается со снижением активности цитотоксических Т-лф, экспрессии АГ МНС, снижением продукции цитокинов ИЛ-12, ИФ
Опухолевые клетки сами могут секретировать некоторые цитокины - ИЛ-1, 2, 6, 10, 13, 15, ФНО
Слайд 23
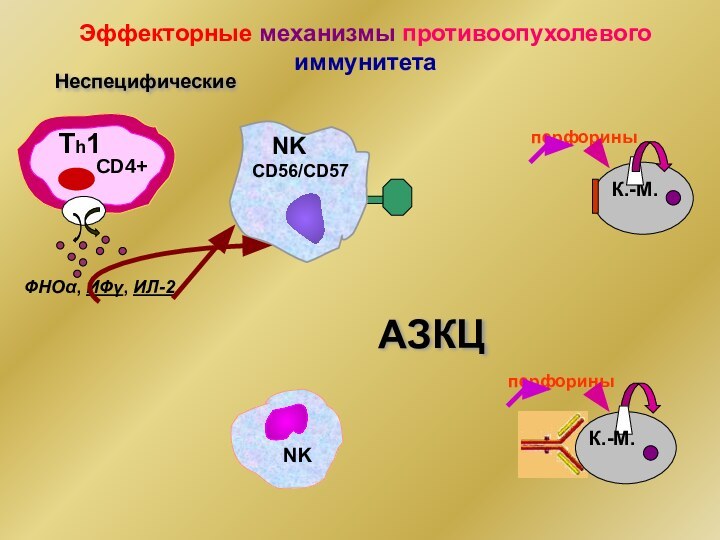
Эффекторные механизмы противоопухолевого иммунитета
Неспецифические
ФНОα, ИФγ, ИЛ-2
Тh1
CD4+
NK
CD56/CD57
К.-М.
перфорины
перфорины
АЗКЦ
NK
К.-М.
Слайд 25
Специфические
МНСI
АГ
К.-М.
АПК
Т (CD4)
Тk(CD8)
перфорины
цитотоксические
гуморальные
C5b6789 МАК
комплементарный
К.-М.
комплемент
Слайд 27
инфильтративный рост
аппозиционный рост
происходит за счет неопластической
трансформации нормальных клеток в опухолевые, что наблюдается в опухолевом
поле
Слайд 30
ПАРАНЕОПЛАСТИЧЕСКИЙ СИНДРОМ
дистанционное (системное) воздействие новообразования, не связанное
с прямой инвазией или компрессией опухоли и/или метастазами
Паранеопластический
синдром обусловлен глубокими биохимическими сдвигами, является следствием аутоиммунных реакций. Проявления паранеопластического процесса могут возникать на ранних стадиях развития опухоли, до появления клинической картины опухолевого поражения органа Анемия обусловлена коротким периодом жизни эритроцитов и нарушением метаболизма железа. Наблюдается гипохромия эритроцитов, анизоцитоз, пойкилоцитоз, снижение уровня гемоглобина и сывороточного железа