Слайд 2
Эпидемиология первичного рака печени (ПРП)
- Только 10-25%
больных ПРП являются операбельными.
- У 80% - после радикальной
резекции развиваются рецедивы.
В США в 1999 г. ПРП выявлен у 14 тыс. больных. Если в США показатель заболеваемости ПРП находится в пределах 5:100000 населения, то в Юго-Восточной Азии и Китае он гораздо выше - от 20 до 150 на 100 тыс. населения, причем соотношение заболевших мужчин и женщин повсеместно составляет 3-5:1.
Наследственность
Гепатит B Гликогенозы
цирроз алкогольный Дефицит альфа-1антитрипсин
Гемохроматоз
Микотоксин
Дополнительные факторы
Пероральные контрацептивы
Андрогены, анаболические стероиды
Неалкогольный, невирусный цирроз
Факторы риска развития ПРП
Слайд 4
Диагностика ПРП
УЗИ
Mетод позволяет дифференцировать солидные образования и жидкость
содержащие кисты, гемангиомы и злокачественные опухоли.
Ультразвуковое допплеровское исследование
сосудов печени и ворот органа.
Интраоперационное УЗИ необходимо при операциях на печени по поводу опухолей, поскольку позволяет выявить внутрипеченочные не пальпируемые метастазы и опухолевые тромбы, идентифицировать опухолевые узлы при циррозе печени, уточнить внутрипеченочную сосудистую архитектуру.
Слайд 5
Диагностика ПРП
Компьтерная томография
Является наиболее информативным методом в диагностике
первичного рака печени.
С помощью метода внутривенного "усиления" КТ позволяет
дифференцировать первичный рак печени от гемангиом, узлов регенераторной гиперплазии, метастазов опухолей внепеченочных локализаций.
Метод также информативен в топической диагностике опухолей печени.
Слайд 7
Магнитно-резонансная томография
Не менее чем КТ информативна в обнаружении
внутрипеченочных отсевов опухоли,
распространении опухоли на ворота печени,
дифференциальной диагностике
рака и хорошо васкуляризированных образований печени (узловая гиперплазия, аденома, гемангиома).
Слайд 8
Тонкоигольная пункционная цитобиопсия
ТПЦ - метод морфологической диагностики опухолей
печени осуществляется под контролем УЗИ, РКТ, лапароскопии, при пальпируемых
опухолях "в слепую".
Может выполняться неоднократно, в амбулаторных условиях
Используются иглы длиной 10-15 см с наружным диаметром иглы 0,5 - 1,2 мм.
Конец иглы может иметь сложную конфигурацию, способствующую взятию материала.
Слайд 9
Ангиография
Рентгенологическое исследование сосудов печени высокоинформативно в установлении природы,
характера опухоли печени, распространенности процесса внутри и вне печени.
Метод позволяет довольно точно предположить гистогенез опухоли печени.
Четкая визуализация печеночных артерий во время целиакографии,
воротной вены и ее ветвей при возвратной сплено-(мезентерико-) портографии,
нижней полой вены при нижней каваграфии - дает пока незаменимую информацию о сосудистой анатомии печени, ее воротах. То есть метод позволяет достоверно судить о резектабельности процесса в печени.
Слайд 10
Онкомаркеры
Альфа-фетопротеин (АФП).
Увеличение содержания онкомаркера выявляется у 80%
больных с раком печени.
обнаружение при этом образования в
печени практически свидетельствует о наличии у пациента печеночно-клеточного рака.
В пользу метастатического рака свидетельствует повышение содержания РЭА, СА 19-9.
Слайд 11
Классификация ПРП
Т1 – солитарный узел 2 см. или
менее, измеренный в наибольшем диаметре, без васкулярной инвазии
Т2- солитарный
узел 2 см. или менее, измеренный в наибольшем диаметре с васкулярной инвазией или множественные опухоли, располагающиеся в одной доле, меньше чем 2 см. без васкулярной инвазии или один солитарный узел более 2 см. без васкулярной инвазии
Т3 – солитарный узел более 2 см. в наибольшем измерении с васкулярной инвазией или множественные опухоли, располагающиеся в одной доле, меньше чем 2 см. с васкулярной инвазией или множественные опухоли в одной доле более 2 см. в диаметре с васкулярной инвазией и без нее
Т4 – множественные опухоли более чем в одной доле или опухоли с вовлечением портальной или печеночной вен, опухоли с прямой инвазией на соседние органы или опухоли с вовлечением висцеральной брюшины
N1 – метастазы в регионарные лимфоузлы (гепатодуоденальная связка)
M1 – отдаленные метастазы
Слайд 12
Лечения больных опухолями печени
I. Хирургическое лечение:
1. Резекции печени;
2.
Гепатэктомия с ортотопической алло- (ауто) трансплантацией.
II. Локальное аблативное и
циторедуктивное лечение:
1. Радиочастотная термодеструкция опухоли;
2. Криодеструкция опухоли;
3. Другие виды.
III. Внутрисосудистое чрескатетерное (рентгеноэндоваскулярное)лечение:
1. Эмболизация печеночной артерии;
2. Химиоэмболизация печеночной артерии;
3. Масляная химиэмболизация печеночной артерии;
4. Химиоинфузия печеночной артерии и др. виды.
IV. Системное лекарственное лечение
V. Комбинированное лечение
Слайд 13
Хирургическое лечение больных ПРП
Слайд 15
Показания к выполнению экономных
резекций печени
Цирроз печени
Небольшие размеры
остающейся части печени
Предшествующая длительная многокурсовая химиотерапия
Билобарное поражение печени
Предшествующая обширная
резекция печени
Небольшие размеры опухолевого очага
Слайд 16
Функциональное состояние печени
Если опухоль печени представляется удалимой,
то важнейшим является оценка функциональнго состояния непораженной опухолью паренхимы
печени.
Класс А – 5-6 (любой вид лечения)
Класс В – 7-9 (только экономные резекции, комбинации нехирургич. методов лечения)
Класс С – ≥ 10 (лечение не показано)
Слайд 17
Расширенная гемигепатэктомия справа. Удаление I сегмента. Холангиоеюностомия (по
Roux).
РОНЦ им. Н.Н Блохина РАМН, Ю.И.Патютко
Слайд 18
VIII
IV
Билатеральная резекция печени
РОНЦ им. Н.Н. Блохина РАМН,
Ю.И.Патютко
Слайд 19
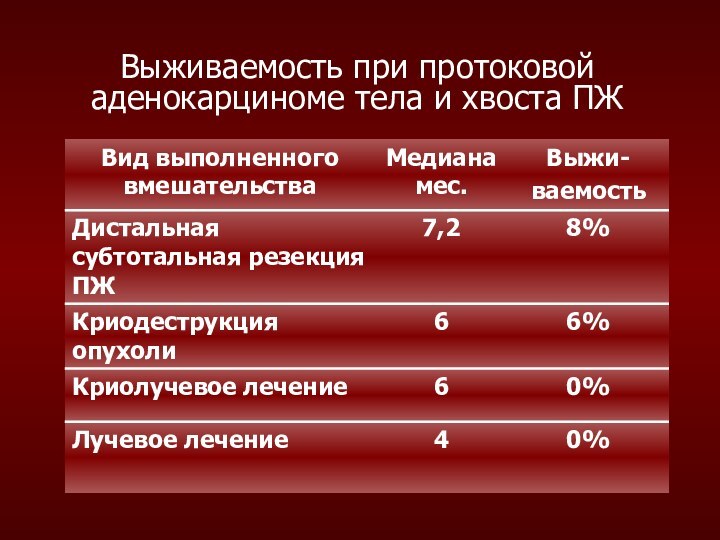
Пятилетняя выживаемость больных ПРП с учетом факторов прогноза
(Япония).
Слайд 20
Алгоритм лечения больных с метастами
колоректального рака в
печень
Больные, подлежащие хирургическому лечению
1. Предоперационная химиотерапия. При небольших
размерах левой доли – эмболизация правой воротной вены.
2. Гемигепатэктомия со стороны большего поражения + крио- или радиочастотное термовоздействие на очаги в остающейся доле.
3. Послеоперационная (через 3-4 нед.) химиотерапия.
4. Динамическое наблюдение (УЗИ 1 раз в 3 мес.)
при выявлении нового очага –
- Радиочастотная термоаблация
- Локальная химиотерапия
- Криоаблация и др.
- Повторная
операция
Слайд 21
В опухоль вводится специальная радиочастотная игла
(зонд) с
раскрывающимся массивом элементов-антенн.
С помощью иглы создается сферическая область
некроза
(абляции).
Опухоль разрушается нагреванием до температуры,
превышающей 52°С. Выделение тепла происходит из-за
смены направления движения ионов под воздействием
высокочастотного (460 кГц) тока.
Радиочастотная термоабляция
Слайд 22
Радиочастотная термоабляция
Контроль позиционирования иглы осуществляется с помощью УЗИ,
КТ или МРТ.
Тепло выделяется в тканях, игла при этом
не нагревается. Зонды имеют систему контроля температуры.
Доступы:
Слайд 23
Через 3 месяца
Через 6 месяцев
До лечения
Радиочастотная термоабляция
Слайд 24
Показания к радиочастотной термоабляции
Неоперабельная гепатоцеллюлярная карцинома
размером до 4,5 см (6,5 при использовании 7 см
иглы), до 5 очагов.
Метастазы в печень размером до 3,5 см (5,5 при использовании 7 см иглы), до 5 очагов.
Слайд 25
Методика портальной венозной эмболизации (ПВЭ) направлена на стимуляцию
компенсаторной гипертрофии остающейся после резекции доли печени и повышение,
таким образом дооперационного функционального резерва органа.
Эмболизацию воротной вены осуществляют с помощью разработанного в Институте хирургии им.А.В.Вишневского биологического окклюзирующего материала РАБРОМ.
РАБРОМ создан на основе фибронектина, получаемого из криопреципитата - препарата плазмы донорской крови, обладает вязкостью близкой к вязкости нативной плазмы, заданным временем отвердения (от 3 до 10 мин), рентгеноконтрастностью и активными антибактериальными свойствами.
Венозная эмболизация
Слайд 26
Интраартериальная химиоэмболизация
Ограничивает кровоснабжение опухолевых масс.
Дополнение эмболизации
воздействием цитостатика в виде суспензии в жировом рентгенконтрастном веществе,
например, в иодолиполе создает условия для длительного цитостатического действия на опухоль.
Доксорубицин (40-80 мг на одну процедуру), иногда в комбинации с митомицином С (10-20 мг) или цисплатином (100-150 мг)
Комбинация метотрексата, 5-ФУ, цисплатина и интерферона альфа-2b.
5-ФУ с лейковорином
Слайд 27
Противопоказания к химиоэмболизации
Слайд 28
Стандарты ХТ ПРП отсутствуют.
Эфективность в монотерапии проявляют:
эпирубицин (17%
ответа), цисплатин (17%), доксорубицин (11-32%, особенно при внутриартериальном введении),
но не в липосомной форме (доксил), оказавшейся менее эффективной, митоксантрон (27%) и гемцитабин (36%).
Комбинации:
Доксорубицин и 5-ФУ (26%)
Эпирубицин и этопозид (39% ответа),
с непостоянством результатов - биомодификации 5-ФУ лейковорином (10-28%) и оксалиплатин с 5-ФУ (34%).
Химиотерапия ПРП
Слайд 29
Прогноз рака ПРП
По данным РОНЦ им. Н.Н.Блохина РАМН
(Ю.И.Патютко): 1 летняя выживаемость больных, подвергшихся резекции печени -100%.
5-летняя выживаемость больных после экономной резекции печени составила 35,7%, больных после гемигепатэктомии - 41,2%, комбинированные резекции печени -17,6%.
Неблагоприятный прогноз:
отсутствие капсулы опухоли, нечеткий ее контур
диффузный рост
низкая степень дифференцировки опухоли
наличие внепеченочных поражений
спонтанный некроз опухоли
морфологические признаки гепатита в паренхиме печени
цирроз печени
инвазия сосудов в опухоли и вне опухоли
повышенная экспрессия трансмембранного гликопротеина
(тирозинкиназы).
Слайд 30
Рак органов билиопанкреатодуоденальной зоны (БПДЗ)
Рак внепеченочных желчных протоков
составляет 2–4,5% всех злокачественных опухолей человека, в структуре новообразований
БПДЗ он занимает 2-е место после опухолей ПЖ и составляет 15% случаев.
Рак внепеченочных желчных протоков чаще всего развивается в области развилок желчных протоков и поражает чаще всего конфлюенс до 41% случаев, общий печеночный проток в месте слияния с пузырным протоком – до 28%, холедох – до 25% случаев.
Рак большого дуоденального сосочка (БДС) составляет 0,1–0,3% всех вскрытий, 0,5–1,6% всех злокачественных новообразований и более 2% опухолей желудочно кишечного тракта.
Слайд 31
Внепеченочные желчные протоки
долевые печеночные протоки
зона слияния долевых печеночных
протоков (конфлюенс)
общий печеночный проток
общий желчный проток (холедох) и Фатеров
сосочек
Слайд 32
Относительная частота рака различных органов билиопанкреатодуоденальной зоны
Слайд 33
Рак желчного пузыря
В России регистрируется у 2800 пациентов/год.
Предрасполагающие
факторы – желчекаменная болезнь, аномалии строения желчных протоков, ожирение,
кальцификация стенок желчного пузыря.
Экзогенные канцерогены – изоцианиды, нитрозамины, противозачаточные средства, профессиональные вредности у рабочих, занятых в резиновой промышленности.
5-ти летняя выживаемость не превышает 5%.
Слайд 34
Лечение больных раком желчного пузыря
Слайд 35
Алгоритм ведения больных при полиповидных образованиях желчного пузыря
Множественные
гиперэхогенные
полиповидные
образования
до 1 см
1-2 полиповидных
образования до 1 см
на тонкой
ножке с
широким основанием
средней эхогенности
1 полиповидное
образование > 1 см
на тонкой ножке с
широким основанием
средней эхогенности
Наблюдение
(УЗИ)
Контрольные УЗИ
с периодичностью
1 раз в 3 мес.
(или ХЭ)
Расширенная
комбинированная
холецистэктомия
Слайд 36
Холангиоцеллюлярный рак и рак внепечечных желчных протоков
Частота
встречаемости 7-8% от всех злокачественных новообразований периампулярной зоны.
Предрасполагающие заболевания:
первичный склерозирующий холангит, врожденная дилятация интра- и экстрапеченочных желчных протоков, чаще в холедохе (болезнь Caroli), хроническая гельминтная инвазия (opisthorchis viverrini, clonorchis sinensis, opisthorchis felineus). Человек поражается при употреблении сырой и недостаточно обработанных рыбы (в эндемичных районах заболеваемость 80/100 тыс.).
Канцерогены: асбест, диоксин, нитрозамины, радионуклиды (торотраст, радон)
Наследственность.
Слайд 37
Рак проксимальных печеночных протоков (опухоли Клатскина)
Рак ПЖП составляет
10–26,5% от всех злокачественных поражений желчных протоков, до 58
% рака внепеченочных желчных путей.
На аутопсии рак общего печеночного протока выявляют в 0,01% случаев.
Средний возраст от 55 до 65 лет.
Чаще опухоль Клатскина встречается у мужчин – 57–61%.
Без лечения большинство больных раком ПЖП умирают в течение 4 - 6 мес после установления диагноза.
Слайд 38
Рак ПЖП это, как правило, небольшого размера опухоль
в области развилки печеночных протоков, характерная форма роста –
инфильтративная, опухоль распространяется по ходу желчного протока и через его стенку.
Микроскопическая картина – аденокарцинома ацинарного, тубулярного, трабекулярного, альвеолярного или папиллярного типа. Папиллярный тип встречается реже и при нем отмечается более высокая резектабельность и более хорошие отдаленные результаты
Рак проксимальных печеночных протоков (опухоли Клатскина)
Слайд 39
Чрескожная чреспеченочная холангиография
Опухоль общего
печеночного протока
Рак БДС
Слайд 40
Лечение рака проксимального отдела печеночных протоков
Слайд 41
Лечение больных раком холедоха,
БДС, 12ПК
Стандартная ГПДР
Стандартная ГПДР
+ радиотерапия
Слайд 42
Результаты лечения больных резектабельным раком ВЖП, БДС, 12ПК
РОНЦ
им. Н.Н. Блохина РАМН, Ю.И.Патютко
Слайд 43
Эпидемиология рака поджелудочной железы
РПЖ регистрируется
ежегодно у 232 тыс. больных, умирают 227 тыс.
Женщины – 14900 новых случаев, мужчины – 14100 новых случаев. Возраст – старше 50 лет.
Соотношение умерших к регистрируемым - 0,97;
5-летняя выживаемость составляет 3,8% у мужчин и 4,6% у женщин, резектабельны - 5-20%.
Среди американцев афроамериканского происхождения заболеваемость выше, чем в других канцер–регистрах.
Низкая заболеваемость РПЖ на африканском континенте.
Практически не встречается до 30 лет.
Слайд 44
Факторы риска РПЖ
Диета (жирная, калорийная пища)
Доброкачественные заболевания
Имеются
противоположные точки зрения на взаимосвязь РПЖ и сахарного диабета
Наследственность – 10% (семейный РПЖ, синдром Пейтца-Ейгертца, атаксия-телеангиоэктазия, BRCA2, наследственный панкреатит).
Различия в экспрессии генов K–ras и p53 могут быть основанием в различной заболеваемости и выживаемости у афроамериканцев.
Слайд 45
Факторы риска РПЖ
Ожирение, высокий рост.
Пестициды, формальдегиды, хлорированные
углеводороды, бензидин, продукты бензина.
По данным японских авторов, относительный
риск смертности от РПЖ среди мужчин, выкуривающих 40 и более сигарет в день, составляет 3,3 (95% CI:1,38–8,1). Вредное влияние курения сохраняется до 2 лет после отказа от курения, а через 15 лет риск уравнивается с некурящими.
Влияние алкоголя (прямое) и кофе не доказано.
Слайд 46
Молекулярно-генетические нарушения при РПЖ
Активация клеточного онкогена K-ras
(клеточная пролиферация). Частота мутаций – 70-100%
Инактивация гена-супрессора р53. Встречается
у 70% больных. Среди мутаций наиболее часто встречают точковые в 4-10 экзонах и частичные делеции гена.
Инактивация генов-супрессоов р16 и DPC4 (в 80% и 50% случаев РПЖ соответственно).
Слайд 47
Клиника РПЖ
Сахарный диабет
Похудание
Желтуха
Кожный зуд
Болевой синдром
Дуоденальная непроходимость
Асцит
Слайд 48
Диагностика РПЖ
УЗИ брюшной полости (может использоваться как скрининг).
Повышение
уровня CA-19-9 (sialyl-Lewis-a antigen), может использоваться как скрининг.
Спиральная компьютерная
томография.
МРТ (с контрастированием протоков).
Лапароскопия (с интракорпоральным УЗИ).
ЭРХПГ (с аспирационной биопсией сока ПЖ).
Ангиография.
Пункционная биопсия.
Слайд 49
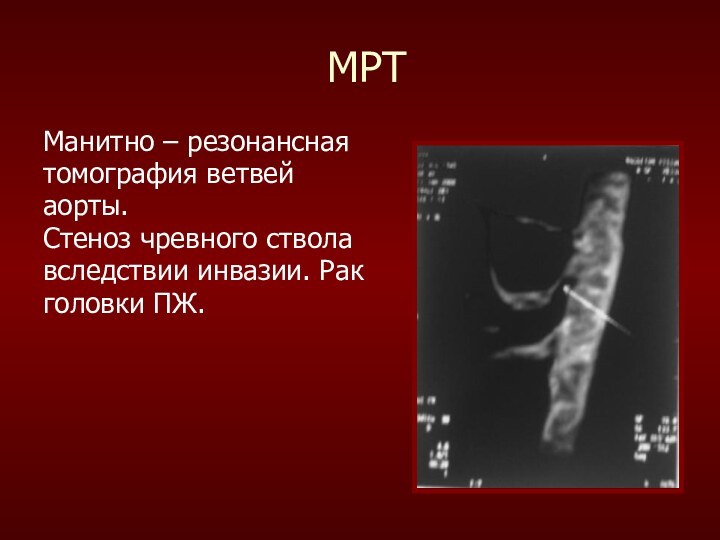
МРТ
Манитно – резонансная
томография ветвей
аорты.
Стеноз чревного
ствола
вследствии инвазии. Рак
головки ПЖ.
Слайд 50
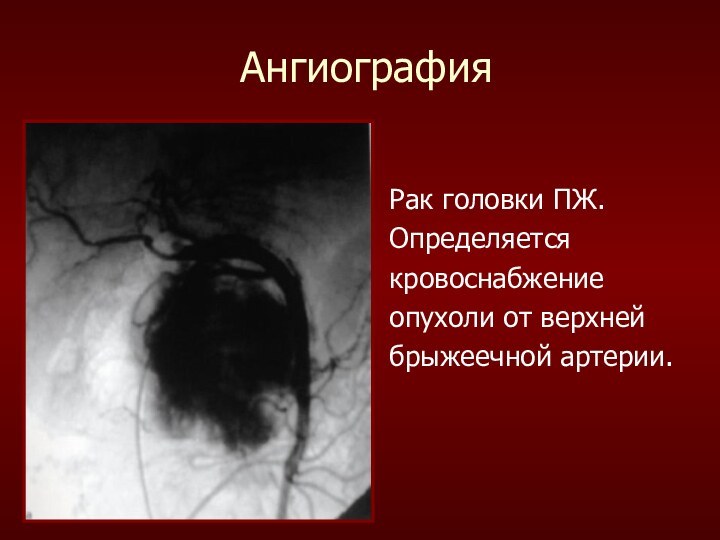
Ангиография
Рак головки ПЖ.
Определяется
кровоснабжение
опухоли от верхней
брыжеечной артерии.
Слайд 51
Виды желчеотводящих операций
Чрескожное чреспеченочное дренирование желчных протоков
-наружное чрескожное
чреспеченочное
(требует реинфузии желчи в жкт)
-наружно-внутреннее чрескожное чреспеченочное Осложнения: внутрибрюшное
кровотечение, гемобилия, желчеистечение и др.
Эндопротезирование желчных протоков
Эндохирургическое и хирургическое желчеотведение
Слайд 52
Чрескожное чреспеченочное дренирование
Слайд 53
Раздельное чрескожное чреспеченочное наружное дренирование желчных протоков правой
и левой долей печени
Чрескожное чреспеченочное наружное-внутреннее дренирование желчных протоков
левой доли печени при раке желчных протоков в области ворот печени - проведение катетера через зону опухолевой стриктуры в 12 пк. (W. Molnar, A.E.Stockum, 1974 г.)
Слайд 54
Двойное чрескожное чреспеченочное наружное-внутреннее дренирование желчных протоков правой
и левой долей печени при раке желчных протоков в
области ворот печени
Слайд 55
Эндопротезирование холедоха металлическим саморасправляющимся стентом
а)
Слайд 56
Эндопротезирование холедоха
металлическим саморасправляющимся
стентом
б)
Слайд 57
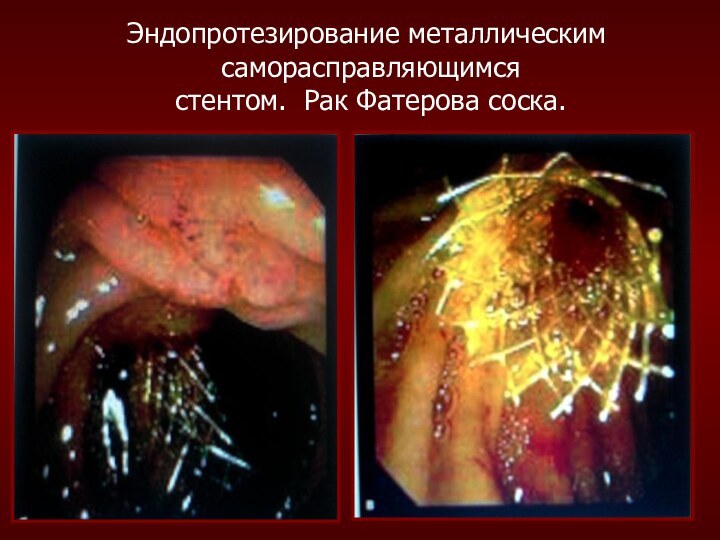
Эндопротезирование металлическим
саморасправляющимся
стентом. Рак Фатерова соска.
Слайд 58
Холангиогастральное дренирование
Слайд 59
Билиодигестивные анастомозы
Билиодигестивные анастомозы относятся к числу вмешательств, направленных
на декомпрессию желчевыводящей системы. Они могут выполняться как этап
перед радикальной операцией, либо являться самостоятельным оперативным пособием.
Слайд 60
Показания к наложению билиодигестивных анастомозов
Абсолютные показания обычно возникают
при
непроходимости желчных путей, когда другие способы восстановления оттока желчи
в кишечник невозможны.
Варианты операций:
для отведения желчи могут быть использованы желчный пузырь,
пузырный проток,
общий печеночный проток или внутрипеченочные желчные протоки, которые соединяются соустьем с двенадцатиперстной или тонкой кишкой.
Слайд 61
Выбор метода операции
определяется:
– распространенностью опухоли;
– уровнем сдавления желчных
путей;
– состоянием желчных путей (функционирующи или блокированный желчный пузырь,
расширенны или нормального калибра желчные протоки, наличие измененных стенок желчного пузыря и желчных протоков, явления холангита, выполнение ранее операций на желчных путях);
– состоянием желудка, двенадцатиперстной или тонкой кишок, с которыми предполагается наложение анастомоза (наличие сращений, фиксация органов, прорастание опухолью, застойные явления в желудке, дуоденальный стаз, кишечная непроходимость и др.);
– состоянием больного, допускающим или ограничивающим проведение оперативных вмешательств.
Слайд 62
Холедохоэнтеро-
анастомоз с межкишечным соустьем и выключением приводящей петли
по А.А.Шалимову
Холецистоэнтеро-
анастомоз с межкишечным соустьем и выключением приводящей петли
по А.А.Шалимову
Слайд 63
Холедохоэнтеро-
анастомоз на отключенной петле тонкой кишки по Ру
Для
профилактики послеоперационных опухолевых стриктур сформированных анастомозов и необходимости санации
желчевыводящей системы у ряда больных
выполняют транспеченочное дренирование желчных протоков.
При этом может осуществляться как наружное дренирование (по Прадери–Смиту) Рис.1
так и проведение сменных транспеченочных дренажей
(СТД по Гетсу-Сейполу-Куриану).
Рис.2
Слайд 64
Гепатикоеюностомия
на транспеченочном
дренаже по Прадери-
Смиту
Гепатикоеюностомия
на транспеченочном по
Гетсу-Сейполу-Куриану
2
1
Слайд 65
Классификация рака ПЖ
Тх – первичная опухоль недоступна оценке
Т0
– нет признаков первичной опухоли
Т1 – опухоль в пределах
поджелудочной железы, размеры которой не превышают 2 см. в наибольшем измерении
Т2 – опухоль в пределах поджелудочной железы, размеры которой превышают 2 см. в наибольшем измерении
Т3 – распространение опухоли опухоли на 12-п.кишку, желчный проток, парапанкреатические ткани (забрюшинную клетчатку, брыжейку тонкой и поперечноободочной кишок, малый и большой сальник и кишку, крупные сосуды (воротную вену, чревный ствол, верхнюю брыжеечную артерию, общую печеночную артерию, кроме селезеночных сосудов)
Слайд 66
Nx – регионарное метастазирование недоступно оценке
N0 – отсутствие
метастазирования в регионарные лимфоузлы
N1 – наличие метастазирования в регионарные
лимфоузлы
N1a – единичный метастаз в один регионарный лимфоузел
N1b – множественные метастазы в нескольких регионарных л/узлах
Мх – отдаленное метастазирование недоступно оценке
М0 – отсутствие отдаленного метастазирования
М1 – наличие отдаленного метастазирования
Слайд 67
Гистологическая классификация экзокринных злокачественных опухолей ПЖ
1. протоковая аденокарцинома
-
муцинозная некистозная карцинома
- перстневидноклеточная карцинома
- железистоплоскоклеточная карцинома
- недифференцированная (анапластическая)
карцинома
- смешанная протоково-эндокринная карцинома
2. гигантоклеточная опухоль
3. серозная цистаденокарцинома
4. муцинозная цистаденокарцинома
5. внутрипротоковая папиллярно-муцинозная карцинома
6. ацинарноклеточная карцинома
- ацинарноклеточная цистаденокарцинома
- смешанная ацинарно-эндокринная карцинома
7. панкреатобластома
8. солидная псевдопапиллярная карцинома
9. смешанные карциномы
Слайд 68
Протоковый рак: распространенность и метастазирование
Инвазия передней капсулы
ПЖ – 80%
Инвазия края резекции ПЖ – 40%
Ретроперитонеальная внеорганная
инвазия – 80%
Инвазия крупных сосудов – 60%
Метастазы в регионарные лимфоузлы – 100%
Метастазы в юкстарегионарные лимфоузлы – 80%
Метастазы в печень – 20%
Слайд 69
Лечение рака ПЖ
Хирургическое
Стандартная ГПДР
Расширенная ГПДР
Дистальная субтотальная резекция ПЖ
Панкреатэктомия
Криодеструкция
Химиотерапия
Слайд 70
Радикальная стандартная ГПДР
резекция холедоха
резекция выходного отдела желудка с прилежащим малым и правой
половиной большого сальника
удаление головки поджелудочной железы
удаление всей двенадцатиперстной кишки
в удаляемый комплекс входит прилежащая к головке поджелудочной железы клетчатка и фасциально-клетчаточные футляры общей и собственной печеночной артерии, верхей брыжеечной и воротной вены.
Слайд 72
Особенности ГПДР
Предопределяют отсутствие в послеоперационном периоде
осложнений со стороны культи pancreas и панкреатикоеюноанастомоза.
отказ от ушивания
культи ПЖ наглухо или введения в панкреатический проток пломбирующих материалов
максимально щадящие манипуляции на культе ПЖ
отдельное вшивание панкреатического протока в стенку тощей кишки минимальным количеством швов без наружной панкреатикоеюностомии
Слайд 73
Вид после радикальной ГПДР
РОНЦ им. Н.Н. Блохина РАМН,
Ю.И.Патютко
Слайд 74
Тотальная панкреатэктомия
по поводу карциноида поджелудочной железы
Восстановление
непрерывности
пищеварительного
тракта
Слайд 75
Виды резекции ПЖ
Резекция дистальных отделов железы с пересечением
ее справа от верхней брыжеечной или воротной вены с
пересечением селезеночной артерии у ее устья, пересечением нижней брыжеечной вены и селезеночной вены непосредственно у конфлюэнса воротной вены. Удаляются лимфоузлы чревного ствола, в воротах селезенки, вдоль селезеночной артерии и по нижнему краю тела и хвоста железы.
Радикальная дистальная резекция дополняется удалением лимфоузлов общей печеночной артерии, вдоль верхней брыжеечной артерии и вены, от верхнего края чревного ствола до нижнего края левой почечной вены, от нижнего края левой почечной вены до верхнегои края устья нижней брыжеечной артерии.
Слайд 76
Виды комбинированного лечения протокового РПЖ
+
+
+
Стандартная ГПДР + дистанционная
радиотерапия
Маслянная химиоэмболизация ГДА + Стандартная ГПДР + дистанционная радиотерапия
Дистальная
субтотальная резекция ПЖ + дистанционная радиотерапия
Криодеструкция опухоли + дистанционная радиотерапия
Слайд 77
Маслянная химиоэмболизация
1 мес.
1 год.
5 лет
Слайд 78
Гемцитабин является основой лекарственного лечения местнораспространенного и
метастического рака поджелудочной железы. Считается, что комбинация гемцитабина и
доцетаксела обладает умеренной токсичностью и высокой эффективностью.
Предоперационная химиотерапия при местнораспространенном раке поджелудочной железы доцетакселом и гемцитабином позволяет «уменьшить» стадию и повысить резектабельность и выживаемость у 81%.
Химиотерапия РПЖ
Слайд 79
При нерезектабельном РПЖ используется интраперитонеальное введение
5-Фторурацила и лейковорина (назначение 750, 1000, 1250, 1500 mg/m2).
Достигнута выживаемость от 7 до 12.8 месяцев.
Облучение в сочетании с химиотерапией (Gem+FU+LV) повышает медиану выживаемости оперированных больных с 11 мес. до 21 мес. (Pister et al., 2003). Медиана выживаемости при распространенном РПЖ без химиотерапии – 4 мес., при использовании комбинаций на основе гемцитабина - 7-8 мес., единичные пациенты выживают 1 год.
Химиотерапия РПЖ
Слайд 80
Прогноз у больных протоковым раком головки ПЖ
При лечении
выполненном в объеме стандартной ГПДР 36% больных переживают год
и 19% - 2 года.
Расширенная ГПДР позволяет продлить жизнь больным до 3 лет в 25% случаев, а год переживут – 50%, при этом медиана составляет 10 мес.
При комбинированном лечении 1- и 3 годичная выживаемость составляет 59% и 21%, однако еще 11% больных переживут 4 года.
Лучевая терапия – лишь 4% переживут 1 год.
Слайд 81
Прогноз после ГПДР
РОНЦ им. Н.Н. Блохина РАМН,
Ю.И.Патютко