Слайд 2
В дальнейшем:
6. Фармакогенетика
7. Предиктивная медицина и
генетический паспорт
8. Геномный импринтинг, роль импринтинга в
нормальном и патологическом развитии
9. Стволовые клетки и проблемы клонирования
10. Старение организма и проблемы долголетия
11. Генная терапия
Слайд 3
XXI век- век генетики
Геном
Внешняя
среда
Генетика
- наука о наследственности и изменчивости
Медицинская генетика (МГ) - наука о роли наследственности в патологии человека, закономерностях передачи наследственных болезней, их диагностике, лечении, профилактике.
Клиническая генетика - прикладная МГ, направленная на применение достижений генетики и МГ для решения клинических проблем пациентов и их семей.
АКСИОМЫ МЕДИЦИНСКОЙ ГЕНЕТИКИ
1.Наследственные болезни - часть общей
наследственной изменчивости человека
2.Патогенез и клиника любой НБ зависят от генотипа и среды
3.В процессе эволюции генофонд человечества накопил
множество разнообразных мутаций
4.Постоянно меняющаяся среда привела к появлению новых
видов наследственной патологии –экогенетическим болезням
5. Прогресс медицины способствует накоплению вредных мутаций в обществе, но одновременно увеличивает возможности диагностики, лечения и профилактики НБ.
6. Расшифровка генома человека знаменует переход всей медицины на качественно новый уровень, отличительные особенности которого- профилактическая направленность и индивидуальный (персонифицированный) подход к пациенту
Слайд 6
Этиология наследственных болезней (НБ)
НБ
- часть наследственной изменчивости (НИ)
Мутации - причины всех НБ
Генетический груз (ГГ) -НИ в популяции, приводящая к появлению менее приспособленных особей, подлежащих естественному отбору
- Мутационный груз - 1 мутация на 106 гамет
- Сегрегационный груз - из поколения в поколение
- Субституционный груз - эффект при изменении условий среды
Генетический мониторинг (С.Н.Давиденков)- контроль за уровнем ГГ, частотой сторожевых фенотипов
- Раннее выявление новых мутаций
- Генетическое консультирование семей с НБ
- Создание условий непроявления генных мутаций
Слайд 7
Величина генетического груза
Летальность -
70% всех зигот человека
Новорожденные с НБ и врожденными пороками 5-5,5%
Пороки развития - 2,5% новорожденных
Наследственные болезни - 1,5%
Хромосомные - 0,5% Генные - 1,0%
Болезни с выраженной наследственной
предрасположенностью (дети до 5 лет) - 3-3,5%
Всего известно НБ - более 4 000
Доля 15 наиболее частых НБ до 5 лет - > 50%
Число бесплодных супружеских пар - 10-15%
Ежегодно в России рождается 100 000 детей-инвалидов
В Петербурге число детей- инвалидов в 2002г. 13 695
Слайд 8
Классификация наследственных болезней
I.
Генетическая
Генные НБ (моногенные, полигенные)
Мультифакториальные НБ (болезни с
наследственной предрасположенностью)
Хромосомные НБ
Генетические болезни соматических клеток
Митохондриальные болезни
Эпигенетические болезни (болезни импринтинга)
Болезни экспансии (динамические мутации)
Слайд 9
Классификация наследственных болезней
II По типу наследования :
III По клиническому проявлению:
Аутосомно-доминантные
Классификация по органно-
Аутосомно-рецессивные системному принципу:
Сцепленные с полом нервные, мышечные, глазные,
Х-сцепленные доминантные болезни опорно-двигательного
Х-сцепленные рецессивные аппарата, др.
У- сцепленные
Нетрадиционного типа наследования
IV По патогенезу :
Нарушения обмена веществ (1)
Аномалии морфогенеза (2)
Комбинированные (1) и (2)
Слайд 10
Семиотика - раздел медицинской генетики, изучающий симптомы наследственных
болезней, вызванных взаимодействием наследственных и средовых факторов.
1. Особенности
клинических проявлений
2. Принципы клинической диагностики
3. Синдромы НБ
4. Клинико-генеалогический метод
Клинические проявления НБ
семейный характер
хроническое, рецидивирующее течение
резистентность к лекарственной терапии
специфические «маркерные» симптомы
системные поражения органов и тканей
Слайд 11
Особенности клинического проявления
Клинический полиморфизм
(КП)
первичный КП - многообразие проявления признаков НБ связанных с первичным дефектом,
вторичный КП - осложнения вследствие первичного дефекта
пенетрантность - частота признака среди больных
экспрессивность - выраженность клинического признака
Генетический полиморфизм - молекулярная основа КП
разные мутации одного гена - разная клиника, разные заболевания
мутации разных генов - одно заболевание
Слайд 12
Принципы клинической диагностики
Цели клинического осмотра:
Поставить точный диагноз
Установить природу заболевания
Направить на дополнительные лабораторные исследования
В процессе
осмотра обращать внимание на:
Врожденные пороки развития
Антропометрические данные
Врожденные анатомические вариации
Слайд 13
Синдромологический подход
в диагностике НБ
Справочники:
«Наследственные синдромы и
медико-генетическое консультирование» Козлова С.И. соавт М. «Практика» 1996
Справочник В.МакКьюсика -On line Mendelian Inheritance in Man http://www.ncbi.nlm.nih.gov//omim
(National Сenter of Biotechnological Information)
Слайд 14
Генеалогический анализ –метод родословных
Установление наследственного характера признака
Выяснение
типа передачи НБ
Анализ пенетрантности и экспрессивности признака
Сцепление признака с
генетическими и молекулярными маркерами
Медико-генетическое консультирование
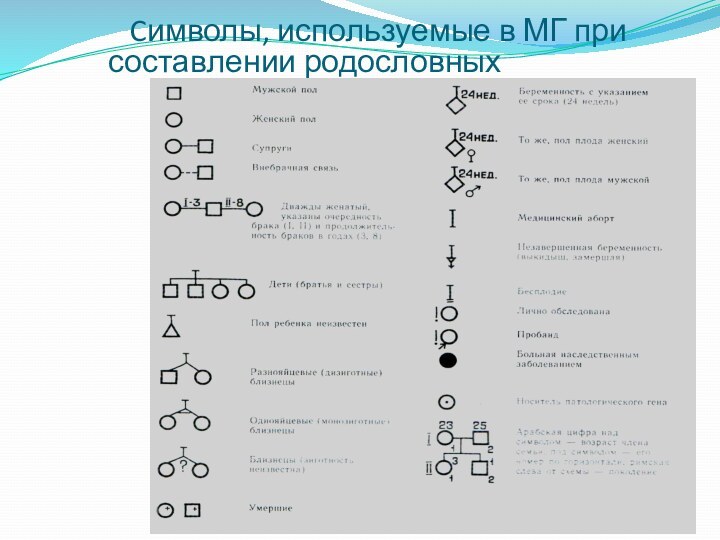
Пробанд - больной или его родственник,
с которого начинается составление родословной.
Слайд 15
Cимволы, используемые в МГ при составлении
родословных
Слайд 16
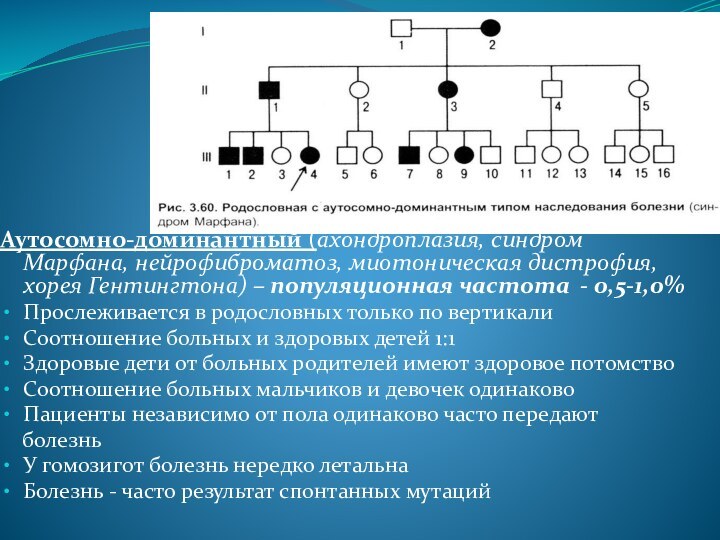
Аутосомно-доминантный (ахондроплазия, синдром Марфана, нейрофиброматоз, миотоническая дистрофия, хорея
Гентингтона) – популяционная частота - 0,5-1,0%
Прослеживается в родословных только
по вертикали
Соотношение больных и здоровых детей 1:1
Здоровые дети от больных родителей имеют здоровое потомство
Соотношение больных мальчиков и девочек одинаково
Пациенты независимо от пола одинаково часто передают
болезнь
У гомозигот болезнь нередко летальна
Болезнь - часто результат спонтанных мутаций
Слайд 17
Другие типы наследования
Аутосомно-рецессивный (муковисцидоз, ФКУ, СМА,
АГС,
мукополисахаридозы) - популяционная частота - 0,25%
Родители клинически
здоровы
Соотношение больных и здоровых детей 1:3
Если больны оба супруга – дети всегда больные
Оба пола поражаются одинаково часто
Не исключено кровное родство супругов
В браке больного и носителя рождается 50% больных,
больного и здорового –рождаются только здоровые
Слайд 18
Х-сцепленные заболевания
- популяционная частота 0,25%
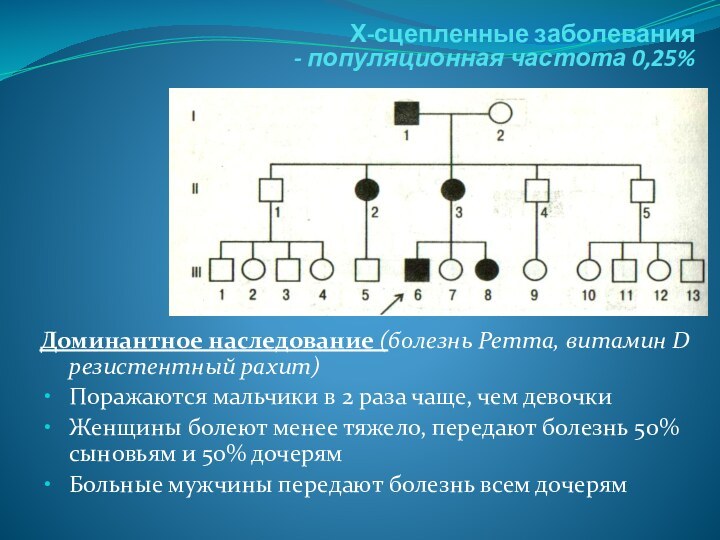
Доминантное наследование (болезнь Ретта,
витамин D резистентный рахит)
Поражаются мальчики в 2 раза
чаще, чем девочки
Женщины болеют менее тяжело, передают болезнь 50% сыновьям и 50% дочерям
Больные мужчины передают болезнь всем дочерям
Слайд 19
Х-сцепленные заболевания
- популяционная частота 0,25%
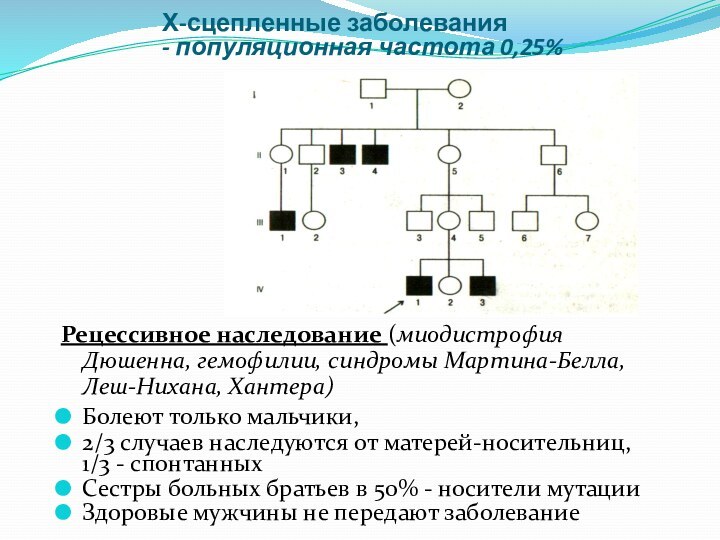
Рецессивное наследование (миодистрофия Дюшенна,
гемофилии, синдромы Мартина-Белла, Леш-Нихана, Хантера)
Болеют только мальчики,
2/3 случаев
наследуются от матерей-носительниц, 1/3 - спонтанных
Сестры больных братьев в 50% - носители мутации
Здоровые мужчины не передают заболевание
Слайд 20
Другие типы наследования
Y-сцепленные (нарушения сперматогенеза, рост тела, конечностей,
зубов)
Митохондриальные болезни (атрофия зрительного нерва Лебера, кардиомиопатии, миоклоническая эпилипсия,
митохондриальная миопатия, прогрессирующая офтальмоплегия)
Болезнь передается только по материнской линии
Болеют мальчики и девочки
Больные мужчины не передают болезнь потомству
Слайд 21
Эпигенетические болезни (болезни импринтинга)
Импринтинг - дифференциальная экспрессия генов
или проявление мутации в зависимости от их родительского происхождения
Число импринтированных генов - 200-500
В настоящее время известно 10 наследственных синдромов, связанных с импринтингом (Прадера-Вилли или Ангельмана; Видемана-Беквита; Рассела-Сильвера; синдромы однородительских дисомий)
Импринтингу отводят важную роль в онкогенезе.
Слайд 22
ГЕНОМ ЧЕЛОВЕКА и НАСЛЕДСТВЕННЫЕ БОЛЕЗНИ
ЭТИОЛОГИЯ
ДИАГНОСТИКА
Слайд 23
Общие представления о работе генома
Определение понятий
Основные итоги Международного проекта
« Геном человека»
«Генетизация» человечества ХХI века
Генетический полиморфизм
Филогенез и этногенез человека
Функциональная геномика
Классификация наследственных болезней
Методы диагностики
Геномика и молекулярная медицина
Слайд 24
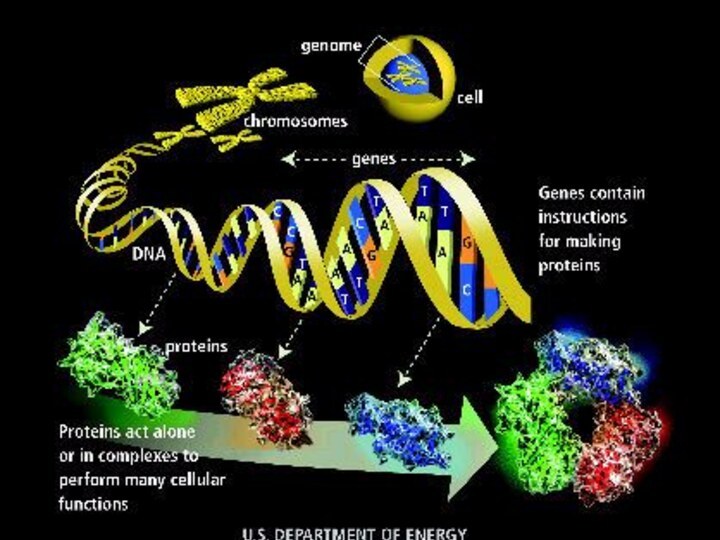
ГЕНЫ и ХРОМОСОМЫ
Все гены человека
упакованы в 23 пары хромосом
2n =46 ; 1n =
23
Эухроматин
Гетерохроматин
Слайд 25
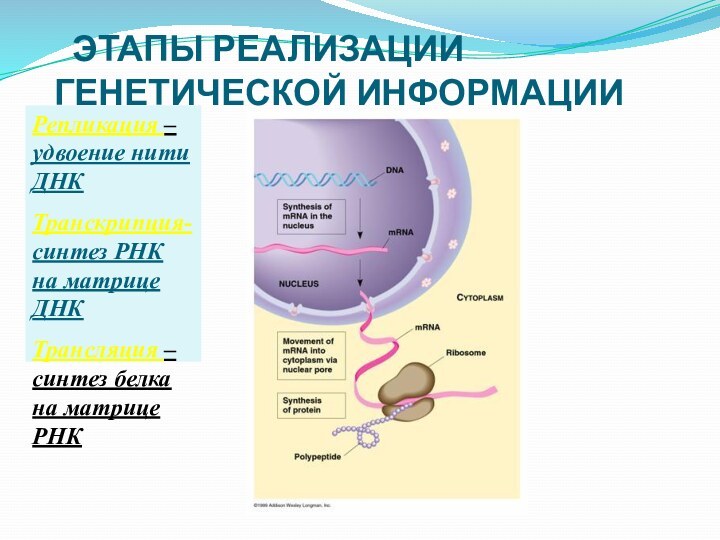
ЭТАПЫ РЕАЛИЗАЦИИ ГЕНЕТИЧЕСКОЙ ИНФОРМАЦИИ
Репликация –удвоение нити ДНК
Транскрипция- синтез РНК на матрице ДНК
Трансляция – синтез
белка на матрице РНК
Слайд 26
ЯДРО - ХРОМОСОМЫ - ДНК– ПЕПТИДЫ - БЕЛКИ
Слайд 27
ПРОЕКТ
ГЕНОМ ЧЕЛОВЕКА
ОФИЦИАЛЬНО
ЗАВЕРШЕН
20 апреля 2003г.
ИССЛЕДОВАНИЯ ГЕНОМА ЧЕЛОВЕКА
АКТИВНО ПРОДОЛЖАЮТСЯ
Слайд 28
Словарь генома
1. Геном –весь наследственный аппарат клетки, её
ДНК
2 .Секвенирование ДНК – выяснение нуклеотидной
последовательности цепочки ДНК
3. Картирование - определение положения гена по отношению
к другим генам - генетическое
к другим ДНК последовательностям - молекулярное
(позиционное)
к рисунку дифференциальной окраске - хромосомное
4. Идентификация гена – установление наличия гена в
библиотеке кДНК, его картирование, выделение в чистом
виде, клонирование вне организма
Слайд 29
ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ГЕНОМА ЧЕЛОВЕКА НА 2006г.
ОБЩИЕ ПОКАЗАТЕЛИ
Длина молекулы
ДНК в каждой клетке 1,5-1,7м
Просеквенировано – 99% эухроматина
Несеквенировано -
10% (9%- гетерохроматина)
Число нуклеотидов в гаплоидном наборе :
всего - 3. 164.7 х 10 6
в эухроматине – 2.900 х 10 6
в гетерохроматине – 0.3 х 10 6
Допустимая частота ошибок 1 х 10 4
Слайд 30
ФУНКЦИОНАЛЬНЫЙ ГЕНОМ ЧЕЛОВЕКА
Транскрибируемая часть
- 28-30% ДНК
до РНК - 23 - 25%
до белка - 5%
Отвечает за синтез белка - 1,2% всей ДНК
«Факультативная » ДНК
LTR, SINE, LINE, Transposones - 50%
короткие повторы (мини- и микро
сателлитная ДНК) - 3%
Повторяющиеся последовательности -
45- 50% всей ДНК
Слайд 31
ГЕНЕТИЧЕСКИЙ ПОЛИМОРФИЗМ
Идентичность геномов разных индивидуумов
- 99,9%
- 0,1% - Межиндивидуальная
2006- 90,9% -10%
вариабельность
Однонуклеотидные замены (SNP) - 10 -12 х 10 6
Внутригенные (смысловые) SNP - 3 - 5 х 10 6
Число картированных SNP в проекте
Гаплоидный геном (HapMap )2006г. 4,5 х 10 6
ПЕРВАЯ ВЕРСИЯ РАЗНООБРАЗИЯ ГЕНОМА ЧЕЛОВЕКА
269 человек (90 белых, 90 африканцев, 89-желтых)
2005г. - 1 млн SNP , 2006г. - 4,6 млн SNP,
2008г. – 9 млн.SNP
Слайд 32
МИНИМАЛЬНОЕ ЧИСЛО ГЕНОВ ЧЕЛОВЕКА
ВСЕГО – около 22 000
Идентифицировано
в библиотеке кДНК - 20 000
Картировано на хромосомах
(31. 08. 07) - 10 432
Идентифицированы и исследованы на
наличие мутаций ( 2003г.) - 1 485
По хромосомам:
хромосома 1 - 3 141
хромосома 21 - 225
хромосома 22 - 525
Х- хромосома - 1 098
РАЗМЕРЫ ГЕНА
Средний - 3 000 п.о.
Максимальный - 2.4 х 10 6 п.о.
Слайд 33
Общая классификация генов
I.РНК-гены (тРНК, рРНК, яРНК, иРНК)
II.Белок-синтезирующие гены
Гены домашнего хозяйства
Гены специальных
функций
III Регуляторные гены (факторы транскрипции)
PAX1-9;HOX 1-35; SOX 1-10; SRY, др.
IV Митохондриальные гены (около 30)
Слайд 34
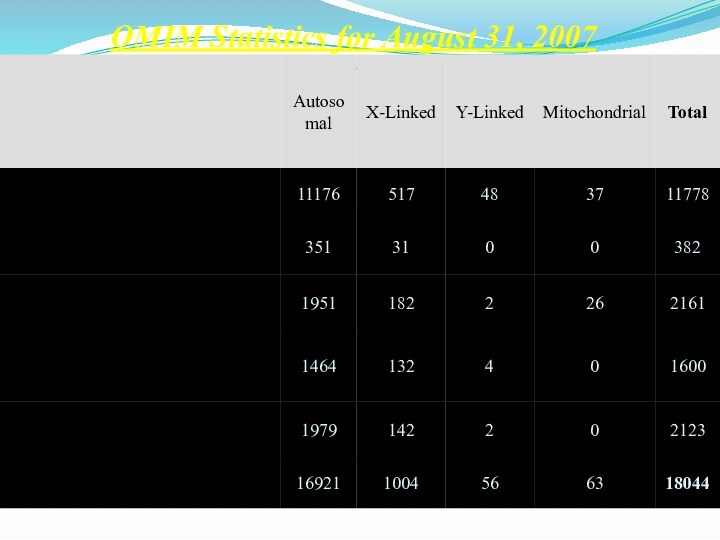
OMIM Statistics for August 31, 2007
Number of Entries
Слайд 35
ГЕНОМ- весь наследственный аппарат клетки, её ДНК
ГЕНОМИКА
– наука о структурно-функциональной организации генома, о взаимодействии генов
и их продуктов в процессах онтогенеза в норме и в патологии
Слайд 36
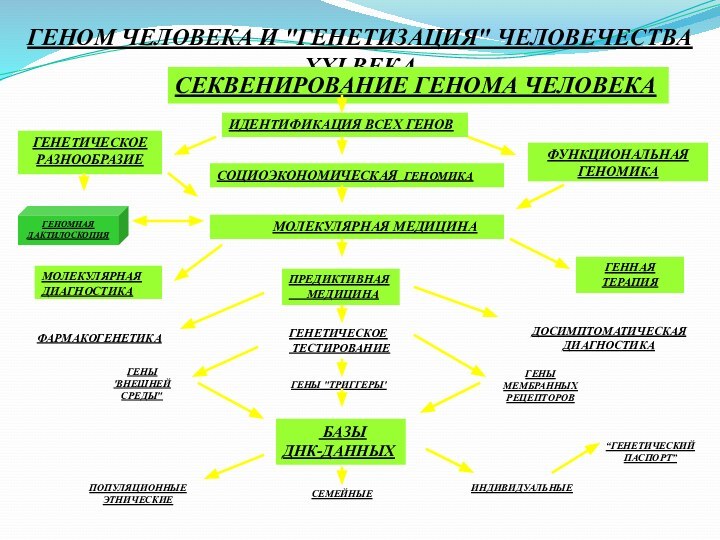
ГЕНОМ ЧЕЛОВЕКА И "ГЕНЕТИЗАЦИЯ" ЧЕЛОВЕЧЕСТВА XXI ВЕКА
Слайд 37
Первый глобальный геноцид – 30 000 лет до
РХ
Слайд 38
СХЕМА ЗАСЕЛЕНИЯ ПЛАНЕТЫ «ЗЕМЛЯ»
ВЕЛИКОЕ ПЕРЕСЕЛЕНИЕ НАРОДОВ
Слайд 40
НОВЫЕ НАПРАВЛЕНИЯ ГЕНОМИКИ
«Гаплоидный геном» (HapMap)- распределение однонуклеотидных
полиморфизмов в гаплоидном наборе 23 хромосом
«Энциклопедия ДНК-элементов»
( ENCODE) идентификация - и картирование белок - синтезирующих элементов генома человека
«Химическая Геномика» –создание библиотеки хим.
в-в, взаимодействующих с геномом человека
«Геном для жизни» - особенности организации геномов патогенных микроорганизмов
Консорциум по структурной геномике – направленный поиск лекарств действующих на геном
«Геном человека и окружающая среда» -”Environmental Genome Project”- развитие предиктивной медицины и фармакогенетики
«Персональный геном» Дж.Черч
Слайд 42
ЧТО УЖЕ ДАЛИ МЕДИЦИНЕ ИССЛЕДОВАНИЯ ГЕНОМА ЧЕЛОВЕКА?
Идентифицированы
мутантные гены всех частых моногенных и многих мультифакториальных
заболеваний
Разработаны универсальные методы диагностики наследственных болезней
Внедрены методы геномной дактилоскопии
Заложены основы фармакогенетики и фармакогеномики
Внедряются методы тестирования наследственной предрасположенности (предиктивная медицина)
Разработаны научные основы и начаты клинические испытания по генной терапии.
Слайд 43
Классификация мутаций
I. ГЕНОМНЫЕ
Диплоидный набор 2n=46
Гаплоидный 1n=23
Полиплоидия
(триплоидия 3n=69; тетраплоидия 4n=92)
Анеуплоидия (трисомия 2n=47; моносомия 2n=45
II. ХРОМОСОМНЫЕ
(делеции, дупликации, инсерции инверсии, транслокации)
III ГЕННЫЕ
Точечные (сайтовые) мутации (нейтральные –SNP,нонсенс, миссенс
Внутригенные перестройки (делеции, дупликации, инверсии, инсерции)
Динамические мутации
Перемещение мобильных элементов(Alu -300-500по х100 000 Line( 6 500по х 50 000
Слайд 44
Патогенез наследственных болезней
I.Хромосомные болезни – дисбаланс 1000 генов
одной хромосомы или её фрагментов
Избыток генетического материала (трисомия) менее
драматичен, чем его отсутствие (моносомия)
Нарушения функции генома на уровне ДНК (дисбаланс структурных и регуляторных генов, микро - РНК), на уровне ядра (нарушения микроархитектоники ядра, локализации гетерохроматина, хромосомных территорий, пр.) - «клеточный синдром», неспецифические и специфические фенотипические проявления
II,Генные болезни- дефекты одного гена: природа гена (гены –господа/ гены –рабы) функция гена (место в генной сети), тип мутации ( плюс /минус -эффекты; доминантные/ рецессивные), первичный биохимический дефект
Слайд 45
Уровни патогенеза наследственных болезней
I. Молекулярный: первичный биохимический
дефект
Отсутствие, недостаток или избыток генопродукта
Неправильный по структуре генопродукт,
Нарушения регуляторных
взаимодействий между генами и целыми генными сетями
II. Клеточный уровень:
Нарушения метаболизма клетки, функций мембранных рецепторов, энергетики клетки:
(Болезни накопления - лизосомные болезни, мукополисахаридозы)
III. Тканевой и органный уровни
Первичная и вторичная гетерогенность (плейотропия) наследственных болезней
Слайд 46
Диагностика хромосомных заболеваний
Цитогенетическая диагностика. Этапы :
:
Приготовление метафазных пластинок
Окраска препаратов
Кариотипирование хромосомных препаратов
Специальные методы:
Гибридизация in situ: варианты FISH, ДНК-зонды,
Метод CGH (Comparative Genome Hybridization)
Молекулярная диагностика хромосомных болезней
Слайд 47
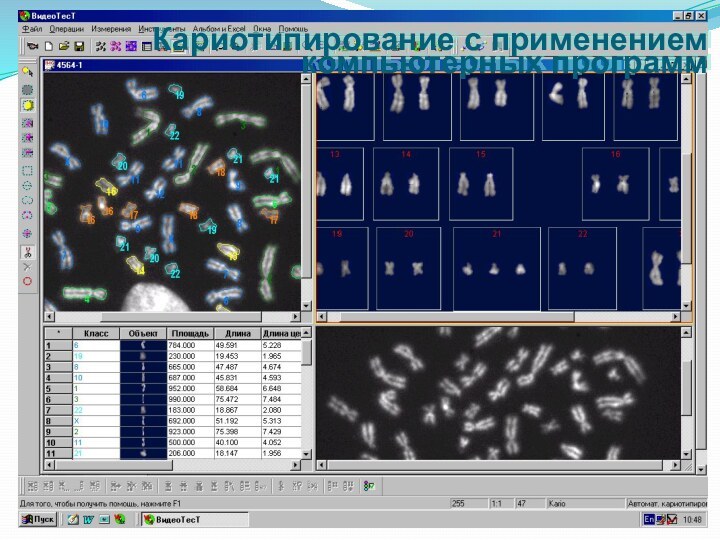
Кариотипирование с применением компьютерных программ
Слайд 48
FISH
с хромосом-специфическими ДНК-пробами
на “прямых” препаратах из
хориона/плаценты
Слайд 49
Диагностика генных болезней
Объектом исследования является молекула ДНК
ДНК-диагностика возможна
на любой стадии онтогенеза
Два варианта ДНК-диагностики:
- прямая –
детекция мутаций
- непрямая – идентификация ДНК-маркера, сцепленного с мутацией или с мутантным геном
ПРИНЦИПЫ ДНК-ДИАГНОСТИКИ
Комплементарность пар оснований
Разделение цепей ДНК при нагревании - денатурация
Объединение комплементарных цепей при охлаждении – ренатурация
Наличие специфических эндонуклеаз
Разделение ДНК-фрагментов электрофорезом в гелях
Полимеразная цепная реакция - ПЦР
Для каждой НБ характерен свой тип мутаций,
свой алгоритм ДНК-диагностики
Слайд 50
Методы детекции мутаций
I. Поиск неизвестных мутаций
конформационный полиморфизм одноцепочечных
фрагментов -SSCP
электрофорез в денатурирующем гралиентом геле DGGE
химическое расщепление некомлементарных
сайтов-CMC
анализ гетеродуплексов -HA
прямое секвенирование -DS
II. Идентификация известных мутаций
Блот - гибридизация по Саузерну (1975)
Полимеразная цепная реакция -ПЦР (1985)
Диагностика с помощью биочипов ( 2 000)
Слайд 51
Технология микробиочипов
Институт молекулярной биологии
им.В.А.Энгельгардта РАН, Москва
Слайд 52
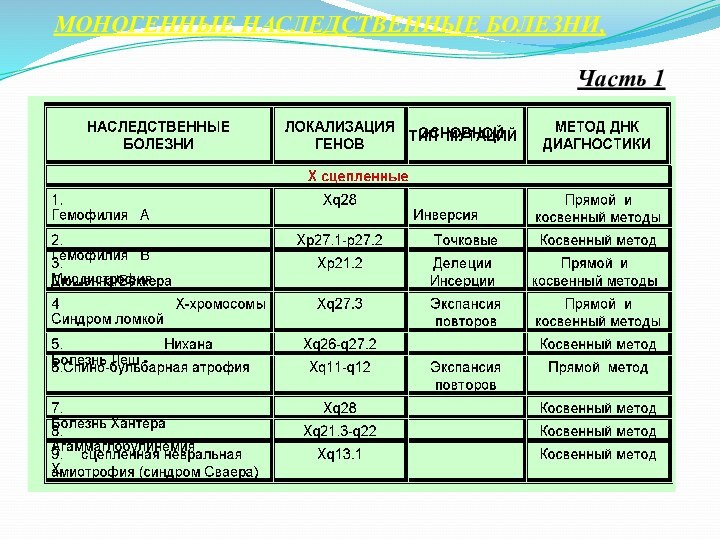
МОНОГЕННЫЕ НАСЛЕДСТВЕННЫЕ БОЛЕЗНИ,
Часть 1
Слайд 53
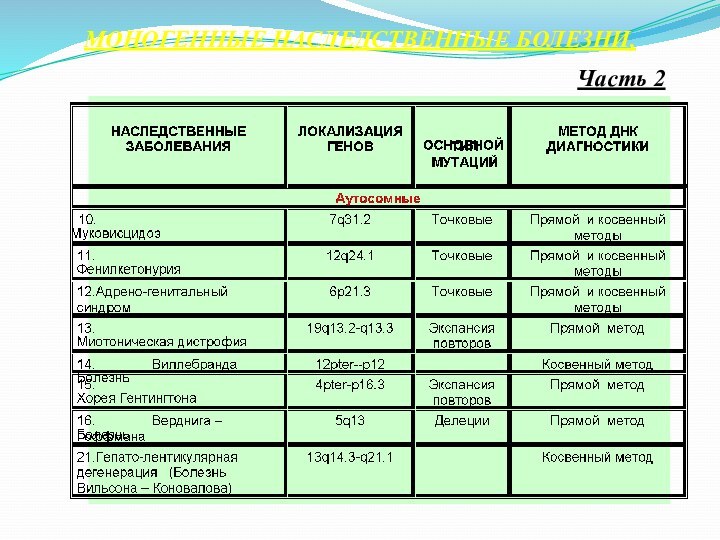
Часть 2
МОНОГЕННЫЕ НАСЛЕДСТВЕННЫЕ БОЛЕЗНИ,
Слайд 54
Идентификацию генов и генных сетей частых мультифакториальных заболеваний;
Диагностику
заболеваний по экспрессионным профилям тысяч генов;
Диагностику наследственной предрасположенности по
тестированию аллельных вариантов "смысловых" SNPs;
Внедрение предиктивного генетического тестирования семей с высоким риском частых мультифакториальных болезней;
Создание индивидуальных, семейных и специализированных баз ДНК-данных (генетический паспорт беременной, спортсмена, призывника и пр.);
Создание новых лекарств направленного действия для индивидуальной молекулярной терапии.
ЧТО ДАДУТ МЕДИЦИНЕ ИССЛЕДОВАНИЯ ГЕНОМА В "ПОСТГЕНОМНУЮ" ЭРУ ?