Слайд 2
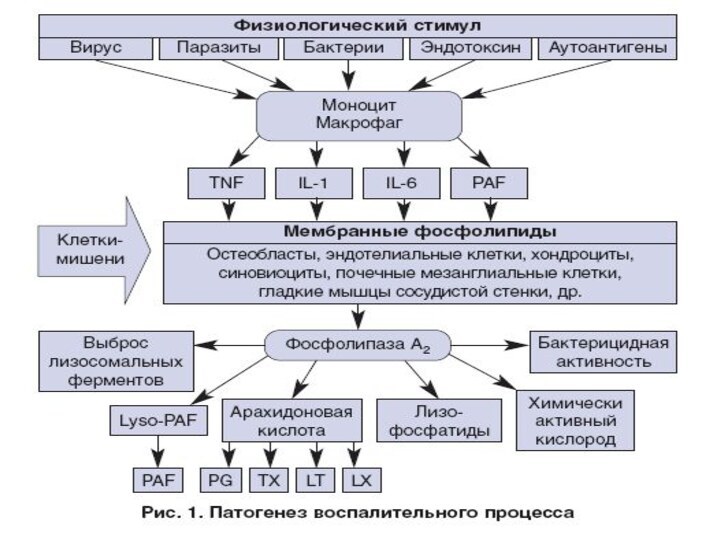
ФАЗЫ ВОСПАЛЕНИЯ
1. Острое воспаление – первоначальный ответ на
поврежд. тканей (опосредован выделением гистамина, серотонина, брадикинина, ПГ, ЛТ)
2.Иммунный
ответ – реакция на присутствие чужеродных антигенов
3. Хронич. воспаление –опосредовано высвобожд. специфических медиаторов (ИЛ-1,2,3; ФНО; CSF-GM; PDGF; интерфероны)
Слайд 3
Эффекты медиаторов острого воспаления
1. Гистамин – вазодилат, сосуд.
проницаемость
2. Серотонин – сосуд. проницаемость
3. Брадикинин – вазодилат., проницаемость,
боль
4. Простагландины –вазодилат., проницаемость,
боль, гипертермия (лихорадка)
5. Лейкотриены – проницаемость, хемотаксис
Слайд 4
Эффекы медиаторов хронического воспаления
ИЛ-1,2,3 (макрофаги Т-лимфоциты) – активация
лимфоцитов, продукция ПГ;
TNF (макрофаги) – продукция простагландинов
Интерфероны (макрофаги, эндотел.
клетки, Т-лимфоциты)
Фактор роста тромбоцитов (PDGF ) (макрофаги, эндотел. клетки, фибробласты, тромбоциты) – хемотаксис фибробластов, пролиферация
Слайд 6
Классификация НПВС
С преимущественным действием на острую фазу воспаления
(эксудативн., альтеративная)
1. Пр-ные салициловой кислоты - салицилаты (ацетилсалициловая к-та,
ацетилсалицилат лизина)
2. Пр-ные пиразолидиндиона – фенилбутазон (бутадион)
3. Пр-ные индолуксусной к-ты –индометацин, сулиндак (метиндол, клинорил)
Слайд 7
Классификация НПВС
4. Пр-ные фенилалкановых кислот- ацеклофенак, диклофенак натрия,
ибупрофен, кетопрофен
5. Оксикамы – пироксикам, мелоксикам, лорноксикам
6. Пр-ные п
– аминофенола - ацетаминофен (парацетамол, панадол)
7. С-ва, содержащие сульфонамидную группу – нимесулид, целекоксиб
8. Ср-ва с разной хим. структурой – кеторолак, к-та тиапрофеновая, набуметон
Слайд 8
Базисные противовоспалительные ср-ва, включены в стандарт медицинской помощи
больным ревматическими заболеваниями
1. Иммунодепрессанты + цитостатические ср-ва: лефлуномид
(арава),
метотрексат, азатиоприн,
циклофосфамид
2. Генно-инженерно-биоло-
гические препараты:
а. блокаторы ФНО-α (моно-
клональные антитела): инфликсимаб (ремикейд), адалимумаб (хумира);
Слайд 9
Базисные ПВС, для лечения ревматических заболеваний (продолжение)
б.
Блокатор рецепторов ИЛ-6: - тоцилизумаб (актемира)
Блокатор
рецепторов ИЛ-1: - анакинра (кинерет)
в. Модуляторы В-клеточного звена иммуните-
та: ритуксимаб (мабтера)
3. Стероидные гормоны – метилпреднизолон, преднизолон, дексаметазон, бетаметазон
4. НПВС – Диклофенак, индометацин, ибупрофен, мелоксикам, нимесулид
Слайд 11
Базисные противовоспалительные ср-ва (вспомогательные)
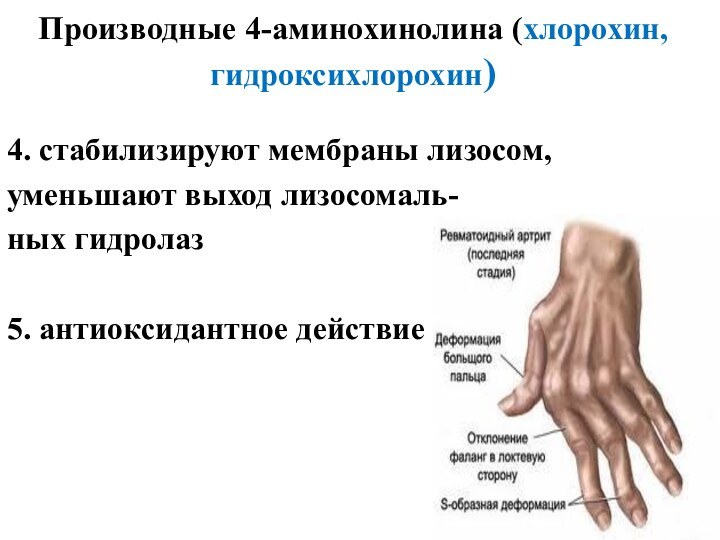
Производные 4-аминохинолина (хлорохин, гидроксихлорохин)
Препараты золота
(кризанол, ауранофин)
Производные D-пеницилл-
амина (пеницилламин,
купренил)
Слайд 12
Торможение молекул клеточной адгезии
подавляют экспрессию молекул адгезии-1, селектинов
в эндотелии сосудов
Подавляют экспрессию молекул адгезии на мембране лейкоцитов
и тромбоцитов – интегринов
Подавляют экспрессию молекул адгезии и нарушает миграцию клеток в очаг воспаления
Слайд 13
Антагонизм НПВС с медиаторами воспаления
Ингибируют ферменты участвующие в
синтезе гистамина, серотонина, брадикинина, простагландинов.
Повышают содержание ц АМФ в
результате блокады ФДЭ
Слайд 14
Антагонизм НПВС с медиаторами воспаления
Подавляют дегрануляцию тучных клеток
и выход из них БАВ (салицилаты, бутадион, диклофенак натрия,
нимесулид)
Блокируют рецепторы гистамина и
серотонина (индометацин, бутадион)
Слайд 16
Индексы ингибирования ЦОГ-1/ЦОГ-2
Индометацин
- 30
Диклофенак Na - 2,2
Мелоксикам
- 0,33
Нимесулид - 0,2
Целекоксиб - 0,001
Слайд 17
Стабилизация лизосом. мембран и антиоксидантный (АО) эффект НПВС
Тормозят
выход лизосом. гидролаз (протеаз,
липаз, фосфатаз), вызывающ. тканевой некроз
НПВС связываясь
с SH- группами цистеина
мембр. белка блокируют вход в лизосомы Сa2+
Снижают вход ионов Сa2+ тормозят ПОЛ
в лизосомальных мембранах
АО эффект НПВС обусловлен торможением
синтеза в ЦОГ реакции эндопероксидов (ПГG2 и ПГН2 )
Слайд 18
Торможение энергопродукции в очаге воспаления
Биохимические реакции, лежащие в
основе воспаления – высоко энергозатратны:
синтез медиаторов воспаления
хемотаксис
фагоцитоз
пролиферация соединительной ткани
НПВС нарушают синтез АТФ (подавляю
гликолиз и аэробное окисление, разобщают ОФ)
Слайд 19
Влияние НПВС на процессы пролиферации
НПВС тормозят формирование соединительной
ткани
(синтез коллагена):
Снижают активность фибробластов
Нарушают энергообеспечение пролифера-
тивных
процессов
Наибольшим антипролиферативным эффектом
обладают индометацин, диклофенак натрия, ацеклофенак, пироксикам, лорноксикам, мелоксикам
Слайд 20
Иммунотропное действие НПВС
Подавляют активацию фактора транскрипции (NF-kB) в
Т-лимфоцитах
Ингибируют синтез цитокинов (ИЛ-1,6,8, интерферон-β, ФНО-α), ревматоидного фактора, комплемента
и молекул адгезии
Снижают общую иммунологическую реактивность
Угнетают специфические реакции на нтигены
Слайд 21
Механизм обезболивающего действия
Снижают гипералгезию в результате:
блокады синтеза ПГ
и простациклина,
которые потенцируют раздражающ. дей-е
ИЛ-1, ФНО-α, гистамина, серотонина,
брадикинина и
нейрокининов на болевые
рецепторы.
Уменьшения отека и механического
раздражения болевых рецепторов в
замкнутых полостях
Слайд 22
Механизм обезболивающего действия (продолжение)
Уменьшают поток болевых импульсов из
зоны воспаления в ЦНС
Ингибируют ЦОГ-2 и синтез ПГЕ в
ЦНС, где он участвует в проведении и восприятии боли.
Повышают высвобождение эндорфинов и усиливают блокаду NMDA рецепторов глутаминовой кислоты
Слайд 23
По мере убывания обезболивающего эффекта препараты располагаются:
Кетопрофен, лорноксикам,
мелоксикам,
пироксикам, нимесулид
ацеклофенак→напроксен, целекоксиб→индо-
метацин →бутадион→анальгин→ибупрофен
→парацетамол →кислота ацетилсалициловая
Слайд 24
Механизм формирования лихорадки
В очаге воспаления в избытке образуются
индукторы ЦОГ-2 (ИЛ-1,6, ФНО-α, интерфероны α и γ
и др. пирогены)
Индукция ЦОГ-2 в преоптической области гипоталамуса сопровождается увеличением синтеза ПГЕ2
В тепловом центре гипоталамуса ПГЕ2 увеличивает содержание ц АМФ, что сопровождается стимуляцией функии центра теплопродукции
Слайд 25
Жаропонижающее действие НПВС
В очаге воспаления блокируют ЦОГ-2
Угнетают
синтез ПГЕ2 - его содержание в тепловом центре
гипоталамуса снижается
Восстанавливают равновесие между функциональными центрами теплопродукции и теплоотдачи в гипоталамусе
НПВС расширяют сосуды кожи и увеличива-
ют теплоотдачу
Слайд 26
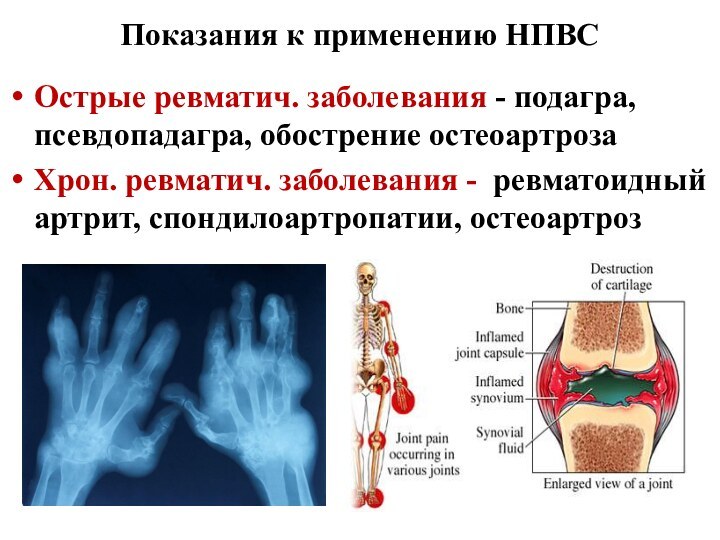
Показания к применению НПВС
Острые ревматич. заболевания - подагра,
псевдопадагра, обострение остеоартроза
Хрон. ревматич. заболевания - ревматоидный артрит, спондилоартропатии,
остеоартроз
Слайд 27
Показания к применению НПВС (продолжение)
Острые неревматич. заболевания -
травмы,
боли в спине, послеоперационная боль,
почечная колика, дисменорея,
мигрень и др.
Другие заболевания - плеврит, перикардит, узловатая эритема, полипоз толстого кишечника; профилактика – тромбоз, рак толстого кишечника
Слайд 28
Побочное действие НПВС
Ульцерогенное действие обусловлено 2-мя механизмами
1. Местным
повреждением клеток слизистой желудка в результате накопления в нейтральной
среде цитоплазмы НПВС
2. Системным истощением цитопро-
текторных ПГ
Слайд 29
Местное повреждение клеток слизистой желудка в результате накопления
в цитоплазме НПВС
Нарушают состав фосфолипидов, гликопро-теинов, гликолипидов эпителиальных клеток
(дезорганизация желудочного сурфактанта)
Разобщают окислительное фосфорилирование
Стимулируют карбоангидразный механизм секреции HCL (индометацин)
Слайд 30
Системное истощение цитопротекторных ПГ
Ингибирование ЦОГ-1 с последующим снижением
синтеза ПГ и простациклина
Снижение содержания ПГ в слизистой желуд-
ка сопровождается:
а) повышением кислотности и перевариваю-
щей способности желудочного сока
б) снижением энергопродукции и дефицитом
цАМФ в эпителиальных клетках
Слайд 31
Системное истощение цитопротекторных ПГ (продолжение)
снижение кровотока и
регенераторного
потенциала тканей
снижение секреции бикарбонатов и
гликозаминогликанов слизи
Повышение содержания лейкотриена В4 ,
вызывающего лейкоцитарную
инфильтрацию
Слайд 32
Ульцерогенное действие
Сильное ульцерогенное д-е
Кеторолак, пирокси-
кам, лорноксикам,
индометацин, бутади-
он, к-та
ацетилсали-
циловая (аспириновая
язва), к-та тиапро-
феновая
Слабое ульцерогенное д-е
Сулиндак, диклофе-
нак натрия, ибупрофен,
напроксен и др.
Наиболее безопасные!!
Ацеклофенак, нимесу-
лид, целекоксиб, набу-
метон
Слайд 33
Рекомендации по ведению больных с поражением ЖКТ НПВС
Симптоматические
побочные эфекты
→антагонисты Н2 рецепторов (ранитидин);
или ингибиторы протонного насоса
(омепразол)
Активная язва, отменить НПВС невозможно!!
→ингибиторы протонного насоса (омепразол)
Активная язва, отменить НПВС можно → рани-
тидин, омепразол
Профилактика → отменить НПВС, мизопро-
стол, Н2-блокаторы, блокаторы протон. помпы
Слайд 34
Аспирин-индуцированное респираторное заболевание (аспириновая астма)
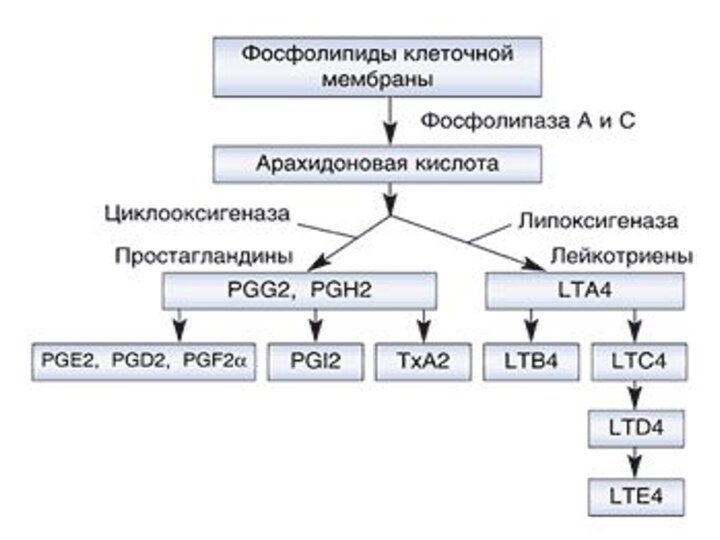
Патогенез аспириновой астмы связан
с переключением метаболизма арахидоновой кислоты с ЦОГ- пути на
липоксигеназный.
В результате шунтирования метаболизма на липоксигеназный путь ↑ синтез лейкотриенов (С4 , D4 и Е4), которые вызывают бронхоспазм, стимулируют образование бронхиальной слизи, отек и клеточную инфильтрацию.
Лечение аспириновой астмы – зафирлукаст, монтелукаст (блокаторы LT-рецепторов)
Слайд 35
Энцефалопатия + жировая дистрофия печени (синдром Рейе)
На
фоне вирусных инфекций прием АСК может
вызвать синдром Рейе
(чаще страдают дети в
возрасте от 4-16 лет), проявляется в течение 3-7
дней от начала вирусной инфекции.
Без лечения в 30-70% случаев синдром Рейе заканчивается летальным исходом.
Причины развития синдрома Рейе: под влиянием АСК и вирусных антигенов нарушается в митохондриях β-окисление жирных кислот. Накапливающиеся ЖК и аммиак оказывают токсическое д-е на мозг, печень
Слайд 36
Медленно действующие БПВ средства
Производные 4-аминохинолина (хлорохин, гидроксихлорохин)
Фармакодинамика –
1. блокируют синтез ДНК и РНК в клетках, нарушают
деление клеток;
2. угнетают продукцию лимфоцитами ИЛ-2 и моноцитами ИЛ-1
3. угнетают хемотаксис лейкоцитов
Слайд 37
Производные 4-аминохинолина (хлорохин, гидроксихлорохин)
4. стабилизируют мембраны лизосом,
уменьшают
выход лизосомаль-
ных гидролаз
5. антиоксидантное действие
Слайд 38
Пенициламин (купренил)
Фармакодинамика –
1. ингибирует активность металоферментов (супероксиддисмутазы,
снижает содержание в тканях АФК);
2. Хелатирует металлы (ограничивает биологическую
активность Fe++ ; Cu++ их элиминации из организма
Слайд 39
Пенициламин (купренил)
продолжение
3. Угнетает Т- хелперную активность лимфоцитов,
снижает хемотаксис нейтрофилов
4. Угнетает синтез коллагена (ингибирует пролингидроксилазу)
5. Ингибирует
синтез иммунных комплексов
Слайд 40
Базисные противовоспалительные ср-ва (Генно-инженерно-биологические препараты)
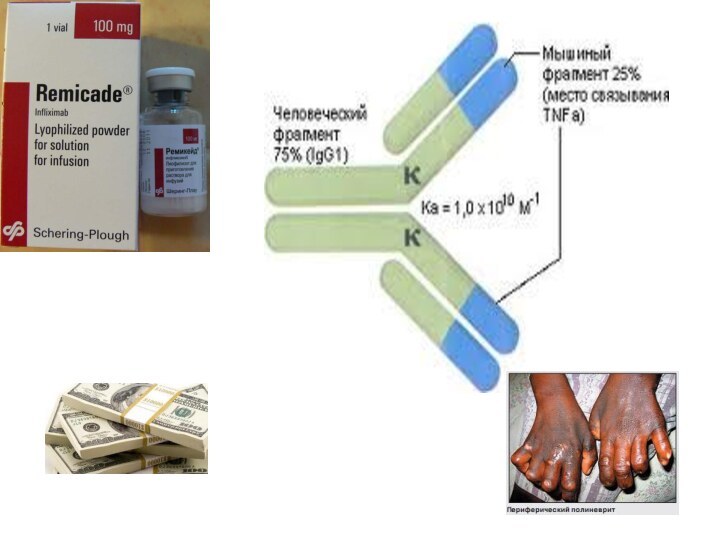
Химерные моноклональные антитела –
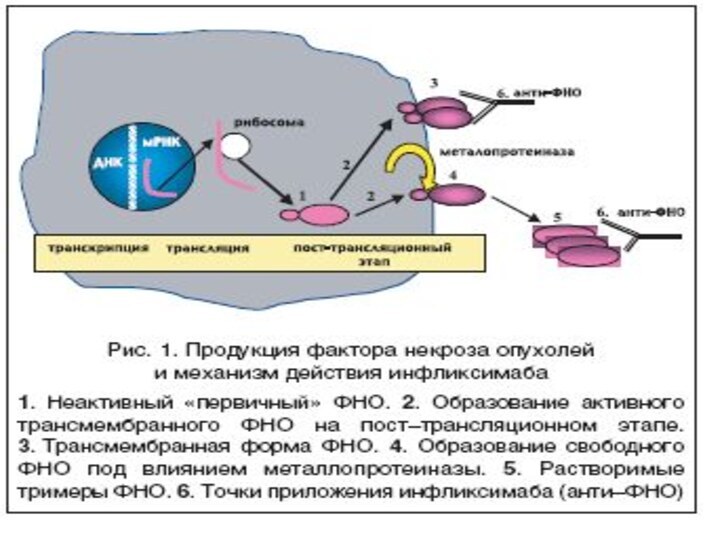
блокаторы ФНО - альфа - инфликсимаб (ремикейд)
1. Инфликсимаб
(ремикейд) – образует устойчи
вое соединение с растворимой и
трансмембранной формами челове
ческого ФНО-α
Показания: Ревматоидный артрит
Слайд 44
Базисные противовоспалительные ср-ва (Генно-инженерно-биологические препараты)
Блокатор ИЛ-6 зависимой клеточной
активации
Ингибирует мембран-
ные и цитозольные реце-
пторы ИЛ-6
Показания: Ревматоидный
артрит. Эффект
наблюдает
ся на 2-ой неделе. Сохраняет-
ся более 18 недель.
Слайд 45
Базисные противовоспалительные ср-ва (Генно-инженерно-биологические препараты)
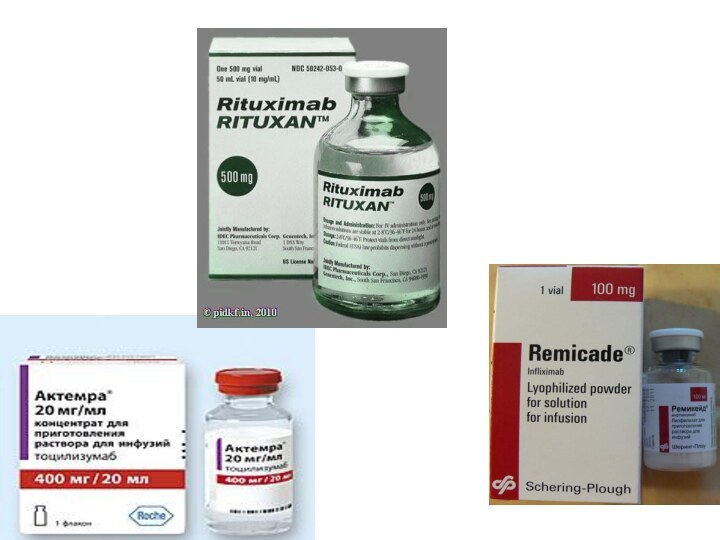
Ингибитор В-клеточного звена иммунитета
- Ритуксимаб (мабтера)
Химерные моноклональные
антитела к СD20 антигену
человеческих В клеток
Показания: Ревматоидный
артрит,
Слайд 47
Медленно действующие противовоспалительные ср-ва
ЛЕФЛУНОМИД (АРАВА) – оказывает выраженное
антипролиферативное, иммуно-
супрессивное, противовоспа-
лительное действие.
Механизм антипролифера-
тивного действия:
1. Ингибирует de
novo синтез
пиримидиновых нуклеотидов лимфоцитов, в поздней фазе клеточного цикла
Слайд 48
Механизм антипролиферативного
действия: ЛЕФЛУНОМИДА (продолжение)
2. Ограничивает пролиферацию Т-лимфоцитов
на
стадии G1 клеточного цикла в результате
ингибирования фермента дигидрооротат дегидрогеназы
3. Блокирует факторы активирующие транскрип-
цию, регулирующие синтез провоспалительных
медиаторов
Слайд 49
Механизм антипролиферативного
действия: ЛЕФЛУНОМИДА (продолжение)
4. Тормозит экспрессию рецепторов
к
ИЛ-2 и ядерных антигенов ( маркеров пролиферации), связанных
с клеточным циклом
Слайд 50
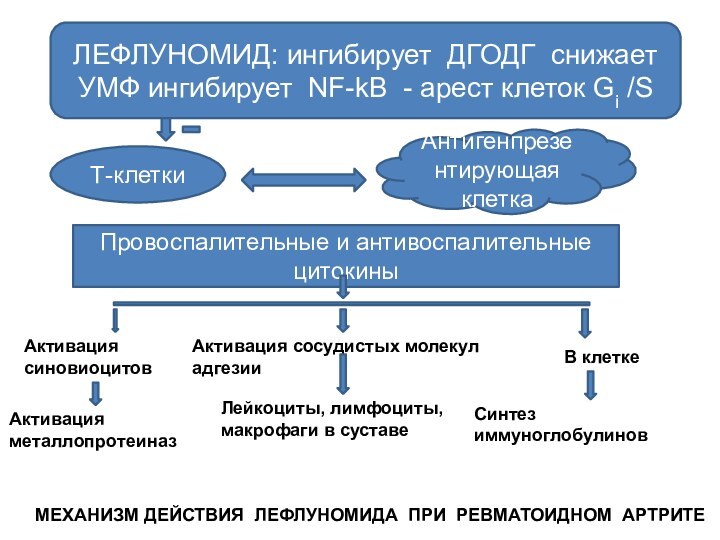
ЛЕФЛУНОМИД: ингибирует ДГОДГ снижает УМФ ингибирует NF-kB -
арест клеток Gi /S
Т-клетки
Антигенпрезентирующая клетка
Провоспалительные и антивоспалительные цитокины
Активация синовиоцитов
Активация
сосудистых молекул адгезии
В клетке
Активация
металлопротеиназ
Лейкоциты, лимфоциты,
макрофаги в суставе
Синтез иммуноглобулинов
МЕХАНИЗМ ДЕЙСТВИЯ ЛЕФЛУНОМИДА ПРИ РЕВМАТОИДНОМ АРТРИТЕ
Слайд 51
Фармакокинетика Лефлуномида
Лефлуномид (арава) пролекарство – в результате метаболизма
в печени и стенке кишечника образуется активный метаболит.
Биодоступность при
приеме внутрь 80-95%,
период полуэлиминации метаболита (Т1/2)- 14 сут
Лечебный эффект наблюдается через 4-6 недель, в дальнейшем нарастает в течение 4-6 месяцев
Слайд 52
Базисный противоревматический препарат Лефлуномид (арава)
Показания к применению: лечение
активной фор-
мы ревматоидного артрита, для уменьшения
симптомов и задержки
структурных повреждений суставов.
Побочные эффекты: повышение АД, диспепсия, повышение уровня печеночных трансаминаз, лейкопения