Слайд 2
Основные функции селезёнки:
высвобождЛимфатические узлы
Это многочисленные органы иммунной системы.

У взрослого человека их около пятисот. Они расположены по
пути тока лимфы. Это такие образования круглой или овальной формы, размер которых от 2 до 20 мм. Находятся они в местах слияния лимфатических сосудов — под мышками, в паху, в шее, в области таза.
Лимфатические узлы
Это многочисленные органы иммунной системы. У взрослого человека их около пятисот. Они расположены по пути тока лимфы. Это такие образования круглой или овальной формы, размер которых от 2 до 20 мм. Находятся они в местах слияния лимфатических сосудов — под мышками, в паху, в шее, в области таза.
Лимфатический узел состоит из соединительнотканной капсулы и лимфоидной ткани. Он служит барьером для распространения инфекции и раковых клеток по организму. В лимфатическом узле образуются лимфоциты, которые активно участвуют в уничтожении чужеродных веществ и клеток.
Основные функции лимфатических узлов: задержка бактерий и вирусов по пути тока лимфы; кроветворная функция.
Пейеровы бляшки
Это узелковые скопления овальной или круглой формы, которые находятся в лимфоидной ткани. Располагаются они в слизистой оболочке тонкой кишки. Их диаметр — от 0,5 до 3 мм.
Основные функции пейеровых бляшек:
участие в процессе созревания Т- и В-лимфоцитов;
формирование иммунного ответа организма.
Слайд 3
Фундаментальным и наиболее исследованным свойством иммуноглобулинов является их
способность связывать и нейтрализовать самые разнообразные по структуре соединения
–антигены.
Однако за последние два десятилетия открыты первые природные антитела c каталитической активностью, катализирующие самые разные химические реакции
Антитела-ферменты (АntiBody - enzyme) получили название “абзимы” (ABZYME)
Такие антитела появляются в биологических жидкостях больных
различными аутоиммунными заболеваниями
Слайд 4
В настоящее время показано существование двух путей наработки
антител ферментов.
Первый путь – наработка антител к молекулам, моделирующим
переходные состояния химических реакций
Слайд 5
Еще одним путем генерации индуцированных абзимов является аутоиммунизация
организма различными ферментами и наработка антител против активных центров
ферментов.
Активный центр фермента в этом случае играет роль первого антигена (АГ1), на который вырабатываются первые идиотипические АТ1, которые являются слепком с активного центра фермента. АТ1 в свою очередь также являются антигеном, на который вырабатываются вторичные –антиидиотипические АТ2, которые содержат элементы, соответствующие внутреннему образу активного центра фермента и могут обладать каталитической активностью
Согласно сети Эрне могут быть вплоть до нескольких этапов наработки антител – экспериментально показано формирование АТ4
Слайд 6
К настоящему моменту открыты природные абзимы, гидролизующие:
1.
Белки
2. ДНК
3. РНК
4. Полисахариды
5. Нуклеотиды (АТР и
т.д.)
ФОСФОРИЛИРУЮЩИЕ:
Белки
2. Липиды
3. Полисахариды
С функциями фермента пероксидаз и оксидоредуктаз
Слайд 7
К настоящему моменту показано, что ДНК-гидролизующие абзимы отсутствуют
у здоровых доноров, но есть в крови пациентов с
:
Системная красная волчанка
Рассеянный склероз
Полиартрит и полимиозит
Аутоимунный тиреоидит (Тиреореодит Хашимото)
5. ВИЧ-инфекция
6. Клещевой энцефалит
7. Вирусный гепатит
8. Шизофрения
9. Сахарный диабет
10. Кровь и молоко лактирующих женщин
Слайд 8
Отнесение каталитической активности непосредственно к абзимам требует проверки

большого числа жёстких критериев
Основные критерии: а) АТ должны быть
электрофоретически гомогенными при нанесении на дорожку геля 10-15 мкг и последующей окраске геля серебром;
б) гель-фильтрация АТ в условиях диссоциации сильных нековалентных комплексов в кислом буфере (рН 2,6) не должна приводить к исчезновению активности и положение пика активности должно совпадать с таковым для интактных антител
в) при нанесении АТ на колонки с сорбентами, содержащими иммобилизованные антитела животных против человеческих антител, в элюате не должно быть активности; пик ферментативной активности при специфической элюции АТ с сорбента кислым буфером должен совпадать с пиком антител;
г) каталитической активностью должны обладать F(ab) и F(ab)2 фрагменты АТ; д) cродство антигенов-субстратов к абзимам должно быть выше, чем к каноническим ферментам.
д) После SDS-PAGE положение пика активности должно совпадать с положением белковой полосы антител
Слайд 9
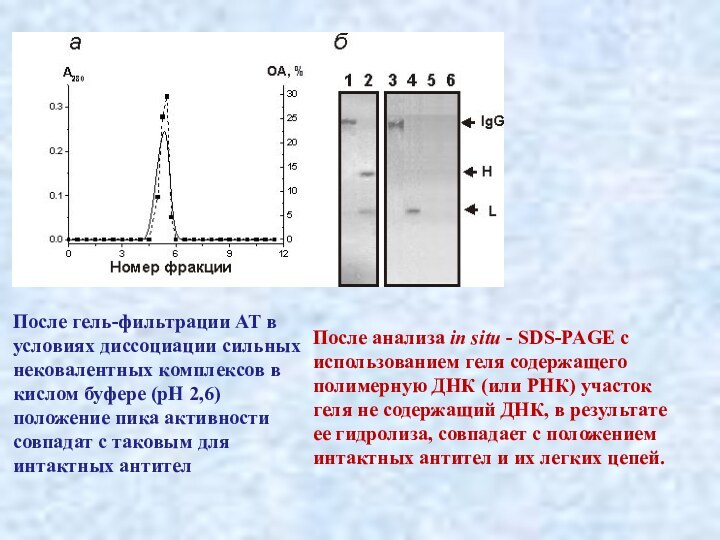
После гель-фильтрации АТ в условиях диссоциации сильных нековалентных
комплексов в кислом буфере (рН 2,6) положение пика активности
совпадат с таковым для интактных антител
После анализа in situ - SDS-PAGE c использованием геля содержащего полимерную ДНК (или РНК) участок геля не содержащий ДНК, в результате ее гидролиза, совпадает с положением интактных антител и их легких цепей.
Слайд 10
Показано, что анализ относительной активности антител в гидролизе
ДНК может быть использован для оценки глубины аутоиммунных реакций
при аутоиммунных заболеваниях
Относительная активность ДНК-гидролизующих антитед очень сильно
зависит от пациента
K1 1 2 3 4 5 6 7 8 9 10 K2 K3
Относительная активность антител 10 пациентов
Слайд 11
Эффект лечения больных
аутоиммунным тиреоидитом плаквинилом
Слайд 12
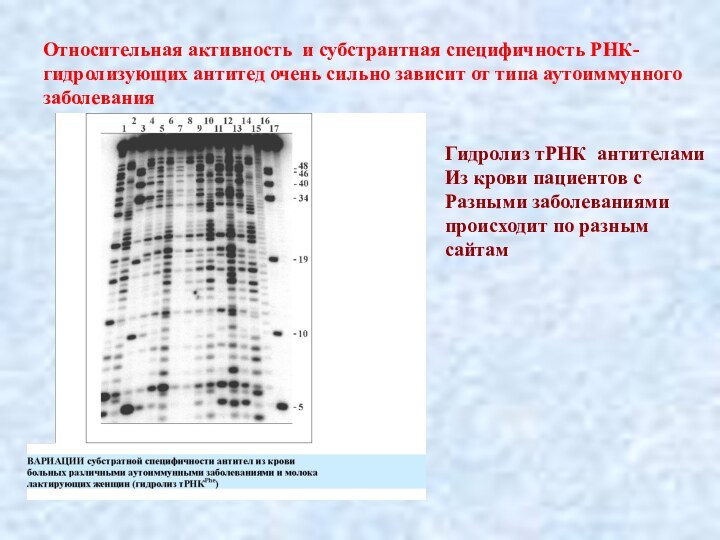
Относительная активность и субстрантная специфичность РНК-гидролизующих антитед очень
сильно зависит от типа аутоиммунного заболевания
Гидролиз тРНК антителами
Из крови
пациентов с
Разными заболеваниями
происходит по разным
сайтам
Слайд 13
Впервые показано, что абзимы крови больных рассеянным склерозом
специфично гидролизуют основный белок миелина – белково-липидной оболочки аксонов,
такие активности появляются на ранних стадиях заболевания и анализ их активности может быть использован для диагностики заболевания.
Активность IgG антител существенно ниже, чем IgM абзимов; у здоровых доноров такой активности иммуноглобулинов нет
Слайд 14
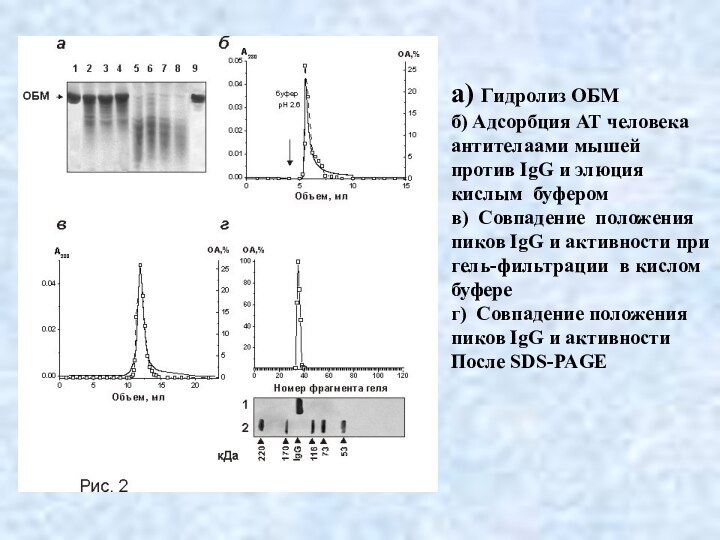
а) Гидролиз ОБМ
б) Адсорбция АТ человека
антителаами мышей
против
IgG и элюция
кислым буфером
в) Совпадение положения
пиков IgG и
активности при
гель-фильтрации в кислом
буфере
г) Совпадение положения
пиков IgG и активности
После SDS-PAGE
Слайд 15
На примере антител, гидролизующих основной белок миелина, нами
впервые показано, что антитела с протеолитической активностью могут быть
металло-протеазами
Небольшая фракция антител имеет сродство к сорбенту Chelex, связывающему металлы. Эта фракция антител гидролизует основной белок миелина только в присутствии ионов металлов:
Дорожка 1 – hMBP инкубиро- ванный без АТ, дорожки 2 – 6 в присутствии IgG: 2 – без Me2+ ионов, 3 – 5 мМ CaCl2 4 – 5 мМ CuCl2, 5 – 5 мМ MnCl2 6 – 5 мМ MgCl2.
Металло-протеаза
Слайд 16
Зависимые и независимые от ионов металлов антитела, гидролизующие
основной белок миелина обнаружены в крови пациентов с:
Рассеянный склероз
Системная
красная волчанка
Шизофрения
Слайд 17
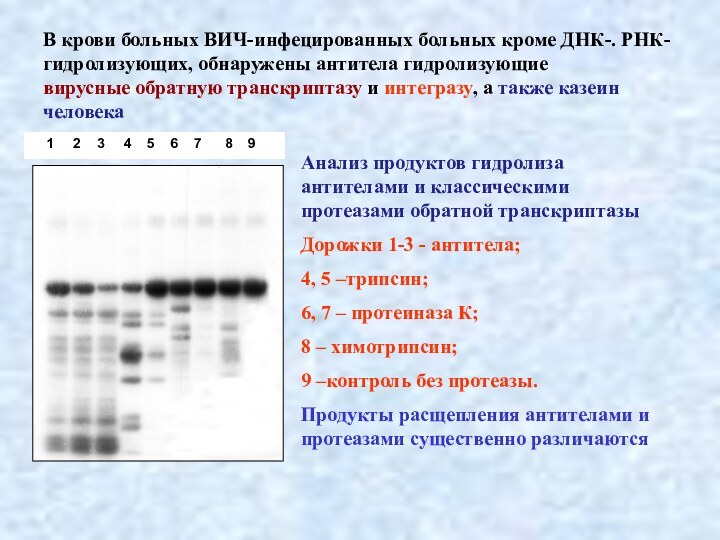
В крови больных ВИЧ-инфецированных больных кроме ДНК-. РНК-
гидролизующих, обнаружены антитела гидролизующие
вирусные обратную транскриптазу и интегразу,
а также казеин человека
Анализ продуктов гидролиза антителами и классическими протеазами обратной транскриптазы
Дорожки 1-3 - антитела;
4, 5 –трипсин;
6, 7 – протеиназа К;
8 – химотрипсин;
9 –контроль без протеазы.
Продукты расщепления антителами и протеазами существенно различаются
Слайд 18
Как указывалось ранее, теоретически количество антител против одного
антигена может быть очень большим – до одного миллиона.
Реально их образуется в организме человека намного меньше, но все равно много.
У больных АИЗ может формироваться в зависимости от индивида и его заболевания относительно узкий или достаточно обширный набор моноклональных ДНК-, РНК- и белок- и других гидролизующих абзимов в составе поликлональных IgG, IgA и IgM, которые исключительно гетерогенны и могут содержать легкие цепи как k-, так l-типа, быть антителами разных классов и подклассов, проявлять максимальную активность при различных значениях pH, иметь различные суммарные заряды, характеризоваться разным сродством к ДНК, РНК и белкам, проявлять различную зависимость активности от ионов одно- и двухвалентных металлов, самое разное сродство к антигенам-субстратам, а абзимы с протеолитической активностью могут быть протеазами четырех разных типов – сериновыми, тиоловыми, кислыми и металло-протеазами.
Слайд 19
Одним из путей разделения разных абзимов является аффинная
хроматография на сорбентах с иммобилизованными субстратами.
Например, аффинная хроматография
антител на ДНК-целлюлозе приводит к разделению IgG с ДНКазной активностью на очень большое число подфракций. Эти подфракции демонстрируют различное сродство к ДНК и различные уровни относительной активности в присутствии и отсутствии ионов разных металлов (Mg2 +, Mn2 + и Ca2 +).
Слайд 20
.
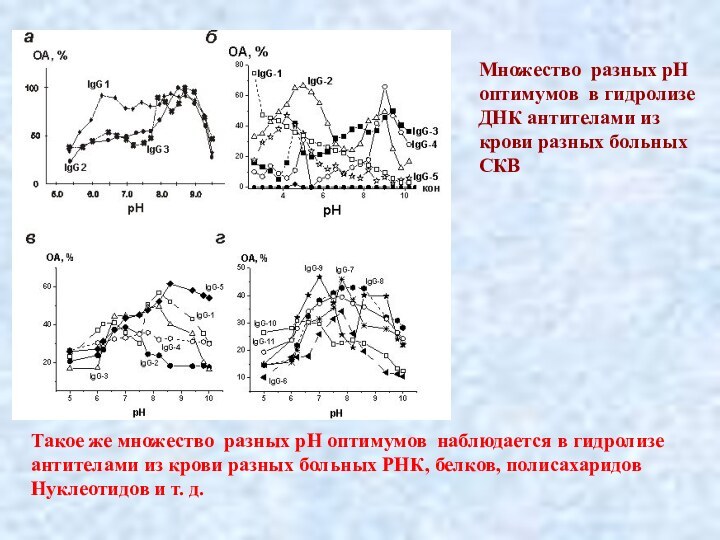
Множество разных рН
оптимумов в гидролизе
ДНК антителами из
крови разных
больных
СКВ
Такое же множество разных рН оптимумов
наблюдается в гидролизе антителами из крови разных больных РНК, белков, полисахаридов
Нуклеотидов и т. д.
Слайд 21
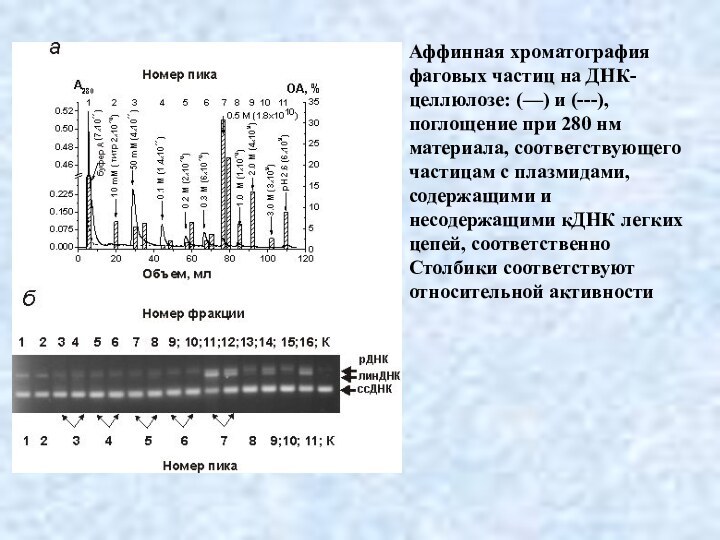
Аффинная хроматография фаговых частиц на ДНК-целлюлозе: (—) и
(---), поглощение при 280 нм материала, соответствующего частицам с
плазмидами, содержащими и несодержащими кДНК легких цепей, соответственно
Столбики соответствуют относительной активности
Слайд 22
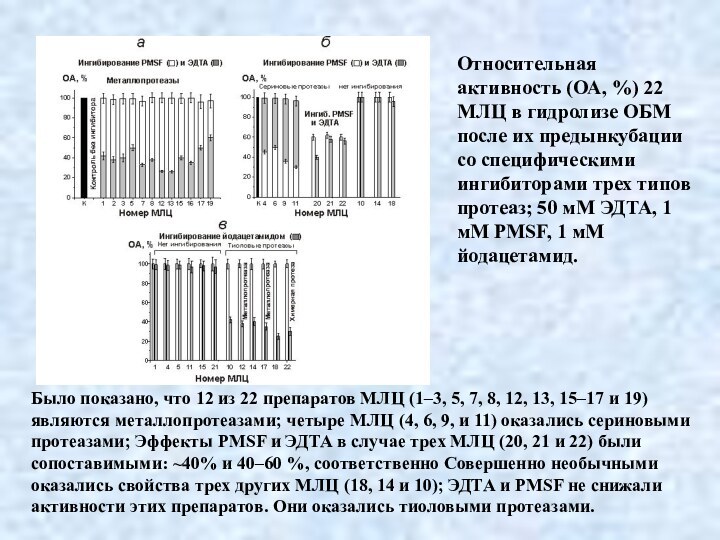
Относительная активность (ОА, %) 22 МЛЦ в гидролизе
ОБМ после их предынкубации со специфическими ингибиторами трех типов
протеаз; 50 мM ЭДТА, 1 мM PMSF, 1 мМ йодацетамид.
Было показано, что 12 из 22 препаратов МЛЦ (1–3, 5, 7, 8, 12, 13, 15–17 и 19) являются металлопротеазами; четыре МЛЦ (4, 6, 9, и 11) оказались сериновыми протеазами; Эффекты PMSF и ЭДТА в случае трех МЛЦ (20, 21 и 22) были сопоставимыми: ~40% и 40–60 %, соответственно Совершенно необычными оказались свойства трех других МЛЦ (18, 14 и 10); ЭДТА и PMSF не снижали активности этих препаратов. Они оказались тиоловыми протеазами.
Слайд 23
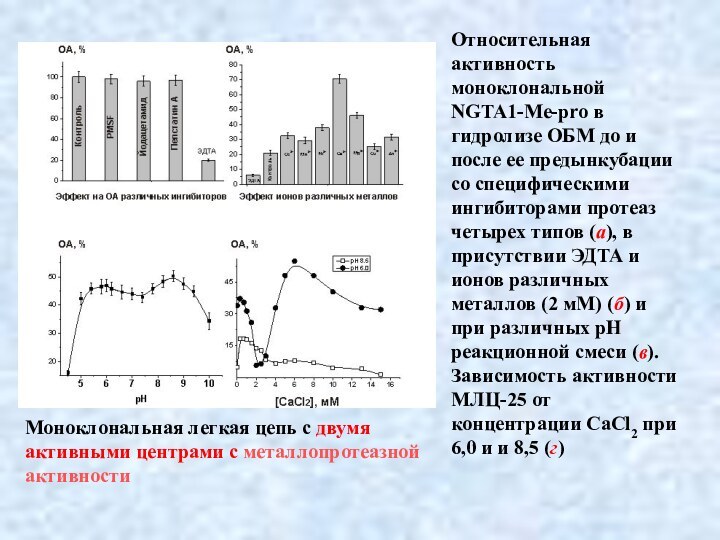
Относительная активность моноклональной NGTA1-Me-pro в гидролизе ОБМ до
и после ее предынкубации со специфическими ингибиторами протеаз четырех
типов (а), в присутствии ЭДТА и ионов различных металлов (2 мМ) (б) и при различных рН реакционной смеси (в). Зависимость активности МЛЦ-25 от концентрации СаСl2 при 6,0 и и 8,5 (г)
Моноклональная легкая цепь с двумя
активными центрами с металлопротеазной
активности
Слайд 24
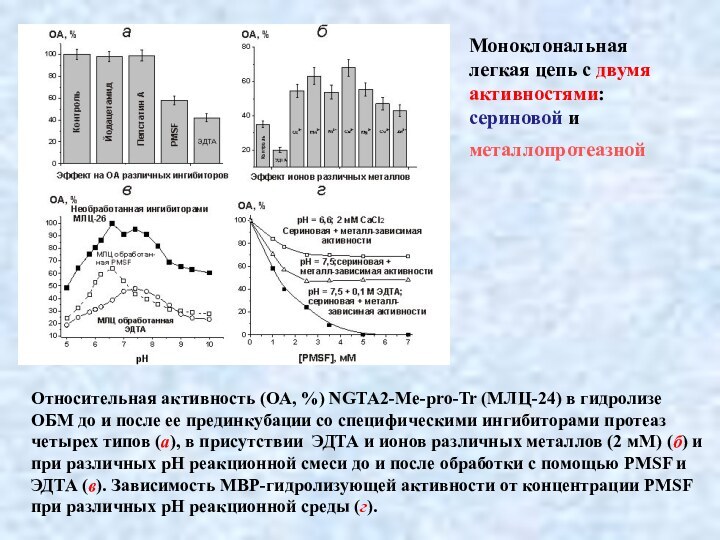
Относительная активность (ОА, %) NGTA2-Me-pro-Tr (МЛЦ-24) в гидролизе
ОБМ до и после ее прединкубации со специфическими ингибиторами
протеаз четырех типов (а), в присутствии ЭДТА и ионов различных металлов (2 мМ) (б) и при различных рН реакционной смеси до и после обработки с помощью PMSF и ЭДТА (в). Зависимость МВР-гидролизующей активности от концентрации PMSF при различных рН реакционной среды (г).
Моноклональная
легкая цепь с двумя
активностями:
сериновой и
металлопротеазной
Слайд 25
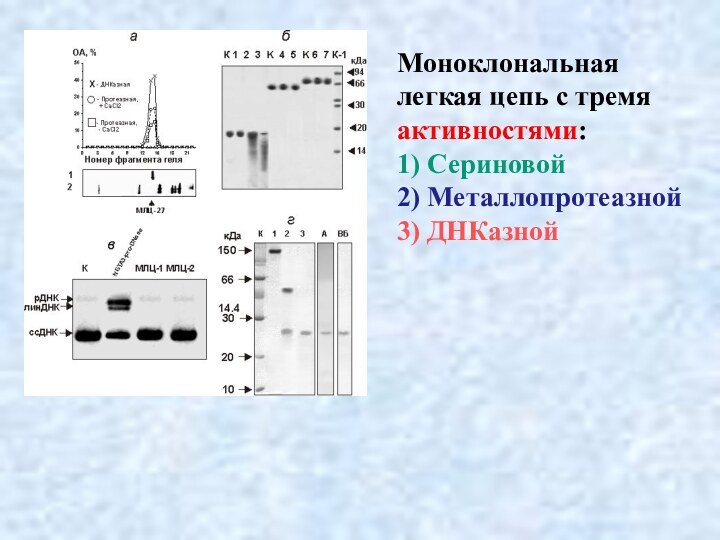
Моноклональная
легкая цепь с тремя активностями:
1) Сериновой
2) Металлопротеазной
3)
ДНКазной
Слайд 26
Современная теория кроветворения, основанная на унитарной теории отечественного
гистолога А.А. Максимова, различает шесть классов кроветворных клеток. Нормальное
кроветворение поликлональное, т.е. с одновременным участием многих клеточных клонов. Все клетки крови происходят из единой родоначальной клетки — полипотентной стволовой кроветворной клетки. При делении стволовая клетка образует две клетки, одна из них сохраняет свойства стволовой, а другая обладает способностью к дифференцировке во все без исключения клетки крови.
1. Мегакариоцитарному, заканчивающемуся образованием тромбоцитов.
2) Эритроидному, приводящему к формированию безъядерных, переносящих кислородэритроцитов крови;
3) Гранулоцитарному - с тремя дополнительными направлениями дифференцировки, заканчивающимися образованием трех самостоятельных клеточных типов: базофилов,эозинофилов и нейтрофилов.
Слайд 27
4) Моноцитарно-макрофагальному. На территории костного мозга дифференцировка в

данном направлении завершается образованием моноцитов, мигрирующих в кровь; окончательные
зрелые их формы в виде тканевых макрофагов локализуются в различных органах и тканях, где они получили специфические названия: гистиоциты соединительной ткани, звездчатые ретикулоциты печени, макрофаги селезенки, макрофаги лимфатических узлов, перитонеальные макрофаги, плевральные макрофаги, клетки микроглии нервной ткани.
5) Т-клеточному. Данный росток дифференцировки на территории костного мозга проходит только самый начальный этап развития: формирование предшественника Т-клеток (пре-Т-клеток) от лимфоидной стволовой клетки; основные события по созреванию различных субпопуляций клоноспецифических Т-клеток разворачиваются в тимусе ;
6) В-клеточному. В отличие от Т-клеточного направления развития В-клеточная дифференцировка характеризуется практически полной завершенностью; в связи с этим не случайно костный мозг относят к центральному органу иммунитета.
Кроме развивающихся B-клеток в постнатальном костном мозге присутствуют зрелые плазматические и T-клетки. Следовательно, у человека костный мозг функционирует и как важный вторичный лимфоидный орган.
Большинство антиген-презентирующих клеток также образуется в костном мозге, хотя их гемопоэтический предшественник остается неизвестным.
Мы будем анализировать пять типов гомопоэтических предшественников
1. BFU-E, erythroid burst-forming unit (early erythroid colonies);
2. CFU-GM, granulocytic-macrophagic colony-forming unit,
3. CFU-E, erythroid burst-forming unit (late erythroid colonies)
4. CFU-GEMM, granulocytic-erythroid-megacaryocytic-macrophagic colony-forming unit
5. Lymphocytes (T and B-cells)
Слайд 28
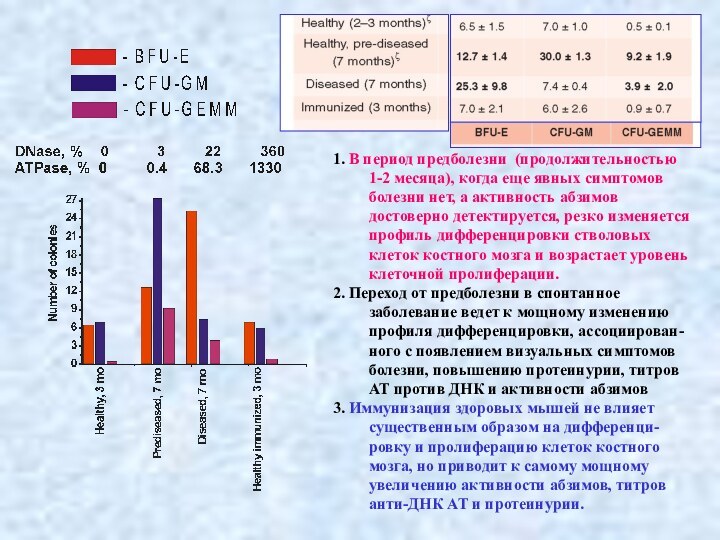
1. В период предболезни (продолжительностью 1-2 месяца), когда
еще явных симптомов болезни нет, а активность абзимов достоверно
детектируется, резко изменяется профиль дифференцировки стволовых клеток костного мозга и возрастает уровень клеточной пролиферации.
2. Переход от предболезни в спонтанное заболевание ведет к мощному изменению профиля дифференцировки, ассоциирован-ного с появлением визуальных симптомов болезни, повышению протеинурии, титров АТ против ДНК и активности абзимов
3. Иммунизация здоровых мышей не влияет существенным образом на дифференци-ровку и пролиферацию клеток костного мозга, но приводит к самому мощному увеличению активности абзимов, титров анти-ДНК АТ и протеинурии.
Слайд 29
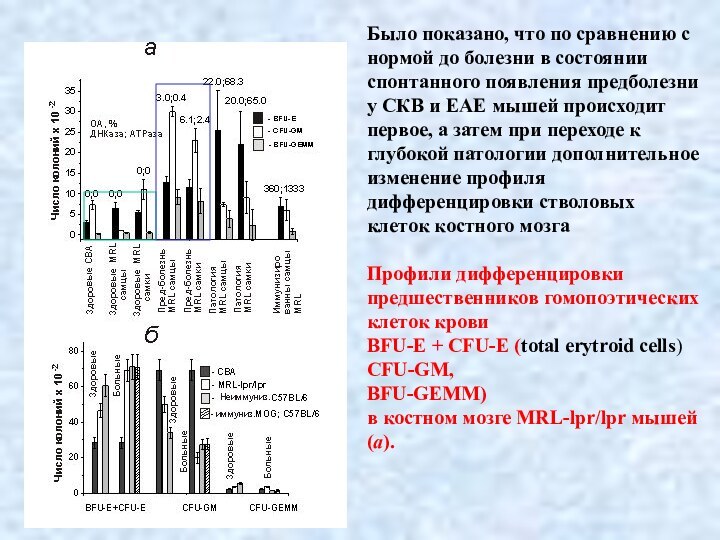
Было показано, что по сравнению с нормой до
болезни в состоянии спонтанного появления предболезни у СКВ и
ЕАЕ мышей происходит первое, а затем при переходе к глубокой патологии дополнительное изменение профиля дифференцировки стволовых
клеток костного мозга
Профили дифференцировки предшественников гомопоэтических клеток крови
BFU-E + CFU-E (total erytroid cells)
CFU-GM,
BFU-GEMM)
в костном мозге MRL-lpr/lpr мышей (а).
Слайд 30
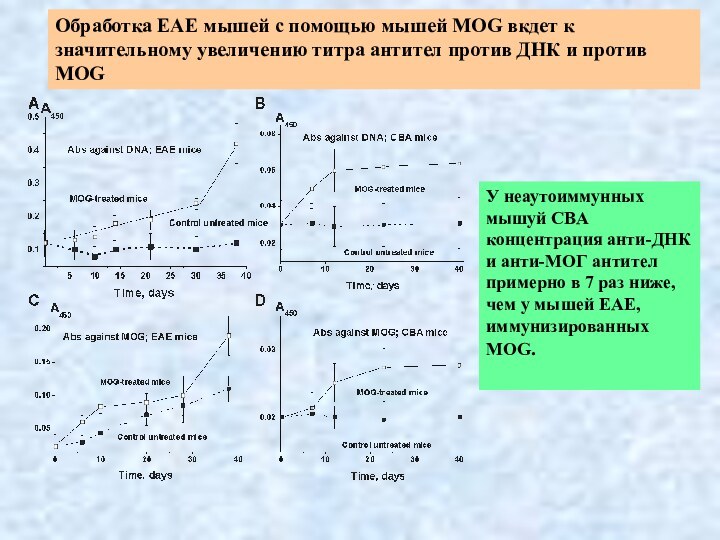
Обработка EAE мышей с помощью мышей MOG вкдет
к значительному увеличению титра антител против ДНК и против
MOG
У неаутоиммунных мышуй CBA концентрация анти-ДНК и анти-МОГ антител примерно в 7 раз ниже, чем у мышей EAE, иммунизированных MOG.
Слайд 31
После иммунизации ЕАЕ мышей с помощью MOG происходит
резкая активация болезни по сравнению с контролем
ГИДРОЛИЗ ДНК
ГИДРОЛИЗ MOG
ГИДРОЛИЗ Основного
белка миелина
Слайд 32
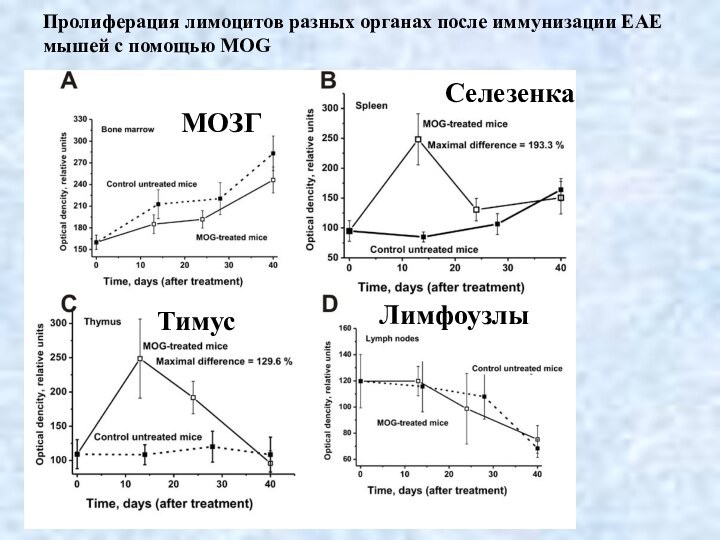
Пролиферация лимоцитов разных органах после иммунизации ЕАЕ мышей
с помощью MOG
МОЗГ
Селезенка
Тимус
Лимфоузлы
Слайд 33
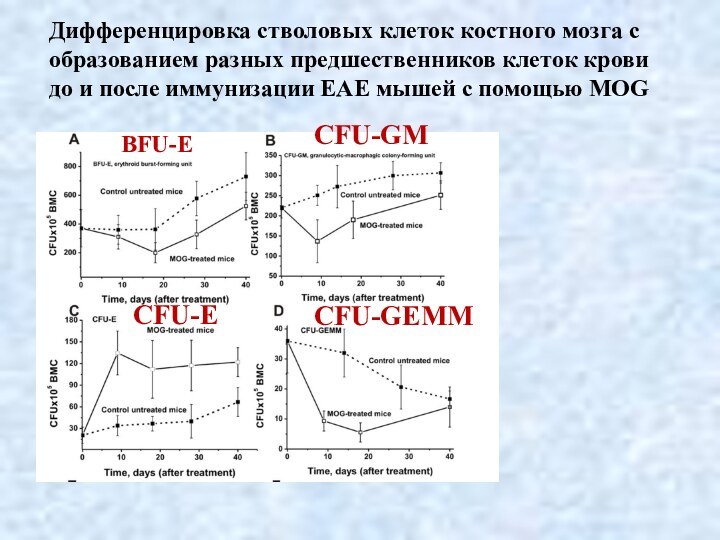
Дифференцировка стволовых клеток костного мозга с образованием разных
предшественников клеток крови до и после иммунизации ЕАЕ мышей
с помощью MOG
BFU-E
CFU-GM
CFU-E
CFU-GEMM
Слайд 34
Дифференцировка стволовых клеток костного мозга с образованием разных
предшественников клеток крови до и после иммунизации SLE ЕАЕ
и неаутоиммунных мышей с помощью ДНК и MOG
ОТНОСИТЕЛЬНОЕ КОЛИЧЕСТВО РАЗНЫХ КЛЕТОК В КОСТНОМ МОЗГЕ
BFU-E
CFU-E
CFU-GM
CFU-GEMM