Слайд 2
Лимфоцит – центральная фигура в иммунной системе
В организме
человека содержится 1013 лимфоцитов (каждая 10 клетка тела –
лимфоцит), общая масса – 1,5 кг
Лимфоциты не «сидят» постоянно в лимфоидных органах, а интенсивно циркулируют по организму между лимфоидными и нелимфоидными органами через лимфатические сосуды и кровь (рециркуляция).
Через один лимфатический сосуд в течение одного часа проходит 108 лимфоцитов.
Миграция лимфоцитов из крови в ткань и наоборот происходит через стенку сосудов, за счет специфического взаимодействия определенных молекул на мембране лимфоцита с определенными молекулами на мембране клеток эндотелия стенки сосудов (интегрины, адгезины, хоминг-рецепторы) и строго регулируется рядом факторов.
Этот процесс получил название homing-эффект лимфоцитов
Слайд 3
В развитии специфического иммунного ответа принимают участие три
основных клеточных типа:
В‑лимфоциты,
Т‑лимфоциты
антигенпрезентирующие клетки – АПК
(макрофаги, дендритные клетки).
Слайд 4
Т- и В-лимфоциты – истинные иммунокомпетентные клетки, способные:
Распознавать
АГ с помощью антигенспецифических рецепторов (TCR, BCR)
Развивать антигенспецифические иммунные
реакции, направленные на элиминацию АГ
Создавать клоны себе подобных клеток после антигенной стимуляции
Формировать иммунологическую память
Развивать иммунологическую толерантность
Другие клетки иммунной системы не способны реализовать полный набор свойств иммунокомпетентных клеток, им могут быть присущи отдельные свойства из перечисленных
Слайд 6
В развитии В- и Т-лимфоцитов выделяют 2 периода:
антиген-зависимый (иммунопоэз)
антигеннезависимый (лимфопоэз)
Лимфопоэз - образование (из стволовой кроветворной клетки),
созревание и дифференцировка иммунокомпетентных клеток – происходит в центральных органах иммунной системы:
в тимусе формируются Т‑лимфоциты, а в красном костном мозге – В‑лимфоциты
Слайд 8
В-лимфоциты – отвечают за гуморальный иммунный ответ
Зрелые
В-лимфоциты составляют 60-70% всех В-клеток крови. Срок жизни зрелых
В-клеток меньше, чем Т-лимфоцитов (несколько суток)
Наличие на их поверхности рецепторов для распознавания антигенов - молекулы иммуноглобулинов.
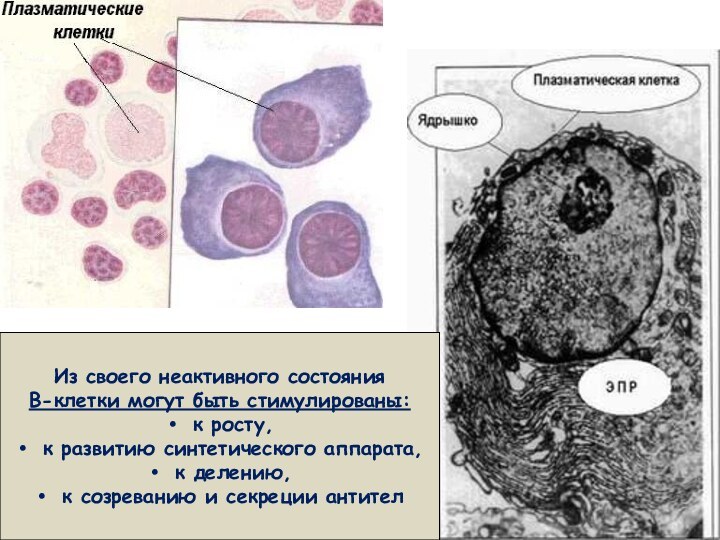
После взаимодействия с антигеном В-лимфоциты дифференцируются в плазматические клетки, секретирующие иммуноглобулины, а также В-клетки памяти, которые при повторном введении АГ быстро активируются фолликулярными дендритными клетками и обеспечивают гуморальную защиту (20-30% - клетки памяти) – основа вакцинации
Слайд 10
Типы молекул на поверхности В-лимфоцитов
Слайд 11
В-лимфоциты
В1(CD5+)
Врожденная субпопуляция
В-лимфоцитов
В2(CD5-)
Зрелые В-лимфоциты
Локализуются в лимфоидных
скоплениях слизистых
оболочек и
кожи
1.Основная популяция
В-лимфоцитов
2.Необходима кооперация с
Тх
3.Распознают АГ с помощью BCR,
поглощают его, расщепляют и
презентируют в составе МНС-II
Т-х с последующей активацией
и превращением в плазматическую
клетку (АОК)
4.После превращения в АОК
синтезируют Ig всех классов
против бактерий и вирусов
3.Имеют поверхностные
рецепторы в виде IgМ, IgD, IgG
В1а
В1в
В отсутствии АГ дифференци
руются в плазмобласты и синтезируют полиреактивные IgM (естественные АТ)
Отвечают на АГ пролиферацией, дифференцировкой в плазмоциты и интезируют специфические антитела (IgA) на Т-независимые АГ
(слизистые)
Слайд 12
Также известны В-клетки маргинальной зоны:
Занимают промежуточное положение
между В1- и В2-клетками
Располагаются в маргинальной зоне селезенки, у
внутренней стенки синусов ЛУ, в эпителиальных криптах миндалин, под куполом пейеровых бляшек кишечника
Отвечают преимущественно на бактериальные ЛПС и ПС и быстро (3 дня) дифференцируются в плазмоциты
В отличие от В-2 лимфоцитов, они не требуют участия Тх, а от В-1 лимфоцитов – продуцируемый класс антителM, а не IgA)
Крупные клетки с большим объемом цитоплазмы
Слайд 13
Из своего неактивного состояния
В-клетки могут быть стимулированы:
к
росту,
к развитию синтетического аппарата,
к делению,
к созреванию
и секреции антител
Слайд 14
Активация В-клеток также подразумевает "переключение классов Ig“:
первые антителопроизводящие
В-клетки продуцируют IgM;
позднее при первичном ответе, а также
при повторном ответе, преобладают IgG, IgA, а иногда IgE
Синтез высокоаффинных IgG требует обязательного хелперного эффекта с участием Т-клеток.
Продукт Тх-клеток (ИЛ-4), контролирует переключение В-лимфоцитов на продукцию IgE
Возможна активация В-клеток и без участия Т-лимфоцитов. Этим отличаются некоторые молекулы с многократно повторёнными одинаковыми фрагментами, особенно полисахаридные полимеры, например, декстран. ("Т-независимые антигены«).
Слайд 15
Т-лимфоциты – главная популяция в развитии клеточного иммунного
ответа
Развитие Т-лф зависит от тимуса, в котором происходит
их формирование
Наличие на мембране Т-клеток уникального рецептора – TCR, ассоциированного с CD3-рецептором, распознающего АГ-пептид, обеспечивает после связывания с АГ проведение сигнала внутрь клетки
Основная масса Т-лимфоцитов имеет TCR, состоящий из α- и β-цепей (αβ-TCR), но есть подкласс γδ-TCR, которые подобно В-лимфоцитам распознают нативный АГ)
Когда зрелые Т-клетки покидают тимус, они являются либо CD4(+), либо CD8(+)-лимфоцитами.
Основные субпопуляции CD4+ CD8+-лимфоцитов
Т-клетки-хелперы (Ty0, Th1,Th2,Th17)
Регуляторные Т-клетки (Treg,Tr1,Th3)
Цитотоксические Т-клетки (CD8+, ЦТЛ)
Слайд 16
Роль тимуса в Т-клеточной продукции
Тимоциты
(Т-клеточные предшественники из костного
мозга)
ТИМУС
Зрелые (наивные)
Т-лимфоциты
CD4+
CD8+
Слайд 17
Типы молекул на поверхности Т-лимфоцитов
Слайд 18
Стадии антиген-независимой дифференцировки
Т-лимфоцитов
протимоцит
Носители CD2,CD7
Пролиферируют и развиваются
под действием ИЛ-1,2,6,7. Мигрируют из КМ и заселяют Т-зависимую
субкапсулярную кортикальную зону селезенки и обнаруживаются в тимусе
Ранний
тимоцит
Дополнительно экспрессируют CD3 и CD5
Находятся под влиянием ИЛ-2 и ИЛ-4
Промежу-
точный
тимоцит
Дополнительно имеют маркеры CD1, CD4 CD8
CD4+ или
CD8+
тимоцит
Т-хелперы\индукторы, Т-супрессоры\цитотоксические.
Способны к продукции специфических цитокинов
Слайд 19
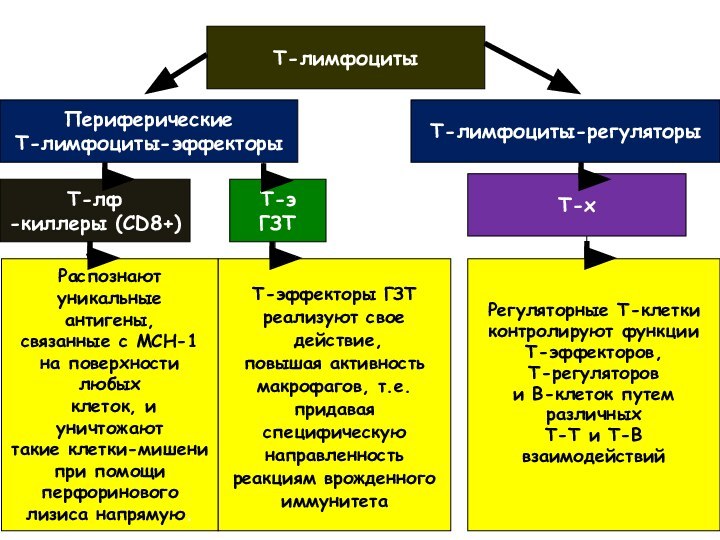
Т-лимфоциты
Периферические
Т-лимфоциты-эффекторы
Т-лимфоциты-регуляторы
Т-лф
-киллеры (CD8+)
Распознают
уникальные антигены,
связанные с МСН-1
на поверхности
любых
клеток, и уничтожают
такие клетки-мишени
при помощи
перфоринового
лизиса напрямую.
Регуляторные Т-клетки
контролируют функции
Т-эффекторов,
Т-регуляторов
и В-клеток путем
различных
Т-Т и Т-В
взаимодействий
Т-х
Т-э
ГЗТ
Т-эффекторы ГЗТ
реализуют свое
действие,
повышая активность
макрофагов, т.е.
придавая
специфическую
направленность
реакциям врожденного
иммунитета
Слайд 20
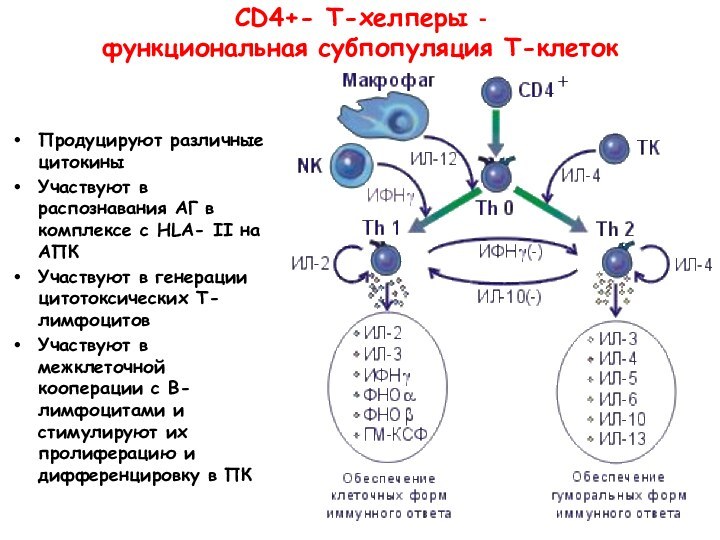
СD4+- Т-хелперы -
функциональная субпопуляция Т-клеток
Продуцируют различные цитокины
Участвуют
в распознавания АГ в комплексе с HLA- II на
АПК
Участвуют в генерации цитотоксических Т-лимфоцитов
Участвуют в межклеточной кооперации с В-лимфоцитами и стимулируют их пролиферацию и дифференцировку в ПК
Слайд 21
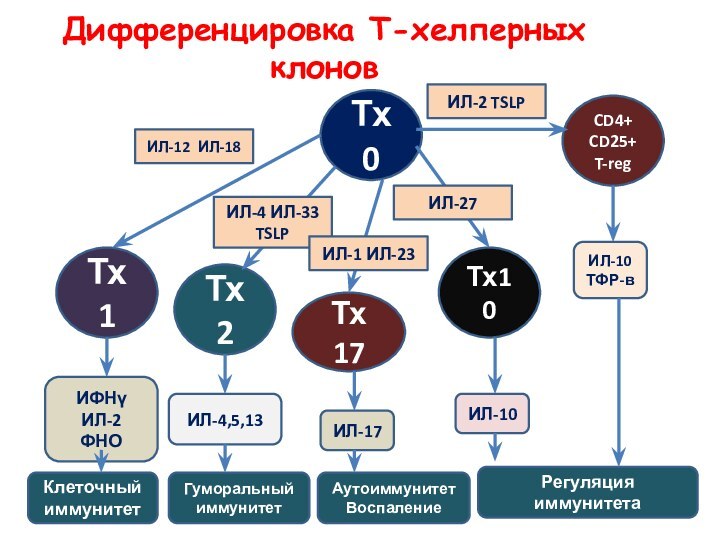
Дифференцировка Т-хелперных клонов
Тх0
Тх1
Тх2
Тх
17
Тх10
CD4+
CD25+
T-reg
ИЛ-12 ИЛ-18
ИЛ-4 ИЛ-33
TSLP
ИЛ-1 ИЛ-23
ИЛ-27
ИЛ-2 TSLP
ИФНγ
ИЛ-2
ФНО
ИЛ-4,5,13
ИЛ-17
ИЛ-10
ИЛ-10
ТФР-в
Клеточный иммунитет
Гуморальный
иммунитет
Аутоиммунитет
Воспаление
Регуляция иммунитета
Слайд 22
Тх1
Тх2
Тх17
CD4+
CD25+
T-reg
МФ
ЭОЗ
НГ
ДК
Защита от внутриклеточных патогенов
Защита от макропаразитов
Защита от внеклеточных
патогенов
Защита от аутоагрессии
Т
ИДС
Аутоиммунные процессы
Аллергии
Клеточные аутоиммунные процессы
Слайд 23
Цитотоксические CD8+-(ЦТЛ, Т-киллеры)
Распознают антигены в комплексе с молекулами
HLA- II и поражают:
инфицированные вирусом клетки-мишени
опухолевые клетки
клетки трансплантата
Накопление
клеточных эффекторов происходит за 5-7 дней (на ранних этапах – на 2-3 день - эту функцию выполняют киллеры врожденного иммунитета – NK-лимфоциты)
Механизм уничтожения распознанной клетки-мишении такой же как и у NK-клеток (с помощью перфоринов и сериновых протеаз, и конечного апоптоза)
Слайд 24
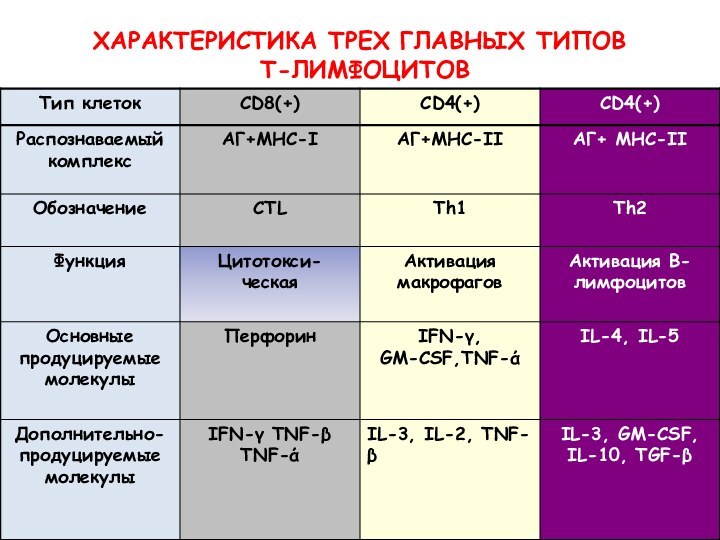
ХАРАКТЕРИСТИКА ТРЕХ ГЛАВНЫХ ТИПОВ
Т-ЛИМФОЦИТОВ
Слайд 25
Регуляторные CD4+CD25+FoxP3+ -
T-лимфоциты (Treg)
Естественные, развивающиеся в тимусе,
вне АГ-стимуляции
(Treg)
Индуцированные на периферии из Тх0 (iTreg)
во
время развития ИО на АГ
Основная функция –
подавление активированных аутоагрессивных клонов CD4+ и CD8+ Т-лимфоцитов и др. клеток,
поддержание толерантности к АГ плода при беременности
ТФРβ, ИЛ-10
супрессия
ТФРβ, ИЛ-10
супрессия
Слайд 26
ЗАБОЛЕВАНИЯ, ПАТОГЕНЕТИЧЕСКИ СВЯЗАННЫЕ
С НАРУШЕНИЕМ ЕСТЕСТВЕННЫХ РЕГУЛЯТОРНЫХ
Т-КЛЕТОК
Содержание
CD4+CD25+Foxp3+ Т-клеток часто понижено
при атопическом дерматите;
при обострении бронхиальной
астмы;
при пищевой аллергии.
Содержание CD4+CD25+Foxp3+ Т-клеток коррелирует
с успешной специфической иммунотерапией;
Слайд 27
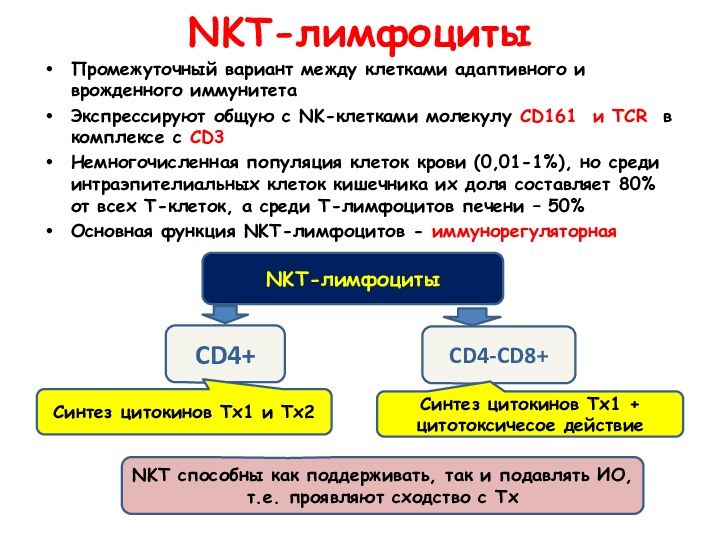
NKT-лимфоциты
Промежуточный вариант между клетками адаптивного и врожденного иммунитета
Экспрессируют
общую с NK-клетками молекулу СD161 и TCR в комплексе
с CD3
Немногочисленная популяция клеток крови (0,01-1%), но среди интраэпителиальных клеток кишечника их доля составляет 80% от всех Т-клеток, а среди Т-лимфоцитов печени – 50%
Основная функция NKT-лимфоцитов - иммунорегуляторная
NKT-лимфоциты
CD4+
CD4-CD8+
Синтез цитокинов Тх1 и Тх2
Синтез цитокинов Тх1 + цитотоксичесое действие
NKT cпособны как поддерживать, так и подавлять ИО, т.е. проявляют сходство с Тх
Слайд 28
ДИФФЕРЕНЦИРОВКА
Т-ХЕЛПЕРОВ
(ВЫБОР ПУТИ
ИММУННОГО ОТВЕТА)
Этот путь
дифференцировки
преобладает
в
слизистой кишечника
Этот путь
дифференцировки
преобладает в
слизистой
дыхательных
путей
IL-5 > IL-4
Слайд 29
Клеточный иммунный ответ
(иммунный ответ по Тх-1 пути)
Участвуют популяции
Тх-1 CD4+ и цитотоксические Т-лимфоциты (CD8+)
Антигенпредставляющие клетки, обычно дендритные,
после процессинга поглощенного АГ представляют ЦТЛ микробные пептиды в комплексе с МНС1
ЦТЛ через ТСR и CD8 распознают микробный пептид и МНС1 (двойное распознавание)
Под действием ИЛ-2 происходит пролиферация ЦТЛ, их активация и уничтожение микробного агента путем выброса из гранул цитотоксических белков (сериновых протеаз) и конечного апоптоза клеток с нарушенной мембраной
Слайд 30
Клеточный
иммунный ответ (Тх1-путь)
Слайд 31
ГУМОРАЛЬНЫЙ ИММУННЫЙ ОТВЕТ (Тх1/Тх2-путь иммунного ответа)
Активация В-лимфоцитов (В2
CD5-) и их дифференцировка в антителообразующие (АОК) плазматические клетки:
Иммуноглобулиновый
рецептор В-лимфоцитов (ВСR) распознает антиген и клетка его поглощает
В-клетка представляет образовавшийся комплекс Тх-2 через ТСR и CD4
Активация покоящихся В-лимфоцитов, их пролиферация с участием цитокинов Тх-2
Популяция (В1 CD5+) находится в лимфоидных образованиях слизистых, кожи и синтезирует преимущественно IgM, участвуя в антибактериальном иммунитете
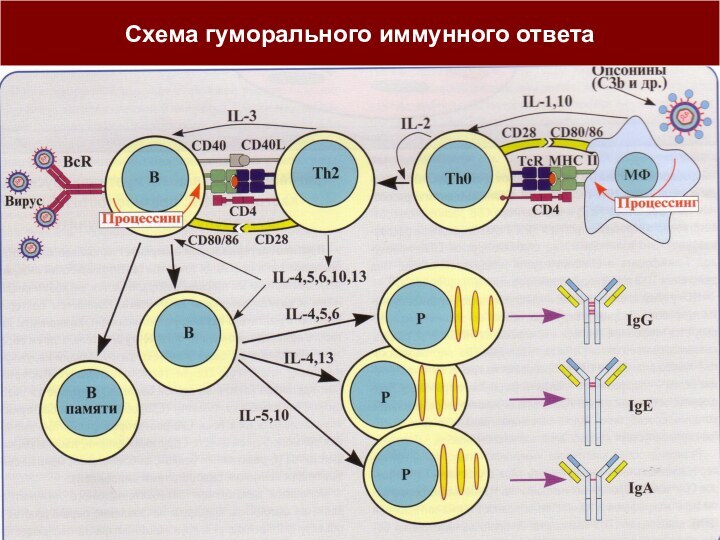
Слайд 32
Схема гуморального иммунного ответа
Слайд 33
Противобактериальный иммунитет (иммунный ответ по Тх2-пути)
Направлен против бактерий
и их токсинов
Бактерии и токсины нейтрализуются антибактериальными и антитоксическими
антителами
Комплексы АГ-АТ активируют комплемент, мембранатакующий комплекс которого разрушает наружную мембрану грамотрицательных бактерий
Пептидогликан клеточной стенки бактерий разрушается лизоцимом
Антитела и комплемент (С3в) обволакивают бактерии для дальнейшего иммунного фагоцитоза
Основной механизм противобактериального иммунитета – фагоцитоз
Противобактериальная защита слизистых оболочек обусловлена секреторным IgA, который препятствует адгезии бактерий на эпителиоцитах
Слайд 34
Антибактериальный иммунный ответ
Слайд 35
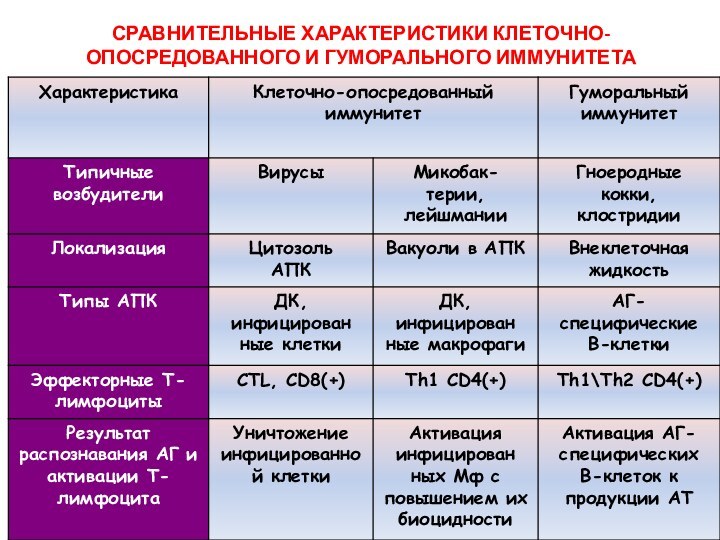
СРАВНИТЕЛЬНЫЕ ХАРАКТЕРИСТИКИ КЛЕТОЧНО-ОПОСРЕДОВАННОГО И ГУМОРАЛЬНОГО ИММУНИТЕТА
Слайд 36
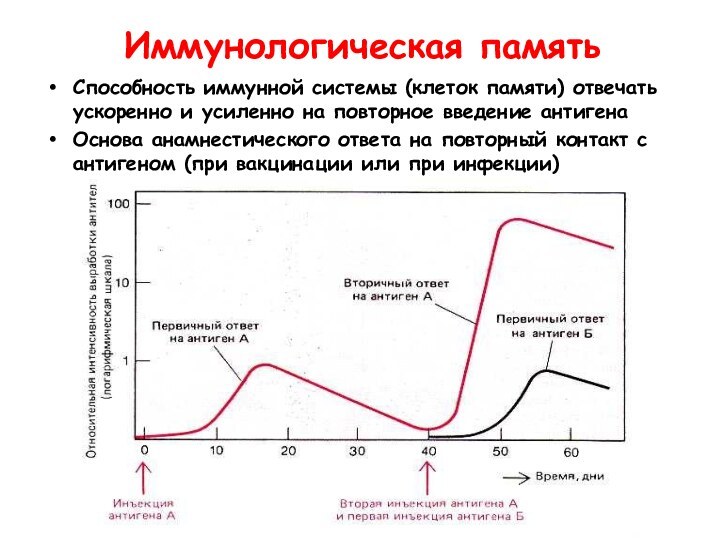
Иммунологическая память
Способность иммунной системы (клеток памяти) отвечать ускоренно
и усиленно на повторное введение антигена
Основа анамнестического ответа на
повторный контакт с антигеном (при вакцинации или при инфекции)
Слайд 37
Т-клетки памяти могут формировать и при отсутствии контакта
с чужеродными АГ:
-
У здорового новорожденного – их до 20%,
- Образуются после лимфопении при регенерации
иммунной системы
- С возрастом их количество растет, а спектр
антигенного распознавания сужается
Т-клетки памяти
Долгоживущие лимфоциты, примированные АГ, но не достигшие стадии дифференцировки в клетку-эффектор
Экспрессируют CD45RO (но не CD45RA!!), CD44, которые поддерживают их длительную рециркуляцию и самоподдержание
При повторном контакте с тем же АГ формируют быстрый и активный ответ за счет аутостимуляции секретируемым ИЛ2
Т-клетки памяти – основная мишень ВИЧ
Слайд 38
Формы клеточной гибели
Апоптоз
Аутофагия
Некроз
Митотическая катастрофа
Ороговение и др.
Классификация по данным
Комитета по номенклатуре клеточной гибели NCCD, основанная на морфологических
проявлениях (2005 г)
Слайд 39
Апоптоз
Запрограммированная смерть клетки - процесс, посредством которого внутренние
или внешние факторы, активируя генетическую программу, приводят к гибели
клетки и ее эффективному удалению из ткани.
Это механизм гибели клеток, который имеет ряд биохимических и морфологических отличий от некроза.
Это биохимически специфический тип гибели клетки, который характеризуется активацией эндогенных эндонуклеаз, которые расщепляют ядерную ДНК на маленькие фрагменты.
Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые тут же фагоцитируются окружающими клетками
Слайд 41
Последовательность ультраструктурных изменений
при апоптозе (справа) и некрозе
(слева)
1 – нормальная клетка;
2 – начало апоптоза;
3 – фрагментация
апоптотической клетки;
4 – фагоцитоз
апоптотических
телец окружающими
клетками;
5 – гибель внутриклеточных
cтруктур при некрозе;
6 – разрушение
клеточной мембраны.
Слайд 42
Апоптоз необходим для элиминации из организма клеток:
пораженных различными
патогенами,
старых клеток, прекращающих выполнять свои функции,
клеток гормонально-зависимых тканей
при снижении концентрации гормонов.
Роль апоптоза в организме
Гибель лимфоцитов при апопотозе – важный механизм регуляции в иммунной системе и средство для поддержания иммунного гомеостаза в организме