Слайд 2
ОПРЕДЕЛЕНИЕ СИНДРОМА ДВС
Неспецифический общепатологический процесс, связанный
с поступлением
в кровоток активаторов свертывания крови и агрегации тромбоцитов,
образованием
в нем тромбина,
активацией и истощением плазменных ферментных систем (свертывающей, калликреин-кининовой, фибринолитической и др.),
образованием в крови множества микросгустков и агрегатов клеток, блокирующих микроциркуляцию в органах,
Все это приводит к развитию тромбогеморрагий, гипоксии, ацидоза, дистрофии и глубокой дисфункции органов, интоксикации организма продуктами белкового распада и к возникновению вторичных профузных кровотечений.
Слайд 3
ДВС является промежуточным механизмом болезней, от выраженности которого
зависят наиболее повреждающие организм эффекты болезней.
ДВС участвует почти всегда:
Сепсис,
септический шок;
Шок различной этиологии;
Синдром гомологичной крови.
В акушерстве:
Преждевременная отслойка плаценты;
Эмболия околоплодными водами;
Тяжелые формы гестозов;
Длительная задержка мертвого плода;
Беременность при ревматизме и нарушении кровообращения;
Заболевания венозной системы.
Слайд 4
ДВС запускают:
Тканевой тромбопластин;
Эндо и экзотоксины бактерий;
Гемолизированные эритроциты;
Протеолитические энзимы;
Комплексы
антиген-антитело;
Гипоксемия и гипоксия;
Жировая эмболия;
Ацидоз;
Длительная стимуляция α-адренорецепторов.
ДВС всегда вторичен
Слайд 5
Для ДВС – синдрома характерен ряд глубоких органных
нарушений, обозначаемых как «СУБСИНДРОМЫ», так как они вторичны.
Поэтому их
нельзя ставить, как это делают многие клиницисты в основу диагноза, обозначая весь процесс как «полиорганную недостаточность».
Слайд 6
Важнейшими из субсиндромов при ДВС являются:
Трансформация асептического ДВС-синдрома
в септический – закономерность, впервые установленная в трудах З.С.Баркагана.
Эта трансформация чаще связана либо с инфицированием мест повреждения тканей, либо с нарушением барьерной функции слизистой оболочки кишечника и массивным проникновением его микрофлоры в кровь.
Тромбоцитопения и тромбоцитопатия потребления.
Слайд 7
Субсиндром легочной(дыхательной) недостаточности;
Субсиндром острой почечной (ОПН) и/или гепаторенальной
недостаточности, требующей подключения к терапии гемодиализа и этапного плазмафереза;
Субсиндромы
поражения и недостаточности др.органов – надпочечников, мозга, сердца;
Субсиндром поражения желудка и кишечника, который включает:
- образование кровоточащих эрозий и язв (шоковые или гипоксические язвы);
- диффузную кровоточивость слизистой оболочки;
- нарушение барьерной функции слизистой оболочки.
Слайд 8
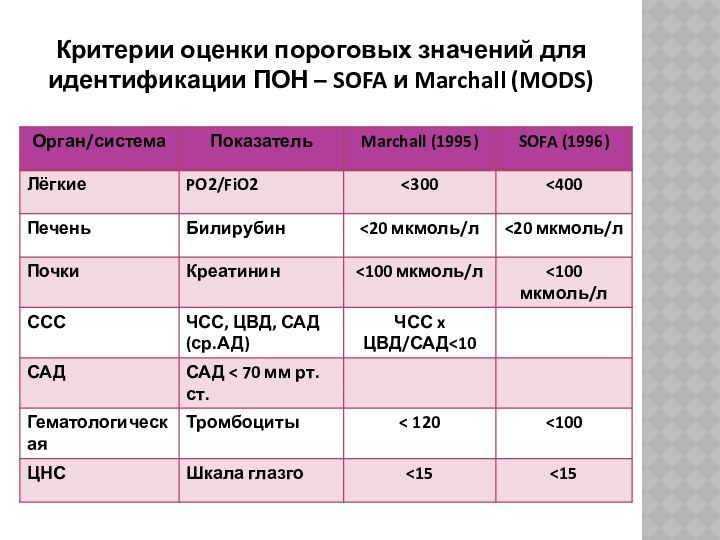
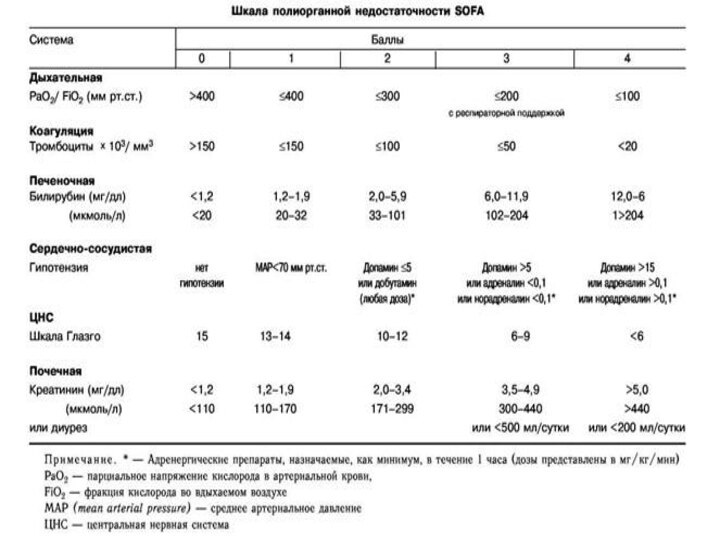
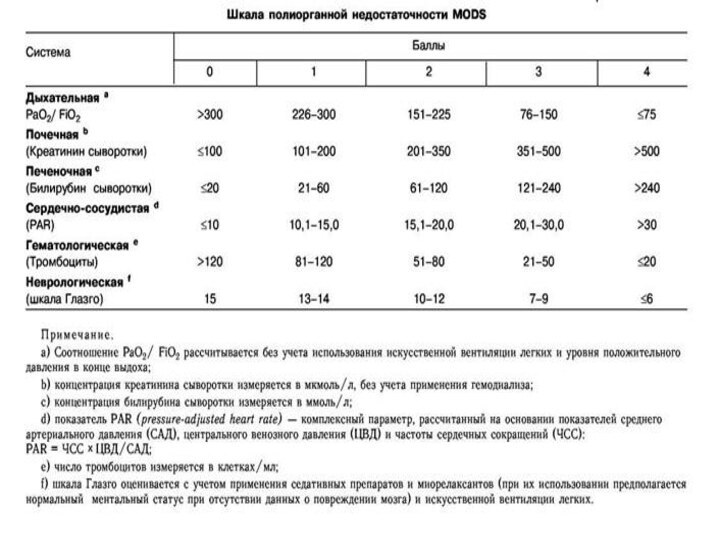
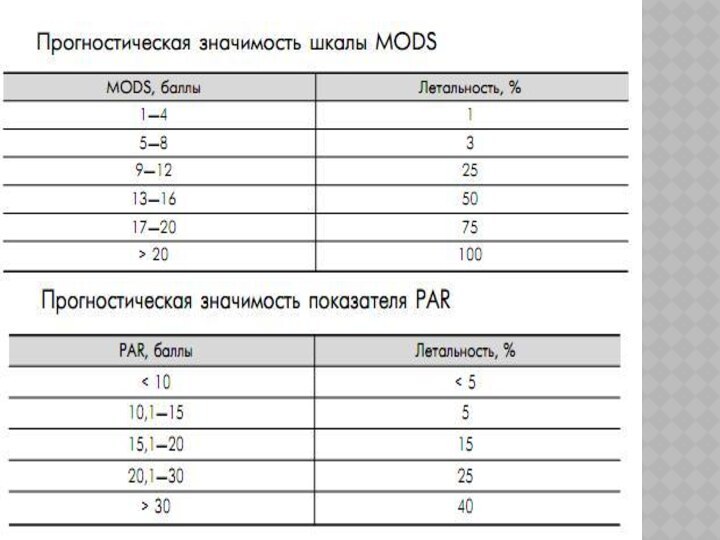
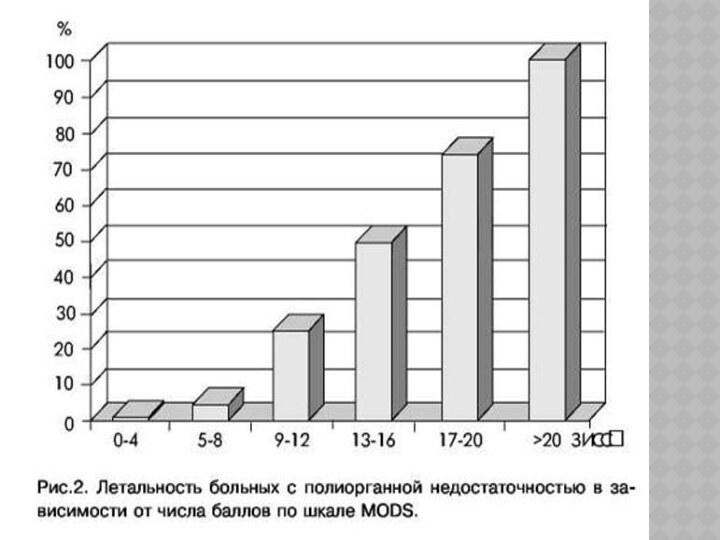
Критерии оценки пороговых значений для идентификации ПОН –
SOFA и Marchall (MODS)
Слайд 13
International Society of Thrombosis and Haemostasis (ISTH) -
Международный комитет по изучению тромбозов и гемостаза.
В 1969 году
на 15-м Ежегодном заседании (ISTH) в Великобритании, ее члены единогласно пришли к утверждению создания Международного общества по изучению тромбозов и гемостаза (ISTH).
Общество выбрало Fritz Koller Швейцарии в качестве ее президента и Sol Шерри США в качестве председателя вновь образованного ISTH. Почти 200 ученых вступили в Общество в этом году, и из них, 37 по-прежнему являются активными членами.
На сегодняшний день в обществе состоит более чем 3600 членов, в более чем 93 странах.
Слайд 14
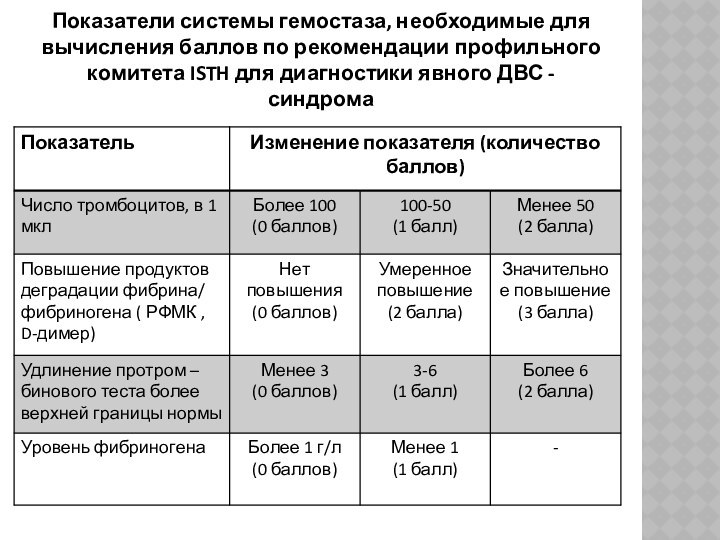
Показатели системы гемостаза, необходимые для вычисления баллов по
рекомендации профильного комитета ISTH для диагностики явного ДВС -
синдрома
Слайд 15
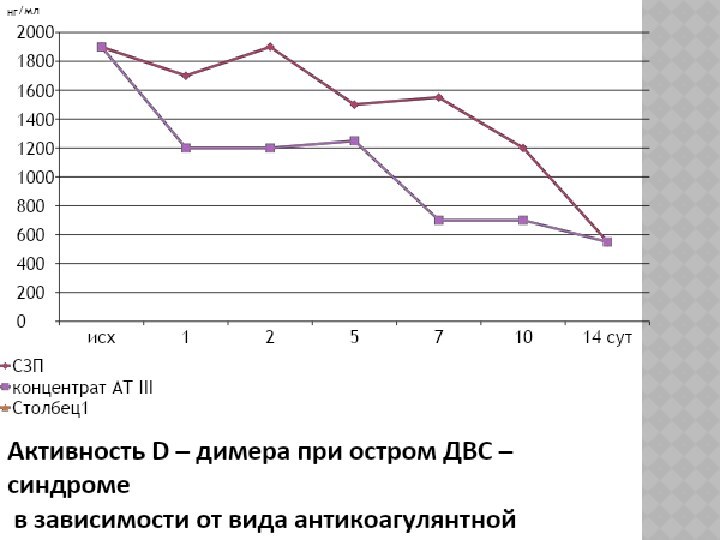
Наиболее высокую чувствительность и специфичность для
количественной оценки интенсивности тромбинемии как ведущего фактора развития полиорганной недостаточности при остром
ДВС-синдроме показали:
уровень РФМК (орто-фенантролиновый тест),
активность D-димера,
Тромбоцитарного фактора 4 (антигепариновый фактор),
антитромбина III,
протеина С.
Эти тесты позволяют целенаправленно проводить интенсивную терапию и своевременно осуществлять ее коррекцию.
Слайд 16
На основе молекулярно-генетического исследования пациентов с низкой фибринолитической активностью в
33,9 % случаев обнаружено гомозиготное носительство аллеля -675 4G/4G гена PAI-1.
При статистическом анализе установлена связь данного вида полиморфизма с наиболее тяжелым течением острого ДВС-синдрома. Высокая частота присутствия гомозиготного носительства аллеля -675 4G/4G гена PAI-1 в этой группе больных, позволяет говорить о возможной генетически детерминированной предрасположенности к тяжелому течению острого
ДВС-синдрома.
«Наследственная тромбофилия и органная недостаточность при остром ДВС-синдроме .»Воробьёва Н.А.Общая реаниматология 2006 г.,II.
Слайд 17
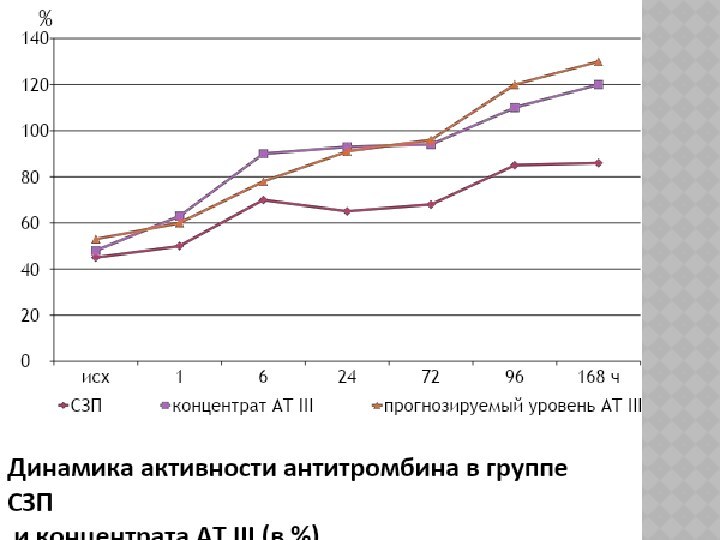
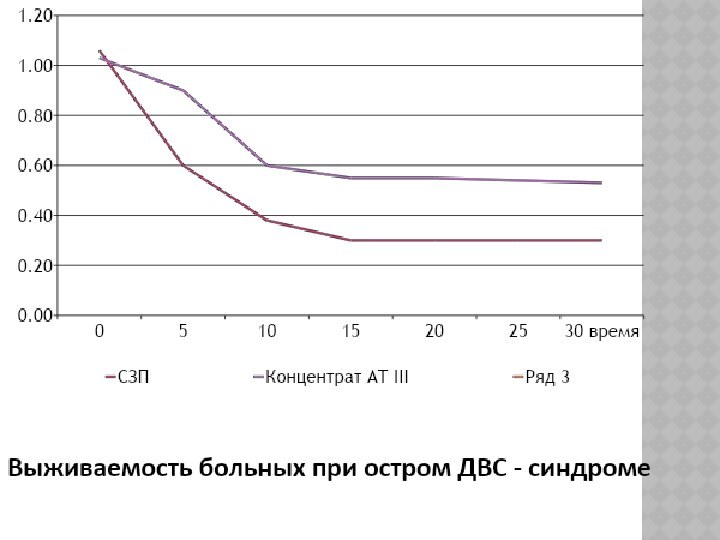
Место концентрата антитромбина III в интенсивной терапии ДВС
–синдрома.
В качестве основного источника антитромбина III в нашей стране
с начала 70-х годов XX века традиционно используется свежезамороженная плазма(Баркаган З.С.,1979, Лычев В.Г. 1979, Thaler E.,1977).
Эффективность трансфузии СЗП малопредсказуема и неконтролируема.
При медленном размораживании плазмы без соблюдения температурного режима разрушается значительное количество АТIII.
Не существует общеиспользуемых формул для расчета необходимого объёма плазмы.
Слайд 18
Низкая функциональная активность АТ III в донорской CЗП
приводит к тому, что для повышения уровня основного антикоагулянта
необходима трансфузия больших объёмов СЗП.
в условиях ДВС – синдрома это не всегда возможно ввиду присутсвия отёка лёгких, мозга, шокового лёгкого, гиперволемии, выраженной ССН, острой почечной недостаточности.
Повторные трансфузии CЗП приводят к сенсибилизации имунной системы, повышает риск аллергических реакций и передачи таких инфекций, как гепатит В,С, ВИЧ – инфекции.
Слайд 19
1 группа – использование донорской CЗП (26 больных).
CЗП вводилась в дозе 10-17 мл/кг (но не более
1000 мл/сут). Вводили струйно или через инфузомат со скоростью 17 мл/мин.
2 группа – использование концентрата антитромбина III. Вводили через инфузомат со скоростью 1000 МЕ/ч в дозе, рассчитанной по формуле, но не более 1500 МЕ в сутки:
доза концентрата АТIII = (100% - активность АТIII в % пациента) X масса пациента (в кг).
Слайд 23
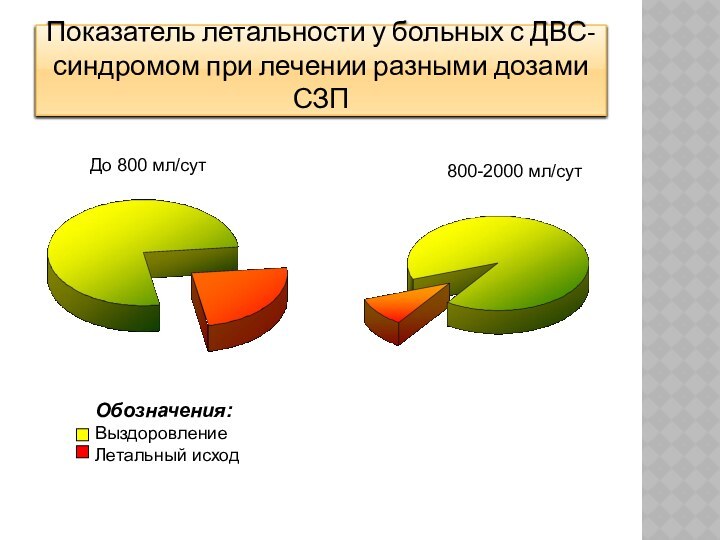
Показатель летальности у больных с ДВС-синдромом при лечении
разными дозами СЗП
До 800 мл/сут
800-2000 мл/сут
Обозначения:
Выздоровление
Летальный исход
Слайд 24
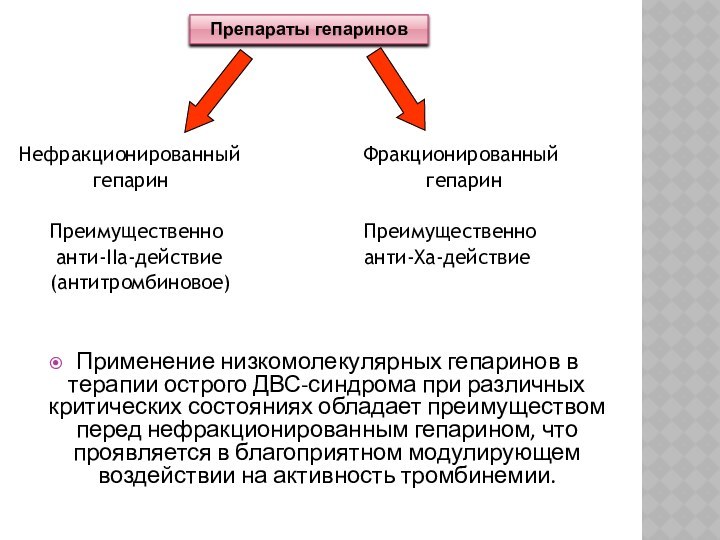
Нефракционированный
Фракционированный
гепарин гепарин
Преимущественно Преимущественно
анти-IIа-действие анти-Xа-действие
(антитромбиновое)
Применение низкомолекулярных гепаринов в терапии острого ДВС-синдрома при различных критических состояниях обладает преимуществом перед нефракционированным гепарином, что проявляется в благоприятном модулирующем воздействии на активность тромбинемии.
Препараты гепаринов
Слайд 25
Выбор фраксипарина в качестве базисного антикоагулянта при остром ДВС-синдроме обусловлен его сохраненным аффинитетом к
фактору IIa.
На основании сравнительного анализа различных режимов дозирования
фраксипарина оптимальным является поддержание анти-Ха-активности плазмы в пределах 0,3-0,4 ME/мл.
Установлено, что эффективной и безопасной дозировкой фраксипарина в терапии острого ДВС-синдрома является доза 80-100 анти-Ха ЕД/кг/сут.
Слайд 26
Терапия ингибиторами фибринолиза (особенно АКК) позволяет уменьшить смертность
от кровотечений, но увеличивает летальность от гемодинамических расстройств, т.к.
они усиливают блокаду микроциркуляции и явления полиорганной недостаточности (З.С. Баркаган, 1988)
Слайд 27
Рекомбинантный VIIа фактор (rFVIIa) (международное название «ЭПТАКОГ АЛЬФА»)
производится фирмой «Novo Nordisk» (Дания) под коммерческим названием NovoSeven® (НовоСэвен®).
Препарат получен с помощью современной ДНК-технологии производства.
Слайд 28
Первое описание успешного лечения некупирующегося
акушерского кровотечения с
применением rFVIIa было
опубликовано F.Moscardo и соавт. в 2001
г. Авторы со-
общили о прекрасном гемостатическом эффекте rFVIIa при
угрожающем жизни МАК после кесарева сечения у женщи-
ны с синдромом диссеминированного внутрисосудистого
свертывания (ДВС), нарушениями функции печени и почеч-
ной недостаточностью.
В дальнейшем G.Breborowicz и соавт, описывая опыт лечения МАК с помощью rFVIIa, сообщили, что применение препарата позволило избежать проведения гистерэктомии в 2 из 6 случаев.
В России первый успешный опыт применения rFVIIa у пациентки с тяжелым послеродовым кровотечением и синдромом массивных гемотрансфузий был получен в 2002 г. в клинике, руководимой проф. З.С.Баркаганом.
Слайд 29
Первый опыт успешного применения рекомбинантного
активированного фактора VII
в терапии терминальной
фазы акушерского ДВС-синдрома.
Больная В.Л., 33 года, поступила в родильное отделение
19.10.2004 г. с 39-недельной беременностью, головным предлежание
для проведения плановых родов.
Настоящая беременнос ть завершилась 05.11.2004 родами крупным плодом (4 119 г, 56 см), которые осложнились острой эмболией околоплодными водами с выраженной
дыхательной недостаточностью и профузным кровотече-
нием из матки несвёртывающейся кровью. Общая
кровопотеря составила около 2,5 литров.
Под прикрытием переливаний свежезамороженной
плазмы (СЗП) и эритромассы была произведена лапаротомия
с перевязкой внутренних подвздошных артерий, а затем — экстирпация матки. Однако кровотечение продолжалось,
и общая кровопотеря составила около 3 литров .
Слайд 30
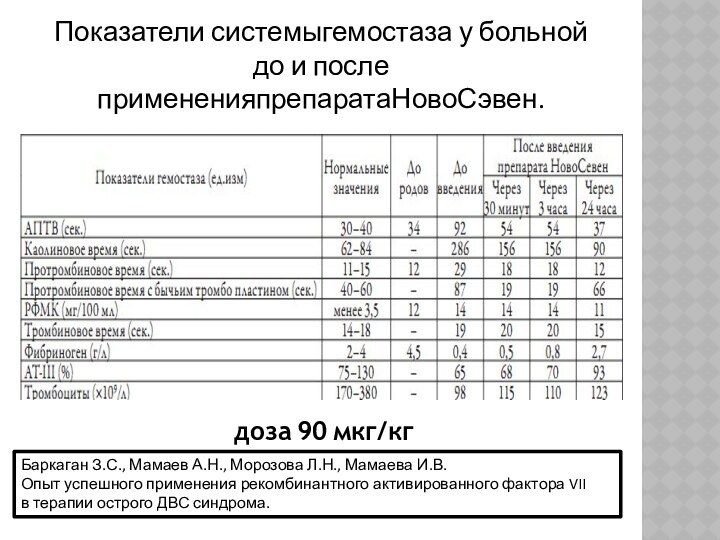
Показатели системыгемостаза у больной до и после примененияпрепаратаНовоСэвен.
доза 90 мкг/кг
Баркаган
З.С., Мамаев А.Н., Морозова Л.Н., Мамаева И.В.
Опыт успешного
применения рекомбинантного активированного фактора VII
в терапии острого ДВС синдрома.
Слайд 31
По данным ВОЗ, массивные акушерские кровотечения входят в
«большую пятерку» причин материнской смертности, составляя в общей структуре
25–30%, что обусловливает постоянный интерес к различным методам их купирования.
Известно, что только 62–65% родов через естественные пути сопровождаются физиологической кровопотерей, 1/3 пациенток теряют от 500 до 1000 мл крови, а в 3–8% слу-
чаев объем кровопотери превышает 1,5% от массы тела роженицы и считается массивным, требующим трансфузии эритроцитной массы и зачастую удаления матки.
Слайд 32
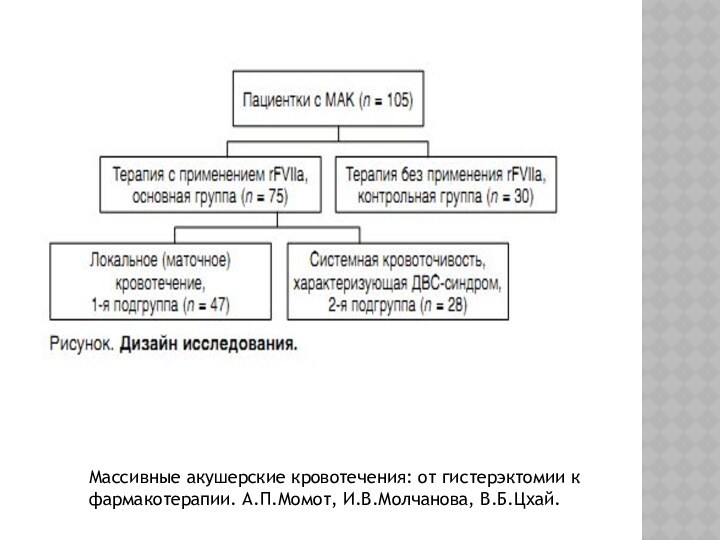
Массивные акушерские кровотечения: от гистерэктомии к фармакотерапии. А.П.Момот,
И.В.Молчанова, В.Б.Цхай.
Слайд 35
Для купирования МАК минимально необходимая доза rFVIIa
должна составлять 50 мкг/кг. Повторное введение rFVIIа может быть
эффективным лишь после исключения ацидоза и гипотермии, а также при соблюдении интервала, не превышающего 2–3 ч от первой инъекции.
В соответствии с использованными в работе критериями эффективности оптимальный гемостатический эффект rFVIIа был получен у женщин с массивным локальным (маточным) кровотечением, у которых применение данного препарата позволило избежать гистерэктомии в 80,8% случаев. В группе пациенток с МАК и синдромом диссеминированного внутрисосудистого свертывания применение rFVIIа было сравнительно менее эффективным. Таким образом, FVIIа является высокоэффективным гемостатическим средством в лечении женщин с МАК, у которых не получен ответ на традиционную гемостатическую тера-
пию, применяемую в акушерской практике.
Слайд 36
Ранее было показано, что применение rFVIIa дает
сравниельно худший гемостатический эффект у больных с тяжелой коагулопатией,
ацидозом и гипотермией. Было установлено, что эффективный гемостаз при применении rFVIIa можно ожидать при следующих показателях:
• протромбиновое время не более чем в 1,5 раза выше нормы;
• концентрация фибриногена более 1 г/л;
• количество тромбоцитов более 50,0 × 109/л;
• pH крови более 7,1;
• отсутствие гипотермии.
Слайд 37
Список литературы
Баркаган З.С., Мамаев А.Н., Морозова Л.И.,
Мамаева И.В. Первый опыт успешного применения рекомбинантного активированного фактора
VII в терапии терминальной фазы акушерского ДВС-синдрома. Тромбоз, гемостаз и реология 2006; 1: 72–3.
З.С. Баркаган, С.А. Ходоренко, А.Н. Мамаев, А.В. Назаров, И.В. Мамаева, Л П. Цывкина, А.В. Россоха. Опыт применения
рекомбинантного фактора VIIа в терапии и профилактике интра- и послеоперационных кровотечений у онкологических больных. Тромбоз, гемостаз и реология 2006; 1.
Массивные акушерские кровотечения: от гистерэктомии к фармакотерапии. А.П.Момот, И.В.Молчанова, В.Б.Цхай. Вопросы гематологии/онкологии и иммунопатологии в педиатрии. 2012г, том11,№2.
Bomken C., Mathai S., Biss T., Loughney A., Hanley J. Recombinant activated factor VII (rFVIIa) in the management of major obstetric haemorrhage: a case series and a proposed guideline for use. Obstet Gynecol Int 2009.