- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Презентація на тему “ Періодична система хімічних елементів
Содержание
- 2. Спроби класифікацій хімічних елементів В хімії існують
- 3. В кінці ХVІІІ ст. А.-Л. Лавуазьє запропонував
- 4. Вчені об'єднали їх в окремі групи. Прості речовини кожної групи отримали такі загальні назви:
- 5. У ХІХ ст. німецький вчений В.
- 6. Він помітив, що в багатьох випадках
- 7. У 1864р. німецький хімік Л.Мейєр запропонував таблицю,
- 8. Періодична система Д.І. Менделеева. Історія відкриття періодичного закону.«Познавая бесконечное, наука сама бесконечна» Д.І.Менделєєв
- 9. Періодичний закон відкритий Д. І. Менделєєвим в
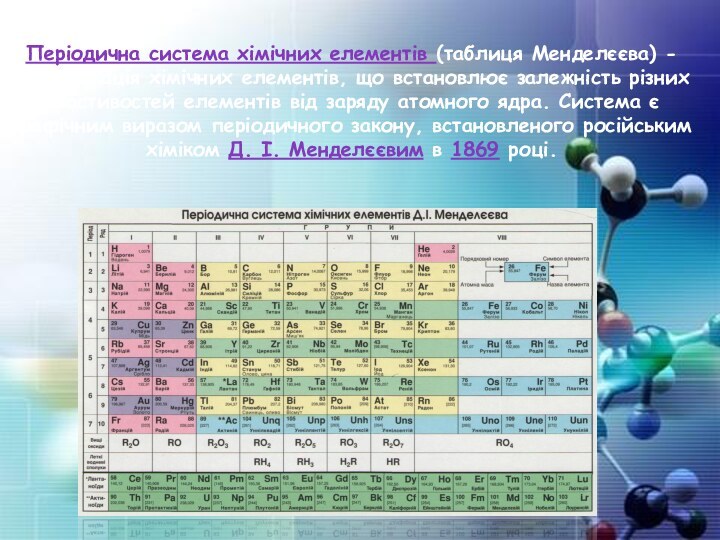
- 10. Періодична система хімічних елементів (таблиця Менделєєва) -
- 11. Періоди — це горизонтальні ряди в таблиці
- 12. Зіставляючи між собою відомі на той час
- 13. При переміщенні вздовж періоду справа ліворуч
- 14. Біографія Д.І.Менделєєва
- 15. Дмитро Іванович Менделєєв народився 8 лютого1834 року
- 16. Був направлений учителем гімназії спочатку в
- 17. Феозва Микитична Лещова,Дружина Менделєєва, 1860-е рокиГанна Іванівна Попова, Друга дружина Менделєєва
- 18. Дочка Д.І.Менделєєва – Ольга Трирогова та його внучка НаталяДочка Менделєєва Люба та її чоловік
- 19. У наступні роки з-під пера Менделєєва вийшло
- 21. Скачать презентацию
- 22. Похожие презентации



















Слайд 2
Спроби класифікацій хімічних елементів
В хімії існують класифікації елементів,
речовин, хімічних реакцій
певними ознакамиСлайд 3 В кінці ХVІІІ ст. А.-Л. Лавуазьє запропонував першу
класифікацію хімічних елементів. Він розділив прості речовини на метали
і неметали. Така класифікація була недосконалою, але розподіл простих речовин, а також хімічних елементів на дві великі групи відіграло важливу роль у розвитку хімії.Слайд 4 Вчені об'єднали їх в окремі групи. Прості речовини кожної
групи отримали такі загальні назви:
Слайд 5 У ХІХ ст. німецький вчений В. Деберейнер розподілив
частину подібних елементів на тріади. 1 тріада - лужні елементи 2
тріада – лужноземельні 4 тріада – галогени. Розмістив їх за збільшенням атомних мас. Закономірність: напівсума елементів приблизно дорівнює відносній атомній масі середнього елемента.Слайд 6 Він помітив, що в багатьох випадках кожний восьмий
елемент є подібним до обраного за перший (таку особливість
має звуковий ряд у музиці). Тому таку закономірність виявлену цим ученим назвали правилом октав.У 1865. англійський вчений
Дж. Ньюлендс розмістив відомі тоді хімічні елементи у ряд за зростанням відносних атомних мас.
H, Li, Be, B, C, N,
O, F, Na, Mg, Al, Si, P, S, Cl, K, Ca, Cr,
Ti, Mn, Fe…
Слайд 7 У 1864р. німецький хімік Л.Мейєр запропонував таблицю, в
якій розмістив елементи за зростанням відносних атомних мас і
відповідно до їх валентності. Однак деякі данні були помилковими або взагалі невідомими.
Слайд 8
Періодична система Д.І. Менделеева.
Історія відкриття періодичного закону.
«Познавая бесконечное,
наука сама бесконечна»
Д.І.Менделєєв
Слайд 9 Періодичний закон відкритий Д. І. Менделєєвим в березні
1869 року при зіставленні властивостей всіх відомих на той
час елементів і величин їхніх атомних мас (ваг). Термін «періодичний закон» Д.І.Менделеев вперше вжив у листопаді 1870, а в жовтні 1871 дав остаточне формулювання періодичного закону: «... властивості елементів, а тому і властивості утворених ними простих і складних тіл, стоять у періодичній залежності від їх атомної маси ». Графічним (табличним) зображенням періодичного закону є розроблена Менделєєвим періодична система елементів.Слайд 10 Періодична система хімічних елементів (таблиця Менделєєва) - класифікація
хімічних елементів, що встановлює залежність різних властивостей елементів від
заряду атомного ядра. Система є графічним виразом періодичного закону, встановленого російським хіміком Д. І. Менделєєвим в 1869 році.Слайд 11 Періоди — це горизонтальні ряди в таблиці Менделєєва.
Періоди поділяються на малі, що складаються з одного ряду
(1—3 періоди), і великі, що складаються з двох рядів (4—7 періоди). У періодах добре помітна періодичність зміни властивостей елементів, простих речовин, утворених цими елементами, та їх сполук.У періодах із зростанням порядкового номера елементів їх металічні властивості слабшають, а неметалічні посилюються.Група — це вертикальний стовпчик у таблиці Менделєєва, у якому розміщені подібні за властивостями хімічні елементи.
У короткоперіодному варіанті Періодичної системи кожна група поділяється на підгрупи — головну (або А) і побічну (або Б). До складу головної підгрупи входять елементи великих і малих періодів, а до складу побічних підгруп — тільки великих періодів і лише метали.
У групах у головних підгрупах виявляється подібність елементів (наприклад однакова вища валентність) та їхніх сполук (наприклад загальні формули вищих оксидів і водневих сполук).
У групах із зростанням порядкового номера металічні властивості елементів посилюються, а неметалічні послаблюються.
Слайд 12 Зіставляючи між собою відомі на той час хімічні
елементи, Менделєєв після колосальної роботи відкрив, нарешті, ту чудову
залежність, ту загальну закономірний зв'язок між окремими елементами, в якій вони постають як єдине ціле, де властивості кожного елемента є не чимось відірваним, самостійним , само собою існуючим, а періодично і правильно повторюваним явищем.Періодична система Д. І. Менделєєва стала найважливішою віхою в розвитку атомно-молекулярного вчення.
Завдяки їй склалося сучасне поняття про хімічний елемент, були уточнені уявлення про прості речовини і з'єднаннях.
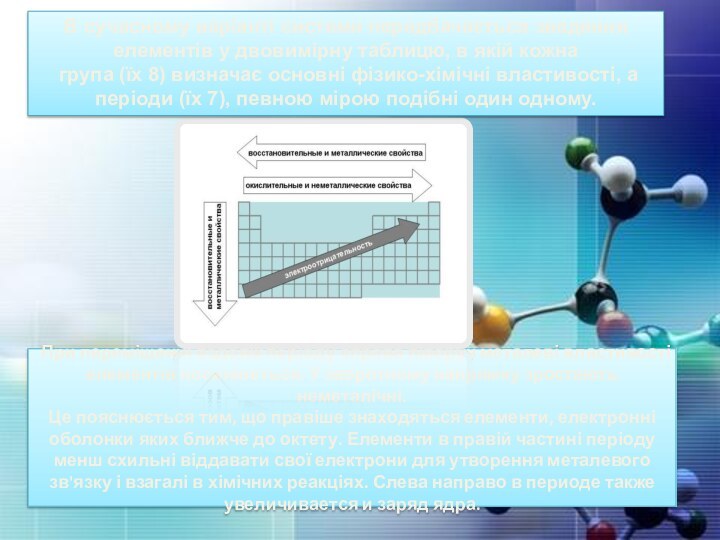
Слайд 13 При переміщенні вздовж періоду справа ліворуч металеві
властивості елементів посилюється. У зворотному напрямку зростають неметалічні. Це пояснюється
тим, що правіше знаходяться елементи, електронні оболонки яких ближче до октету. Елементи в правій частині періоду менш схильні віддавати свої електрони для утворення металевого зв'язку і взагалі в хімічних реакціях. Слева направо в периоде также увеличивается и заряд ядра.В сучасному варіанті системи передбачається зведення елементів у двовимірну таблицю, в якій кожна
група (їх 8) визначає основні фізико-хімічні властивості, а періоди (їх 7), певною мірою подібні один одному.
Слайд 15 Дмитро Іванович Менделєєв народився 8 лютого1834 року у
Тобольську, у родині директора місцевої гімназії. З 1850 р. навчався
на фізико-математичному факультеті Петербурзького педагогічного інституту. У 1855 р. закінчив його з золотою медаллюІван Павлович Менделєєв,
батько вченого
Марія Дмитрівна Менделєєва,
мати вченого
Дмитро Іванович
Менделеев, 1885 год
Тобольська гімназія,
у якій вчився Д.І.Менделєєв
Вид Тобольска
Слайд 16 Був направлений учителем гімназії спочатку в Сімферополь,
а потім в Одесу. У 1856 р. Дмитро Менделєєв відправився
у Петербург і захистив магістерську дисертацію за темою «Про питомі об'єми», після чого на початку 1857 р. був прийнятий приват-доцентом на кафедру хімії Петербурзького університету. 1859 — 1861 р. він перебував у науковому відрядженні у Німеччині, у Гейдельберзькому університеті. У 1860 р. Менделєєв взяв участь у роботі першого міжнародного хімічного конгресу в Карлсрує. У 1861 р. Менделєєв написав перший у Росії підручник з органічної хімії. Навесні 1862 р. підручник був визнаний гідним повної Демидівської премії. У 1863 р. він отримав місце професора у Петербурзькому технологічному інституті, а в 1866 р. — у Петербурзькому університеті, де читав лекції з органічної, неорганічної і технічної хімії. У 1865 р. Менделєєв захистив докторську дисертацію за темою «Про сполуки спирту з водою».перший у Росії підручник
з органічної хімії
Слайд 17
Феозва Микитична Лещова,
Дружина Менделєєва, 1860-е роки
Ганна Іванівна Попова,
Друга дружина
Менделєєва
Слайд 18
Дочка Д.І.Менделєєва – Ольга Трирогова
та його внучка
Наталя
Дочка Менделєєва Люба
та її чоловік
Слайд 19 У наступні роки з-під пера Менделєєва вийшло ще
кілька основних праць з різних розділів хімії. Його повна
наукова і літературна спадщина величезна і містить 431 роботу. Праці Менделєєва отримали широке міжнародне визнання. Він був обраний членом багатьох академій наук, іноземних наукових товариств. Тільки Російська академія наук на виборах 1880 р. забалотувала його через внутрішні інтриги. Пішовши в 1890 у відставку, Менделєєв брав активну участь у виданні Енциклопедичного словника Брокгауза й Ефрона, був консультантом у пороховій лабораторії при Морському міністерстві. Провівши необхідні дослідження, усього за три роки він розробив ефективний склад бездимного пороху. У 1893 р. Менделєєв був призначений хранителем (керівником) Головної палати мір і ваги. Помер у лютому 1907 р. в Санкт-Петербургу від запалення легень.Могила Д.І.Менделєєва
на Волковому кладовищи
Пам'ятник Д.І.Менделєєву





























