Слайд 2
Дубильные вещества – это группа сложных органических соединений,
являющихся производными многоатомных фенолов, имеющих разнообразную химическую структуру, начиная
от простейших производных полифенолов и кончая более сложными высокомолекулярными их производными, так называемыми флобафенами.
Дубильные вещества имеют весьма разнообразное строение, но в основе их лежат вещества полифенольной природы, генетически связанные между собой.
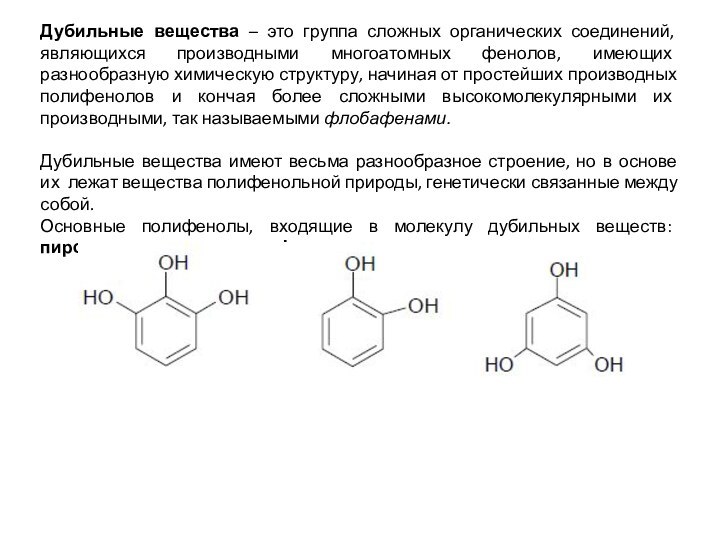
Основные полифенолы, входящие в молекулу дубильных веществ: пирогаллол, пирокатехин, флороглюцин:
Слайд 3
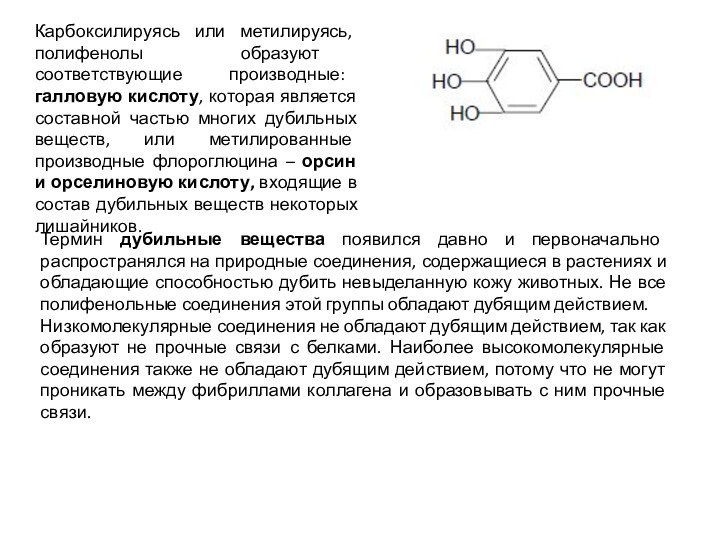
Карбоксилируясь или метилируясь, полифенолы образуют соответствующие производные: галловую
кислоту, которая является составной частью многих дубильных веществ, или
метилированные производные флороглюцина – орсин и орселиновую кислоту, входящие в состав дубильных веществ некоторых лишайников.
Термин дубильные вещества появился давно и первоначально распространялся на природные соединения, содержащиеся в растениях и обладающие способностью дубить невыделанную кожу животных. Не все полифенольные соединения этой группы обладают дубящим действием.
Низкомолекулярные соединения не обладают дубящим действием, так как образуют не прочные связи с белками. Наиболее высокомолекулярные соединения также не обладают дубящим действием, потому что не могут проникать между фибриллами коллагена и образовывать с ним прочные связи.
Слайд 4
Классификация
По классификации Г. Проктера (1894) дубильные вещества в
зависимости от природы продуктов их разложения при 180-200ºC
(без доступа
воздуха) разделяются на две основные группы:
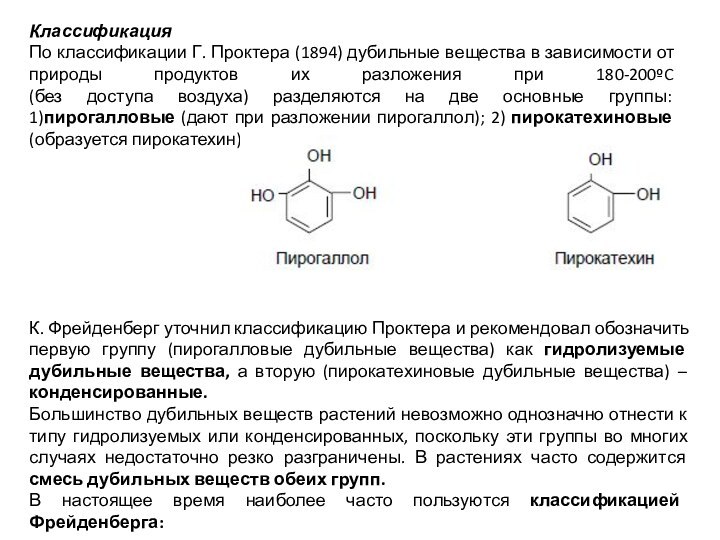
1)пирогалловые (дают при разложении пирогаллол); 2) пирокатехиновые (образуется пирокатехин):
К. Фрейденберг уточнил классификацию Проктера и рекомендовал обозначить первую группу (пирогалловые дубильные вещества) как гидролизуемые дубильные вещества, а вторую (пирокатехиновые дубильные вещества) – конденсированные.
Большинство дубильных веществ растений невозможно однозначно отнести к типу гидролизуемых или конденсированных, поскольку эти группы во многих случаях недостаточно резко разграничены. В растениях часто содержится смесь дубильных веществ обеих групп.
В настоящее время наиболее часто пользуются классификацией Фрейденберга:
Слайд 5
а) галлотанины – эфиры галловой кислоты и сахаров;
галлотаннины – наиболее важные в группе гидролизуемых дубильных веществ.
Встречаются моно-, ди-, три-, тетра-, пента- и полигаллоильные эфиры.
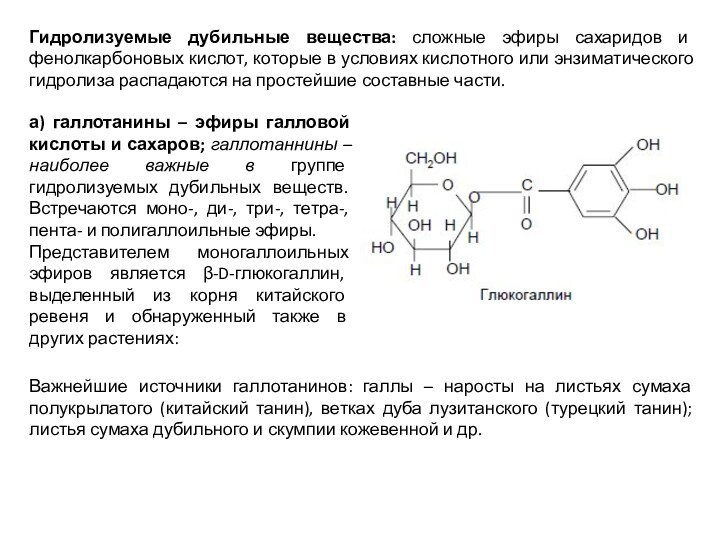
Представителем моногаллоильных эфиров является β-D-глюкогаллин, выделенный из корня китайского ревеня и обнаруженный также в других растениях:
Важнейшие источники галлотанинов: галлы – наросты на листьях сумаха полукрылатого (китайский танин), ветках дуба лузитанского (турецкий танин); листья сумаха дубильного и скумпии кожевенной и др.
Гидролизуемые дубильные вещества: сложные эфиры сахаридов и фенолкарбоновых кислот, которые в условиях кислотного или энзиматического гидролиза распадаются на простейшие составные части.
Слайд 6
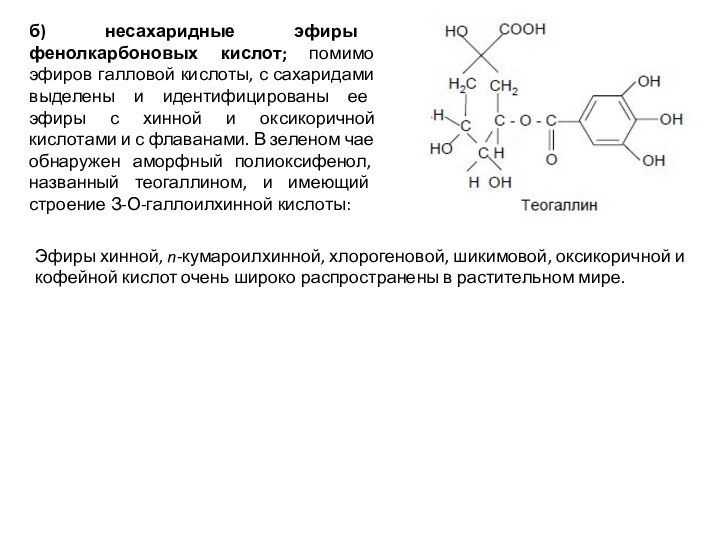
б) несахаридные эфиры фенолкарбоновых кислот; помимо эфиров галловой
кислоты, с сахаридами выделены и идентифицированы ее эфиры с
хинной и оксикоричной кислотами и с флаванами. В зеленом чае обнаружен аморфный полиоксифенол, названный теогаллином, и имеющий строение З-О-галлоилхинной кислоты:
Эфиры хинной, n-кумароилхинной, хлорогеновой, шикимовой, оксикоричной и кофейной кислот очень широко распространены в растительном мире.
Слайд 7
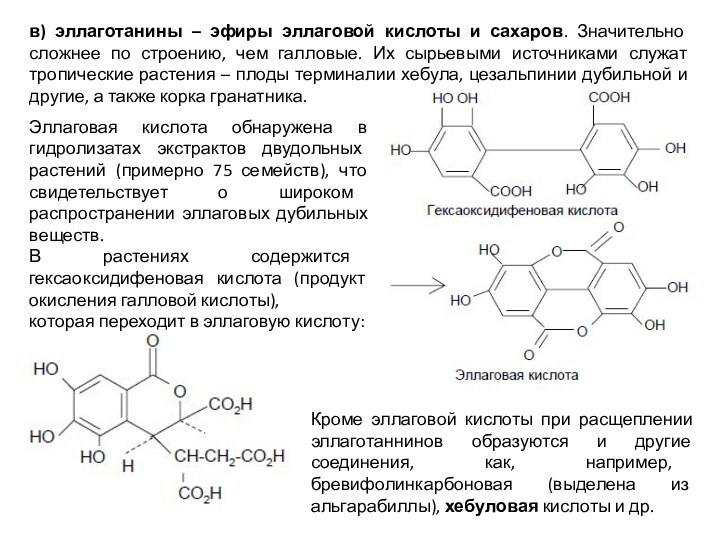
в) эллаготанины – эфиры эллаговой кислоты и сахаров.
Значительно сложнее по строению, чем галловые. Их сырьевыми источниками
служат тропические растения – плоды терминалии хебула, цезальпинии дубильной и другие, а также корка гранатника.
Эллаговая кислота обнаружена в гидролизатах экстрактов двудольных растений (примерно 75 семейств), что свидетельствует о широком распространении эллаговых дубильных веществ.
В растениях содержится гексаоксидифеновая кислота (продукт окисления галловой кислоты),
которая переходит в эллаговую кислоту:
Кроме эллаговой кислоты при расщеплении эллаготаннинов образуются и другие соединения, как, например, бревифолинкарбоновая (выделена из альгарабиллы), хебуловая кислоты и др.
Слайд 8
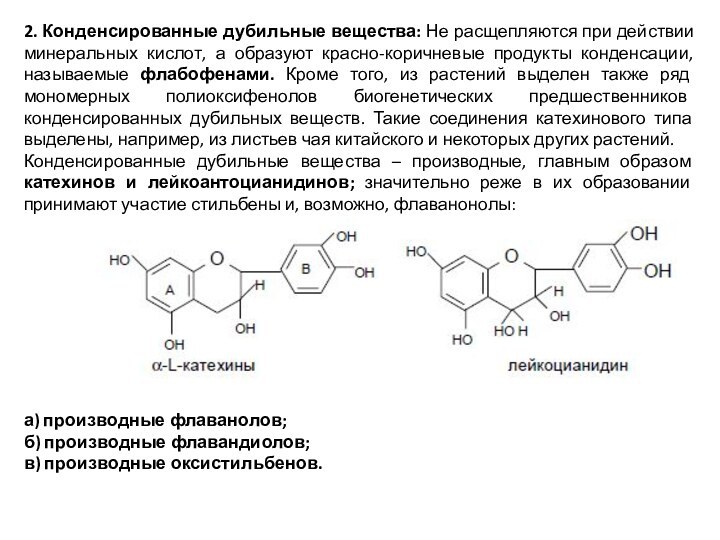
2. Конденсированные дубильные вещества: Не расщепляются при действии
минеральных кислот, а образуют красно-коричневые продукты конденсации, называемые флабофенами.
Кроме того, из растений выделен также ряд мономерных полиоксифенолов биогенетических предшественников конденсированных дубильных веществ. Такие соединения катехинового типа выделены, например, из листьев чая китайского и некоторых других растений.
Конденсированные дубильные вещества – производные, главным образом катехинов и лейкоантоцианидинов; значительно реже в их образовании принимают участие стильбены и, возможно, флаванонолы:
а) производные флаванолов;
б) производные флавандиолов;
в) производные оксистильбенов.
Слайд 9
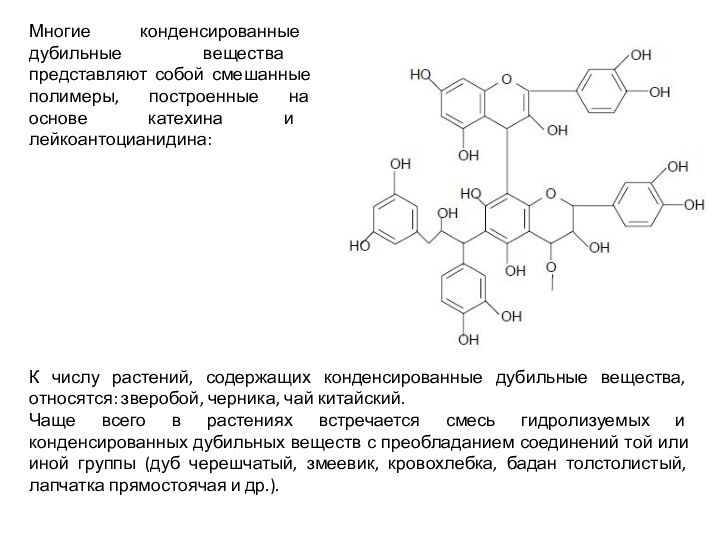
Многие конденсированные дубильные вещества представляют собой смешанные полимеры,
построенные на основе катехина и лейкоантоцианидина:
К числу растений, содержащих
конденсированные дубильные вещества, относятся: зверобой, черника, чай китайский.
Чаще всего в растениях встречается смесь гидролизуемых и конденсированных дубильных веществ с преобладанием соединений той или иной группы (дуб черешчатый, змеевик, кровохлебка, бадан толстолистый, лапчатка прямостоячая и др.).
Слайд 10
Физико-химические свойства
Дубильные вещества (таниды) имеют среднюю молекулярную массу

порядка 1000-5000 (до 20 000) и представляют собой, как
правило, аморфные соединения, образующие при растворении в воде коллоидные растворы. Из органических растворителей таниды растворимы в ацетоне, этиловом спирте, смеси этилового спирта и этилового эфира, отчасти в этиловом эфире, этилацетате, пиридине; нерастворимы в хлороформе, петролейном эфире, бензоле и сероуглероде. Многие дубильные вещества оптически активны; обладают вяжущим вкусом, легко окисляются на воздухе, приобретая более или менее темную окраску.
Катехины – бесцветные кристаллические вещества, хорошо растворимые в воде и органических растворителях (спирты, ацетон и т.д.) Они легко окисляются при нагревании и на свету. Окисление катехинов особенно быстро протекает в щелочной среде, а также при действии окислительных ферментов (полифенолоксидаза, пероксидаза). Молекула катехина содержит два асимметричных атома углерода (С2 и С3), и поэтому каждый из катехинов может быть представлен четырьмя изомерами и двумя рацематами. В зависимости от конфигурации кольца В и гидроксильной группы у С3-атома различают (+) –эпикатехины. В растениях катехины встречаются в изомерных формах, соответствующих (+) – катехину и (-)– эпикатехину.
Для УФ-спектра катехинов характерен основной максимум поглощения в области 270-280 нм.
Слайд 11
Лейкоантоцианиды – бесцветные аморфные вещества, окисляющиеся легче, чем
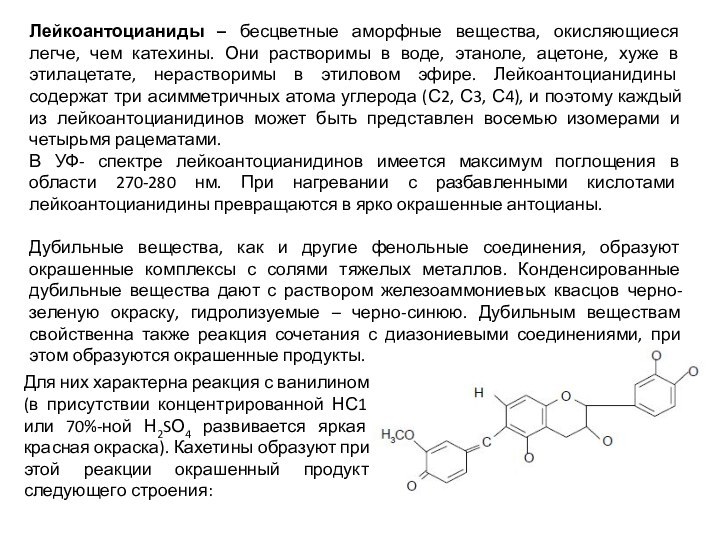
катехины. Они растворимы в воде, этаноле, ацетоне, хуже в
этилацетате, нерастворимы в этиловом эфире. Лейкоантоцианидины содержат три асимметричных атома углерода (С2, С3, С4), и поэтому каждый из лейкоантоцианидинов может быть представлен восемью изомерами и четырьмя рацематами.
В УФ- спектре лейкоантоцианидинов имеется максимум поглощения в области 270-280 нм. При нагревании с разбавленными кислотами лейкоантоцианидины превращаются в ярко окрашенные антоцианы.
Дубильные вещества, как и другие фенольные соединения, образуют окрашенные комплексы с солями тяжелых металлов. Конденсированные дубильные вещества дают с раствором железоаммониевых квасцов черно-зеленую окраску, гидролизуемые – черно-синюю. Дубильным веществам свойственна также реакция сочетания с диазониевыми соединениями, при этом образуются окрашенные продукты.
Для них характерна реакция с ванилином (в присутствии концентрированной НС1 или 70%-ной Н2SО4 развивается яркая красная окраска). Кахетины образуют при этой реакции окрашенный продукт следующего строения:
Слайд 12
Свободная эллаговая кислота дает красно-фиолетовую окраску при добавлении

нескольких кристаллов нитрита натрия и трехчетырех капель уксусной кислоты.
Для обнаружения связанной эллаговой кислоты (или гексаоксидифеновой) уксусную кислоту заменяют 0,1 н. серной или хлористоводородной кислотой (кармино-красная окраска, переходящая в синюю).
Методы выделения и идентификация
Дубильные вещества – это смесь различных полифенолов, имеющих нередко сложную структуру, и очень лабильных, поэтому представляет собой большие трудности.
При выделении из растительного материала получают фракции дубильных веществ. Для этого используют экстракцию растительного материала органическими растворителями: обрабатывают сырье петролейным эфиром, бензолом или смесью бензол – хлороформ (1:1) для удаления основной массы хлорофилла, терпеноидов
и липидов, затем экстрагируют этиловым эфиром, который извлекает некоторые фенольные соединения, в том числе оксикоричные кислоты и катехины; после этого проводят экстракцию этилацетатом, в результате которой в экстракт переходят лейкоантоцианы, димерные проантоцианидины, эфиры оксикоричных кислот и др. В завершение растительный материал экстрагируют метиловым или этиловым спиртом, при этом в раствор переходят многие дубильные вещества и другие фенольные соединения.
Слайд 13
Для получения суммы дубильных веществ используют и другие
способы: растительное сырье вначале экстрагируют горячей водой, а затем
охлажденный водный экстракт обрабатывают последовательно вышеперечисленными растворителями.
Суммарные извлечения дубильных веществ разделяют на индивидуальные компоненты с помощью хроматографических методов.
Для выделения индивидуальных компонентов дубильных веществ (катехинов, лейкоантоцианидинов и др.) используют различные виды хроматографии:
адсорбционную хроматографию на колонках целлюлозы, полиамида (иногда вместо полиамида используют гольевой порошок);
2) ионообменную – на колонках катионита Дауэкс-50 В в Н+- форме;
3) распределительную хроматографию на колонках силикагеля;
4) противоточное распределение;
5) гельфильтрацию на колонках Сефадекса Г-50, Г-100 и др.
Слайд 14
Идентификация индивидуальных компонентов дубильных веществ основана на хроматографических

методах (хроматография на бумаге и тонкослойная), спектральных исследованиях, качественных
реакциях и изучении продуктов расщепления.
Хроматограммы дубильных веществ просматривают в УФ-свете и отмечают характер флуоресценции зон адсорбции. Некоторые производные катехинов имеют слабую голубую флуоресценцию, усиливающуюся после обработки хроматограмм парами аммиака.
Чаще всего для обнаружения катехинов и лейкоантоцианидов и их производных на хроматограммах используют 1%-ный ванилин в концентрированной НС1. Лейкоантоцианиды можно отличить от катехинов при выдерживании хроматограммы в парах соляной кислоты с последующим нагреванием при 105ºC в течение 2 мин, при этом лейкоантоцианиды переходят в антоцианиды (розовый, красно-фиолетовый цвет), а катехины остаются бесцветными или желтеют.
Для более детальной идентификации веществ используют также методы УФ-, ИК- и ПМР- спектроскопии.
Для изучения структуры дубильных веществ широко применяют гидролиз (в частности, ферментативный с помощью танназы), щелочное расщепление с последующим анализом полученных продуктов.
Слайд 15
Качественное определение
Дубильные вещества в растительном сырье определяют качественными

реакциями, которые можно подразделить на две группы: реакции осаждения
и цветные реакции.
Для проведения реакций из сырья получают водное извлечение, к которому добавляют соответствующие реактивы. С растворами желатина, некоторых солей алколоидов и азотистых оснований дубильные вещества дают осадки. С раствором железоаммониевых квасцов гидролизуемые дубильные вещества дают черно-синее окрашивание или осадок, а конденсированные – черно-зеленое окрашивание или осадок.
При кипячении извлечения, содержащего дубильные вещества, со смесью формальдегида и соляной кислоты конденсированные дубильные вещества выпадают в осадок, а гидролизуемые можно обнаружить в фильтрате с помощью железоаммониевых квасцов.
Конденсированные дубильные вещества выпадают в осадок при добавлении бромной воды. Гидролизуемые дубильные вещества осаждают средней солью ацетата свинца в присутствии уксусной кислоты, а конденсированные можно определить в фильтрате по реакции с железоаммониевыми квасцами.
Слайд 16
Для обнаружения дубильных веществ используют также хроматографические методы.
Хроматограммы обрабатывают раствором хлорида железа и ванилиновым реактивом.
В последнее
время широкое распространение при проведении научных исследований получили методы жидкостной хроматографии высокого давления, комбинированные хроматографические методы, особенно при определении индивидуальных веществ.
В нормативной документации на сырье, содержащее дубильные вещества приводится качественная реакция с 1% раствором железоаммониевых квасцов или хлорида окисного железа, которая проводится либо с 10% водным извлечением (отваром) из сырья, либо непосредственно на свежий излом сырья.
Наличие дубильных веществ в растительном сырье можно установить путем непосредственного нанесения на свежий излом (корневище или корень) или на внутреннюю поверхность (кора) раствора железоаммониевых квасцов. В зависимости от природы дубильных веществ появляется черно-синее или черно-зеленое пятно.
Слайд 17
Количественное определение
В литературе описано около 100 различных способов
количественного определения дубильных веществ, которые можно подразделить на следующие
основные группы.
Гравиметрические – основаны на количественном осаждении дубильных веществ желатиной, ионами тяжелых металлов или адсорбцией гольевым порошком.
2. Титрометрические – на окислительных реакциях, прежде всего с применением перманганата калия (метод ГФ ХI).
3. Фотоколориметрические – на реакциях с солями, железа (III) фосфорновольфрамовой кислотой.
4. Методы нефелометрические, хроматоспектрофотометрические в основном используются в научных исследованиях.
Для технических целей используют гравиметрический метод с применением гольевого порошка [весовой единый метод (ВЕМ)].
В ГФ входит титрометрический метод основанный на способности дубильных веществ быстро окисляться перманганатом калия.
Слайд 18
Дубильные вещества широко распространены в растительном мире. Они
обнаружены и у высших, и у низших растений. Особенно
много растений с высоким содержанием дубильных веществ среди двудольных и голосемянных, меньше среди однодольных. У однодольных богаты дубильными веществами древесные растения
– пальмы. Лишайники, грибы, водоросли как правило, содержат небольшие количества дубильных веществ и практического значения не имеют.
Среди многочисленных семейств большим числом растений с высоким содержанием дубильных веществ выделяются такие семейства, как сумаховые, буковые, гречишные, розоцветные, камнеломковые, миртовые, бобовые, вересковые, сосновые и др.
Содержание дубильных веществ в растениях колеблется в широких пределах – от следов до нескольких десятков процентов, а в болезненных наростах растений, так называемых галлах, до 60-80%.
Практическое применение и в медицине, и в промышленности находят только те растения, у которых содержание дубильных веществ 10% и выше.
Слайд 19
Дубильные вещества могут накапливаться в различных органах и

частях растений. У большинства древесных и кустарниковых растений максимальное
количество дубильных веществ накапливается в коре стволов и ветвей (дуб, ива, ель), а так же и в древесине.
У многих травянистых растений большое количество дубильных веществ накапливается в подземных органах: корневище змеевика, лапчатки, бадана, кровохлебки и др.
Несколько меньше содержание дубильных веществ отмечается в листьях, однако известны растения с высоким содержанием (до 20%) дубильных веществ в листьях: скумпия, сумах, чай, бадан, клен приречный и др.
В плодах, семенах, цветках обычно содержатся мало дубильных веществ. Из плодов со значительным содержанием дубильных веществ следует отметить плоды черники, черемухи, соплодия ольхи, плоды щавеля, ревеня и др.
Причем, в незрелых плодах дубильных веществ содержится больше, чем в зрелых. Об этом можно судить по вяжущему вкусу незрелых плодов. Однако уменьшение или исчезновение вяжущего вкуса не всегда происходит за счет снижения общего количества дубильных веществ. У некоторых плодов это происходит за счет
перехода низко- и среднемолекулярных дубильных веществ в высокомолекулярные. Гидролизуемые танины под влиянием ферментов способны превращаться в простейшие соединения (галловая, хебулиновая, эллаговая кислоты и др.).
Слайд 20
В тканях растения дубильные вещества локализуются, главным образом,

в паренхимных клетках. Часто танины присутствуют во всех клетках
данного органа.
В некоторых случаях наибольшее количество их накапливается в клетках возле проводящих пучков. Меньше дубильных веществ обнаруживается в клетках эпидермиса, в пробковой ткани. В механических и проводящих элементах, а также в камбии дубильные вещества, как правило, не содержатся.
Дубильные вещества обычно растворены в клеточном соке. При отмирании клеток дубильные вещества переходят из клеточного сока в оболочку, пропитывая ее.
Для некоторых видов растений характерно накапливание гидролизуемых дубильных веществ: сумах, скумпия, бадан, галлы китайские, турецкие и фисташковые.
В других видах преимущественно накапливаются конденсированные дубильные вещества: чай, зверобой и др.
Но значительно чаще растения содержат дубильные вещества обеих групп с преобладанием той или иной группы. Например, в коре дуба, корневище змеевика, соплодиях ольхи, плодах черемухи, в подземных органах кровохлебки, лапчатки, в коре ивы содержатся дубильные вещества обеих групп.
Роль дубильных веществ, как и других фенольных соединений, в жизнедеятельности растительного организма весьма разнообразна и недостаточно полно изучена в настоящее время. Одной из важнейших функций фенольных соединений является их участие в окислительно-восстановительных процессах, протекающих в растениях. Фенольные соединения выполняют в растениях защитные функции. При механических повреждениях тканей в них начинается интенсивное новообразование фенольных соединений, сопровождающееся окислительной конденсацией, продукты конденсации образуют защитный слой.
Слайд 21
Дубильные вещества, как фенольные производные, обладают бактерицидными и

фунгицидными свойствами и способны защищать растения от возбудителей патогенных
заболеваний.
В целом фенольные соединения и дубильные вещества в их составе играют важную роль в обмене веществ растительной клетки.
Применение танина и растительного сырья, содержащего дубильные вещества в качестве лекарственных средств основано на ряде свойств этих соединений: способности взаимодействовать с белками, солями тяжелых металлов, алкалоидами, на их бактерицидных свойствах.
Лекарственные средства, содержащие дубильные вещества, применяют в качестве вяжущих средств при желудочно-кишечных заболеваниях. Дубильные вещества, образуя на поверхности слизистой кишечника плотную пленку за счет взаимодействия с белками, предохраняют чувствительные окончания нервов от раздражения и тем самым вызывают уменьшение перистальтики кишечника.
За счет образования защитной пленки на раневой поверхности дубильные вещества обладают ранозаживляющим, противовоспалительным и бактерицидным действием и используются при лечении ран, ожогов, язв и т.п. Установлено противоопухолевое действие предшественников дубильных веществ – катехинов и лейкоантоцианидинов.
Слайд 22
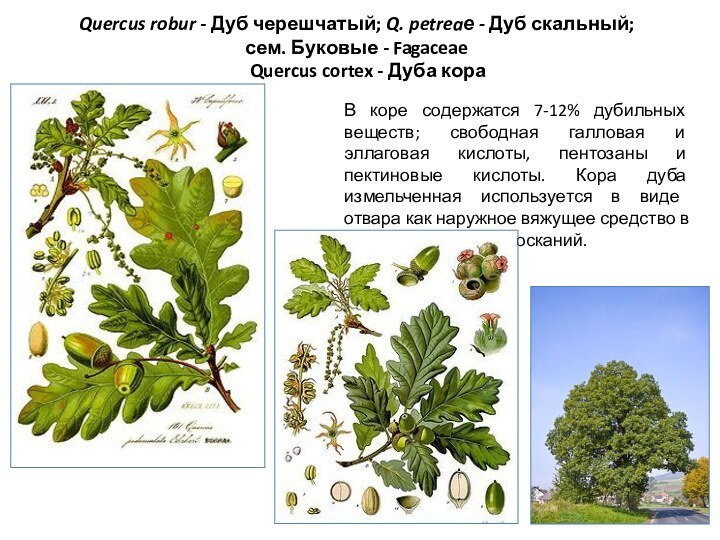
Quercus robur - Дуб черешчатый; Q. petreaе -
Дуб скальный;
сем. Буковые - Fagaceae
Quercus
cortex - Дуба кора
В коре содержатся 7-12% дубильных веществ; свободная галловая и эллаговая кислоты, пентозаны и пектиновые кислоты. Кора дуба измельченная используется в виде отвара как наружное вяжущее средство в виде примочек и полосканий.
Слайд 23
Polygonum bistorta - Горец змеиный, змеевик;
сем. Гречишные
– Polygonaceae
Bistortae rhizomata - Горца змеиного
корневища
Корневище содержит дубильные вещества (до 25%),галловую и эллаговую кислоты и другие соединения.
Измельченное корневище змеевика используется в виде отвара как вяжущее средство.
Слайд 24
Bergenia crassifolia - Бадан толстолистный;
сем. Камнеломковые –
Saxifragaceae
Bergeniae rhizomata - Бадана корневища
Корневища содержат
около 20% дубильных веществ, изокумарин бергенин, сахара, крахмал.
Измельченное корневище бадана используется в виде отвара как вяжущее средство.
Слайд 25
Cotinus coggygria - Скумпия кожевенная;
сем. Сумаховые (Анакардиевые)
- Anacardiaceae
Cotini coggygriae folia
- Скумпии кожевенной листья
В листьях скумпии содержится 15-40% дубильных веществ; галловая кислота; флавоноиды (кверцетин, мирицетан и др.) антоцианы, лейкоантоцианы; эфирное масло (0,15%) и др.
На производстве листья скумпии используются для получения танина и препарата «танальбин», относящихся к вяжущим средствам.
Слайд 26
Rhus coriaria - Сумах дубильный; сем. Сумаховые -
Anacardiaceae.
Rhois coriariae folia - Сумаха
дубильного листья
Листья содержат до 25% дубильных веществ, из них около 15% приходится на танин; галловую кислоту, флавоноиды и другие соединения.
Листья сумаха поступают на производство для получения танина, относящегося к группе вяжущих средств.
Танин (Tanninum, Acidum tannicum).
Фармакологическое действие: вяжущее и местное противовоспалительное средство.
Показания: воспалительные процессы в полости рта, носа, зева, гортани, ожоги, язвы, трещины, пролежни.
Форма выпуска: аморфный порошок для изготовления экстемпоральной рецептуры.
Противопоказания: танин не принимается внутрь, т.к. взаимодействует с белками слизистой оболочки желудка, может вызвать потерю аппетита и расстройство желудка.
Слайд 27
Potentilla erecta (Tormentilla еrecta) - Лапчатка прямостоячая;
сем.
Розоцветные – Rosaceae
Tormentillae rhizomata - Лапчатки
(дикого калгана) корневища
Корневища содержат 15—30% дубильных веществ, эллаговую кислоту, тритерпеновые сапонины, крахмал, смолистые вещества.
Измельченные корневища лапчатки в виде отвара используются как вяжущее средство.
Слайд 28
Sanguisorba officinalis - Кровохлебка лекарственная;
cем. Розоцветные –
Rosaceae
Sanguisorbae rhizomata et radices - Кровохлебки
корневища и корни
В подземных органах содержатся дубильные вещества (12—13%), галловая и эллаговая кислоты, крахмал, сапонины, аскорбиновая кислота, каротиноиды и другие соединения.
Измельченные корневища и корни кровохлебки применяются в виде отвара как вяжущее и кровоостанавливающее средство.
Слайд 29
Alnus incana – Ольха серая; A. glutinosa -
Ольха клейкая;
сем. Березовые – Betulaceae
Alni fructus
- ольхи соплодия
Соплодия содержат дубильные вещества, в состав которых входит до 5% танина и около 4% галловой кислоты.
Измельченные соплодия ольхи применяются в виде отвара как вяжущее средство.
Слайд 30
Vaccinium myrtillus - Черника обыкновенная;
сем. Вересковые –
Ericaceae
Myrtilli fructus - Черники плоды
В
плодах содержатся дубильные вещества (около 12%), антоцианы, органические кислоты, пектиновые вещества, аскорбиновая кислота, каротиноиды и другие соединения. В листьях обнаружены антоцианы, флавоноиды, аскорбиновая кислота, олеаноловая и урсоловая кислоты и другие соединения.
Плоды черники используются как вяжущее средство в виде отвара.
Слайд 31
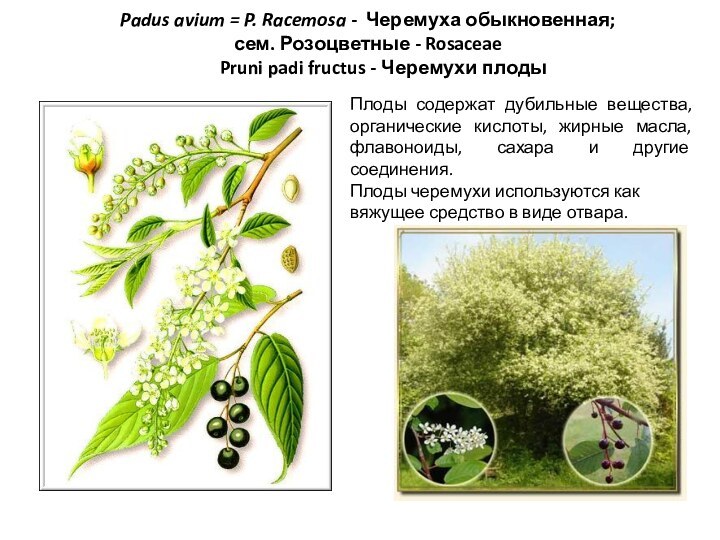
Padus avium = P. Racemosa - Черемуха обыкновенная;
сем. Розоцветные - Rosaceae
Pruni
padi fructus - Черемухи плоды
Плоды содержат дубильные вещества, органические кислоты, жирные масла, флавоноиды, сахара и другие соединения.
Плоды черемухи используются как вяжущее средство в виде отвара.
Слайд 32
Thea sinensis - Чай китайский (чайный куст); сем.
Чайные – Theaceae
Folia Theaea sinensis
- Листья чая китайского
Слайд 33
Листья содержат 9—36 % дубильных веществ, среди них

до 26 % растворимых и до 10 % нерастворимых,
смолы, нуклеопротеиды, содержащие железо и марганец. В состав растворимых дубильных веществ входят галлокатехингаллат, L-эпиатехингаллат, L-эпигаллокатехин, L-галлокатехингаллат и L-эпикатехин, свободная галловая кислота и другие вещества. Так же в листьях найдены алкалоиды — кофеин, теофиллин, теобромин, ксантин, аденин, гипоксантин, параксантин, метилксантин, изатин и другие органические основания. Обнаружены флавоноиды — кемпферол, 3-рамногликозид кемпферола, кверцетин, кверцитрин, изокверцитрин, рутин и др.
В стеблях, корнях и семенах содержатся стероидные сапонины. В семенах 22—25 % жирного масла, 30 % крахмала и стерины — стигмастерин и β, γ-ситостерин, до 8,5 % белка. В листьях имеются также кумарины, витамины — аскорбиновая кислота (более 0,230 %), тиамин, рибофлавин, пиридоксин, филлохинон, никотиновая и пантотеновая кислоты, эфирное масло.
В состав эфирного масла из свежих неферментированных листьев (выход 0,007—0,014 %) входят гексен-З-ол-1 (66 %), метиловый спирт, гексен-2-аль-1, изомасляный и изовалериановый альдегиды, уксусная, пропионовая, масляная, n-капроновая и пальмитиновая кислоты, метиловый эфир салициловой кислоты.
Масло из зелёных ферментированных листьев (выход 0,003—0,006 %) состоит из β, γ-гексенола (25 %), n-гексанола, метилового спирта, n-октилового спирта, гераниола, линалоола, цитранеллола, бензилового, фенилэтилового спирта, вторичных спиртов, бутил-изобутил и изовалерианового альдегидов, гексен-2-аля-1, бензальдегида, ацетофенола, n-оксибензальацетона, крезола, фенола, уксусной, масляной, капроновой, салициловой и фенилуксусной кислот и метилсалицилата.
Слайд 34
Составные части масла из чёрного чая следующие: цитроналлол,

гераниол, линалоол, вторичный терпеновый спирт, бензиловый, фенилэтиловый, бутиловый, изобутиловый,
изоамиловый, гексиловый, октиловый и З-метилбутиловый спирты, альдегиды (капроновый, изовалериановый, бензальдегид), пропионовая, изовалериановая, каприловая и пальмитиновая кислоты, сложные эфиры этих кислот, крезолы, хинолин, метилмеркаптан, метансульфоновая кислота, 2-ацетилпиррол, метил-, диметил-, триметиламины, этиламин, n-пропиламин и др.
Значительная часть листьев и веток чая, срезанных при уходе за плантациями чайного куста (при формовке), а также чайная пыль, образующаяся на чаеразвесочных фабриках, используются в качестве сырья для заводского добывания алкалоидов кофеина и теофиллина.
Кофеин является важным лекарственным средством. Он действует возбуждающе и тонизирующе на центральную нервную систему, улучшает умственную и физическую деятельность, является мочегонным и средством от мигрени.
Теофиллин применяют как средство, улучшающее коронарное кровообращение, как мочегонное при нарушениях кровообращения сердечного и почечного происхождения.
Алкалоиды чая входят в ряд препаратов (эуфиллин, диуретин и др.), применяемых при коронарной недостаточности, гипертонической болезни, бронхиальной астме, стенокардии, отёках сердечного происхождения и др.
Слайд 35
Кроме того, из старых листьев чая и чайной

пыли получают комплекс катехинов с Р-витаминной активностью, используемый при
нарушениях проницаемости и повышенной ломкости сосудов, геморрагических диатезах, кровоизлияниях в сетчатку глаза, при лучевой терапии, гипертонической болезни и др. Благодаря наличию кофеина и дубильных веществ чайный напиток и выделенный алкалоид кофеин используются как противоядие при отравлении ядами, наркотическими веществами и алкоголем.
Наряду с чёрным, так называемым байховым чаем, широко употребляется зелёный чай. Зелёный чай менее ароматичен, но физиологически более активен. В экспериментальных исследованиях установлено, что зелёный чай обладает антимикробными свойствами. Его отвар был предложен для лечения дизентерии. Также он показан при коклюше, энтероколите и диспепсии. В комплексе с другими лекарствами стимулирует кроветворение, повышает упругость и снижает проницаемость стенок кровеносных сосудов, обладает противолучевым действием.
В народной медицине компрессами из крепкого чая снимают боль и жар при солнечных ожогах, воспалении век.
Слайд 36
Hamamelis virginiana - Гамамелис вирджинский;
сем. Гамамелисовые –
Hamamelidaceae
Hamamelidis folia — гамамелиса листья;
Hamamelidis cortex – кора гамамелиса
Листья содержат 7 — 11% дубильных веществ в виде гликозида — гамамелитанина, содержащего отчасти дигаллоилгексозу, а кроме того, свободную галловую кислоту и кверцетин. В свежих листьях содержится немного эфирного масла.
Жидкий экстракт из листьев применяется как кровоостанавливающее при внутренних и геморроидальных кровотечениях, как вяжущее при расстройствах кишечника и наружно как заживляющее раны.
Реже используется кора.
Слайд 37
Quercus infectoria - дуб зараженный; Quercus robur -
дуб черешчатый; сем. Буковые - Fagaceae;
Rhus chinensis -
сумах китайский; Pistscia vera - фисташка
сем. Сумаховые -Anacardiaceae
Gallae - turcicae - галлы турецкие, -chinensis - галлы китайские, -pistaciae - галлы фисташковые = бузгунча
Галлы:
1. на стебле китайской гречихи, вызванные головнёвым грибом Ustilago treubii;
2. на виргинском можжевельнике («кедровые яблоки»), вызванные ржавчинным грибом Gymnosporangium juniperi virginianae;
3. раковые галлы на яблоне, вызванные кровяной тлёй Myzoxylus laniger;
4. мешковидные галлы на листе липы, вызванные клещом Eriophyes tilae; 4а — тот же галл в разрезе;
5. сложные галлы на ели, вызванные тлёй Chaphalodes strobilinus;
6. галлы на дубе, вызванные яблоковидной орехотворкой Diplolepis longiventris (нижний) и Diplolepis quercus folii (два верхних); 6а — тот же галл в разрезе.
Слайд 38
Турецкие галлы содержат 50—60 % (иногда до 80
%) галлотанина, представляющего собой в основном пентадигаллоилглюкозу. К сопровождающим
веществам относятся свободная галловая кислота, сахар, крахмал, смола. Примечание. Приведена формула пентадигаллоилглюкозы, полученной путем синтеза. Промышленное сырье для производства танина, его препаратов; поступает по импорту.
Китайские галлы ("чернильные орешки") содержат 50—80 % галлотанина. Основным компонентом китайского галлотанина является глюкоза, которая этерифицирована 2 молекулами галловой, 1 молекулой дигалловой и 1 молекулой тригалловой кислот. К сопровождающим веществам относятся свободная галловая кислота, крахмал (до 8 %), сахар, смола. Промышленное сырье для получения танина и его препаратов; поступает по импорту.
Слайд 39
Acacia catechu - акация катеху; сем. Бобовые –
Fabaceae
Catechu - катеху
Растет в Индии.
Издавна население приготовляет экстракт (Катеху), вываривая измельченную древесину с водой; процеженный отвар выпаривают до густоты, раскладывают на листья и высушивают на солнце. Поступает в продажу в виде неравномерных кусков темно-бурого цвета, сильно вяжущего и горьковатого вкуса. Катеху должен полностью растворяться в воде и спирте. С железо-аммониевыми квасцами дает черно-зеленый осадок.
Дубильные вещества относятся к группе пирокатехина. Раствор применяют как вяжущее внутрь, для полоскания и как наружное для примочек.
Малайское население изготовляет из катеху массу для жевания — бетель.