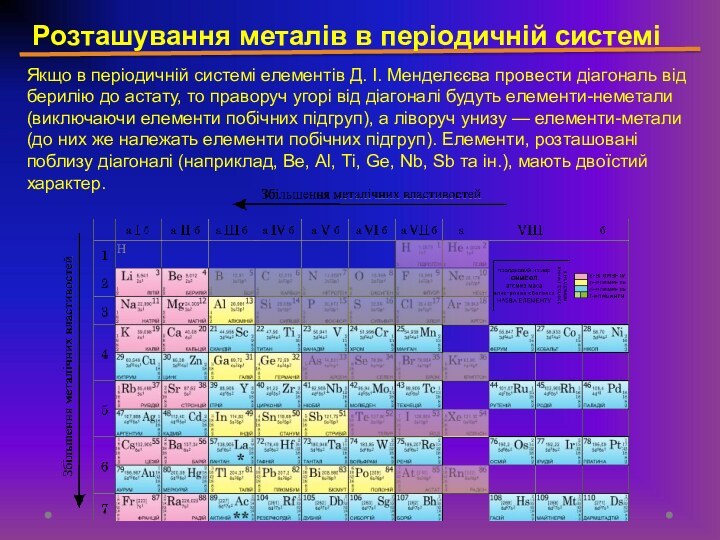
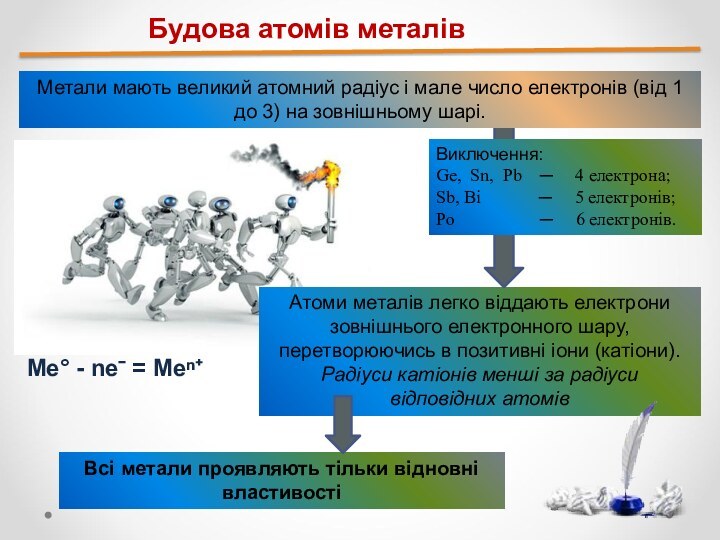
будови атомів металів;
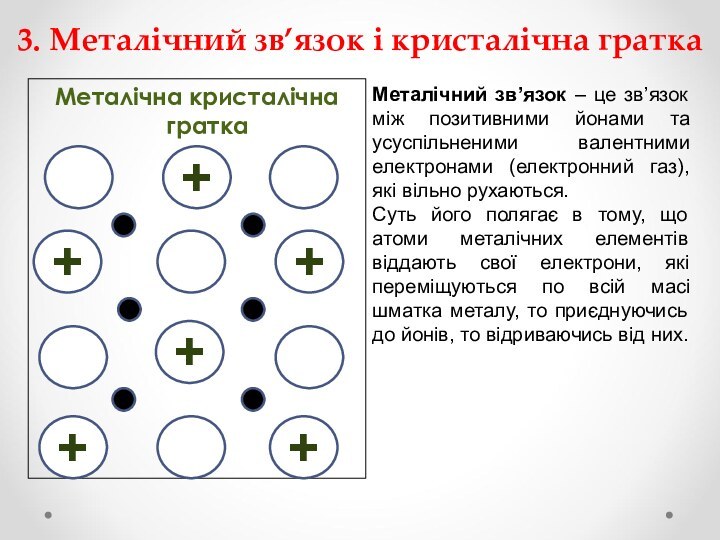
визначити особливості металічного зв’язку;
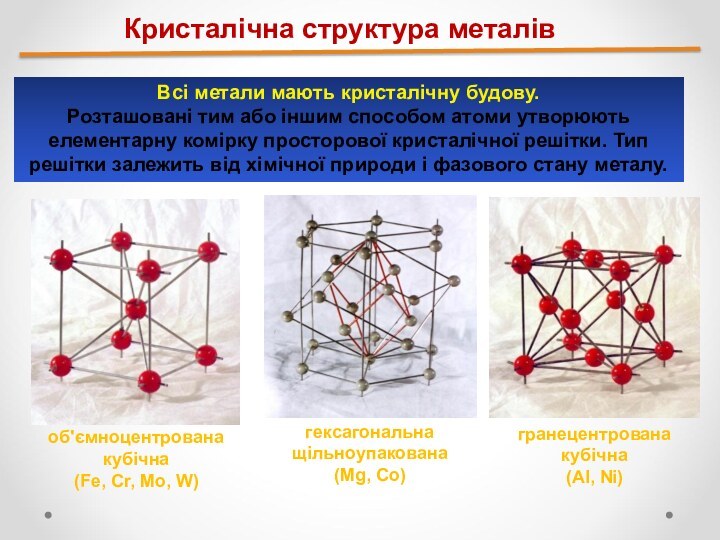
навчитися характеризувати фізичні властивості
металів;розглянути знаходження металів у природі.