- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химииКислород(8 класс.)
Содержание
- 2. Содержание темы: «Кислород»Открытие кислородаКислород в природеФизические свойства
- 3. Кислород – самый распространенный на Земле химический
- 4. ЗадачаВ настоящее время численность населения земного шара
- 5. Кислород почти одновременно был открыт двумя выдающимися
- 6. оксюс – «кислый»генао – «рождаю»Современное название кислороду дал Антуан Лавуазье
- 7. Китайцы описали кислород еще в VIII веке
- 8. Кислород – химический элемент
- 9. Химическая формула О2Молекула Строение
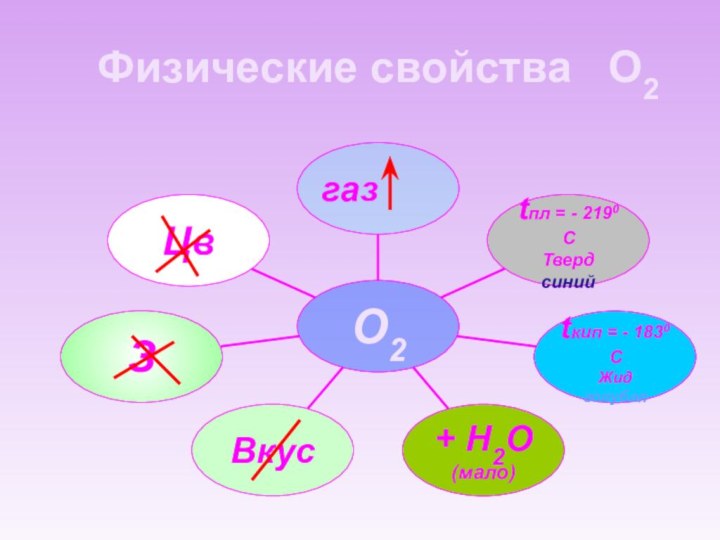
- 10. Физические свойства О2
- 11. Аллотропные модификации3О2 → 2О3 кислород
- 12. Физические свойства озона О3
- 13. Не ядовит, поддерживает процессы дыхания,
- 15. Выделение и потребление кислорода зелеными растениямиФотосинтез
- 16. В промышленности кислород получаютИз жидкого воздухаЭлектролизом воды Н2О = Н2 + О222
- 17. В лаборатории кислород получаютKClO3⭢ KCl + O2 KMnO4 ⭢ K2MnO4 + MnO2 + O22322
- 18. Способы собиранияВытеснением водыВытеснением воздуха
- 19. Химические свойства О2Взаимодействует с простыми веществаминеметаллы металлыобразуя оксиды
- 20. НеметаллыСЕРАS + O2→SO2 СЕРАСЕРАСЕРА
- 21. P + O2 → P2O5НеметаллыФосфорГорение фосфора4 52
- 22. Металлы3Fe+O22⭢Fe3O4ржавчинажелезожелезожелезо
- 23. МеталлыСа+О 2 →СаО22негашеная известькальций
- 24. Сложные вещества
- 25. Применение кислорода
- 26. ЛитератураЗанимательная химия Л.Ю.АликбероваХимия К.К.КурмашеваХимия 8 класс Н.Е.КузнецоваПоурочные разработки по химии М.Ю. ГорковенкоПоурочные планы В.Г. Денисова
- 27. Т е с т«Кислород»
- 28. Химическая формула молекулы кислорода:О2ОN2Cl2
- 29. Этот элемент необходим для жизни: АзотКислородРтутьФтор
- 30. В атмосфере воздуха этого элемента 21% по объему: КислородУглеродАзотАлюминий
- 31. Поддерживает горение:О2СО2
- 32. Как называются соединения, которые образуются в результате взаимодействия кислорода с металлами? ОксидыКислотыСолиОснования
- 33. У м н и ц а !!!
- 34. Скачать презентацию
- 35. Похожие презентации
Содержание темы: «Кислород»Открытие кислородаКислород в природеФизические свойства кислородаХимический элемент и простое веществоПолучение кислородаХимические свойстваПрименение ЛитератураТестирование по теме





























Слайд 2
Содержание темы: «Кислород»
Открытие
кислорода
Кислород в природе
Физические свойства кислорода
Химический
элемент
Слайд 3
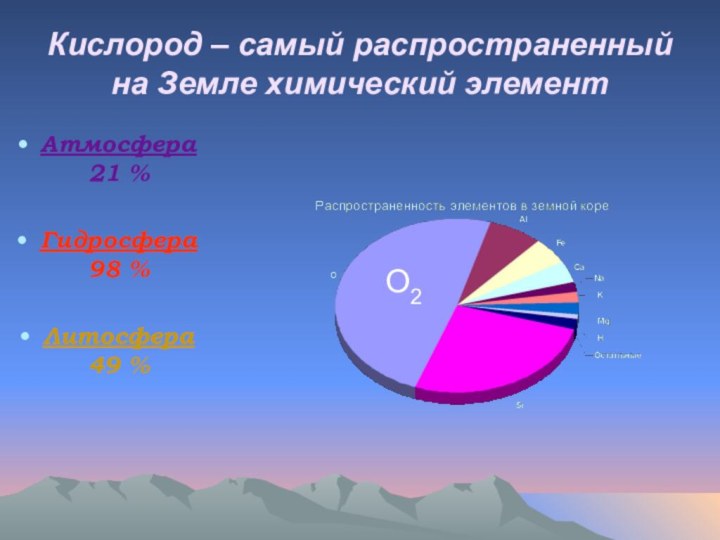
Кислород – самый распространенный на Земле химический элемент
Атмосфера
21 %
Гидросфера 98 %
Литосфера 49 %
О2
Слайд 4
Задача
В настоящее время численность населения земного шара приблизилась
к 6-ти миллиардной отметке, количество кислорода в земной атмосфере
1015 тонн.Сколько атмосферного кислорода по массе приходится на одного жителя планеты? (Общее число жителей планеты - 6 • 109)
Решение:
m(общ) 1015
m (O) = = = 1,67 • 105 т/ чел
n(общ) 6 •109
Ответ:
На одного жителя планеты приходится 167000 тонн атмосферного кислорода (О2)
Слайд 5
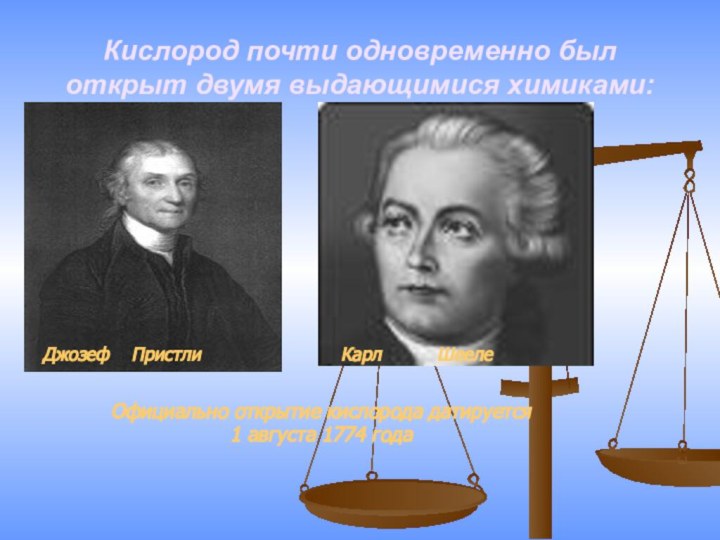
Кислород почти одновременно был открыт двумя выдающимися химиками:
Джозеф
Пристли
Карл ШеелеОфициально открытие кислорода датируется
1 августа 1774 года
Слайд 7
Китайцы описали кислород еще в
VIII веке
В
Европе изобретатель подводной лодки Корнелиус Дреббель в начале XVII
в. выделил кислород, выяснил его роль в дыхании и использовал на своей подводной лодке.
Слайд 9
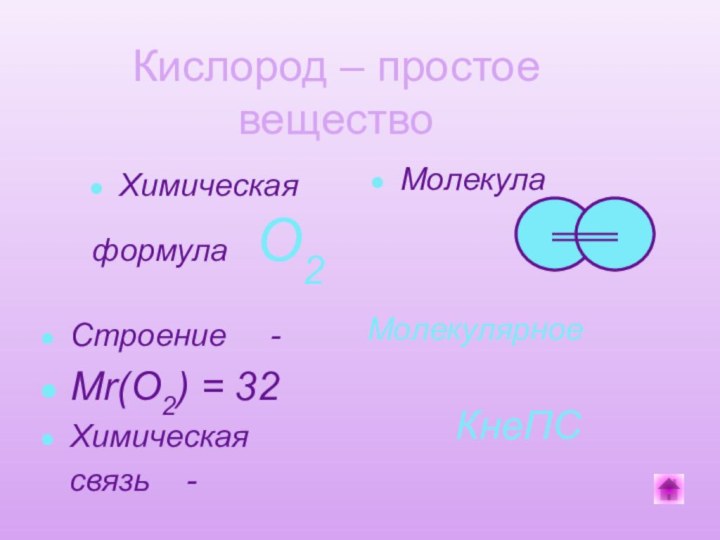
Химическая формула О2
Молекула
Строение
-
Мr(O2) = 32
Химическая
связь -
Молекулярное
КнеПСКислород – простое вещество
Слайд 11
Аллотропные модификации
3О2 → 2О3
кислород
озон
О3 → О +
О2 озон атомарный
кислород
сильный
окислитель
Слайд 13
Не ядовит, поддерживает процессы дыхания, горения,
окисления, гниения
Быстро разрушает резину, обесцвечивает красители, обладает
бактерицидными свойствами, ядовит Сравнительная характеристика
Слайд 24
Сложные вещества
С3Н8 + О2→ СО2⭡ + Н2О
При
горении сложных веществ
образуется столько
продуктов,
сколько элементов было
в сложном веществе.
4
3
5