- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Фосфор, строение атома, аллотропия, химические свойства фосфора. Оксид фосфора(V)
Содержание
- 2. ДЕВИЗ УРОКА: «Фосфор-элемент жизни и мысли»А.Е.Ферсман
- 3. ЦЕЛИ УРОКА:1. Изучить физические и
- 4. ВОПРОСЫ К ТЕМЕ УРОКА1 Открытие фосфора(1669год
- 5. ОТКРЫТИЕ ФОСФОРАФосфор (Phosphorus, от греч. Phoros –
- 6. СТРОЕНИЕ АТОМА ФОСФОРА +15 P ) ) ) 2 8 51S22S22P63S23P31S22S22P63S23P3
- 7. НАХОЖДЕНИЕ ФОСФОРА В ПРИРОДЕ Фосфор
- 8. ФИЗИЧЕСКИЕ СВОЙСТВА. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ФОСФОРА.Черный фосфор Красный
- 9. ХИМИЧЕСКИЕ СВОЙСТВА ФОСФОРА Химические свойства фосфораВ
- 10. Физические и химические свойства оксида фосфора (V).
- 11. Биологическое значение фосфора. Соединения фосфора- обязательная
- 12. Круговорот фосфора в природеРастения поглощают необходимый им
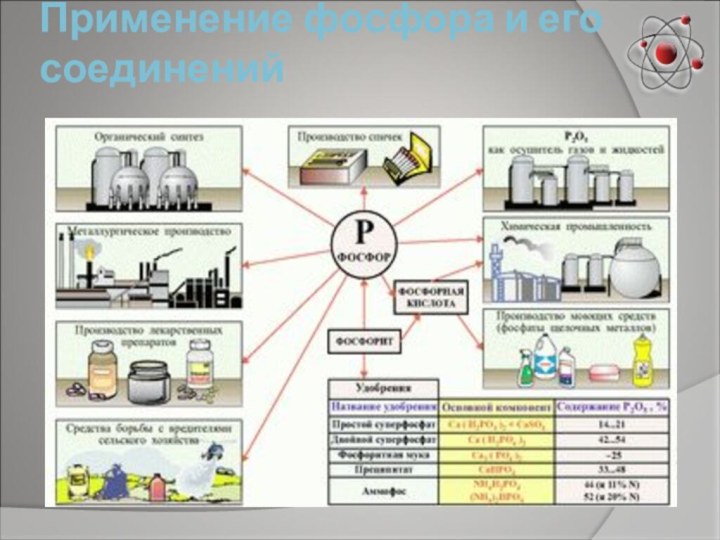
- 13. Применение фосфора и его соединений
- 14. Проверь себя:А1 Электронная конфигурация 1S22S22P63S23P6 соответствует частице:1) Р+32) Р-33) Р+54) N-3
- 15. Проверь себя:А2 С какими из перечисленных веществ
- 16. Проверь себя:А3 Какие из приведенных суждений
- 17. Проверь себя:А4 Наибольшую степень окисления имеет фосфор в соединении:1) Са3Р2 2) Р2О3 3) Н3РО44) РН3
- 18. Проверь себя:А5 Как фосфор так и азот взаимодействуют :с серойс водородомс водой с металлическим магнием
- 19. Проверь себя: А6 Сумма коэффициентов в уравнении
- 20. Проверь себя: А7 Дополните фразу: При взаимодействии с металлами фосфор образуетфосфатыфосфидыгидрофосфатыдигидрофосфаты
- 21. Разминка. Игра-эстафета
- 22. Скачать презентацию
- 23. Похожие презентации



















Слайд 3
ЦЕЛИ УРОКА:
1. Изучить физические и химические
свойства фосфора, оксида фосфора. Закрепить понятие аллотропии на примере
аллотропных модификаций фосфора.3. Развивать интерес к предмету, формирование диалектико-материалистического мировоззрения учащихся, рассматривая круговорот фосфора в природе.
2. Способствовать развитию у учащихся умения анализировать, обобщать, систематизировать полученные знания.
Слайд 4
ВОПРОСЫ К ТЕМЕ УРОКА
1 Открытие фосфора(1669год –немецкий
химик Х. Бранд).
2. Строение атома фосфора.
3. Нахождение
в природе.4. Физические свойства. Аллотропные модификации фосфора.
5. Химические свойства фосфора. Окислительно-восстановительная двойственность.
6. Оксид фосфора(V), физические и химические свойства.
7. Биологическое значение фосфора. Круговорот фосфора в природе. Применение фосфора и его соединений.
Слайд 5
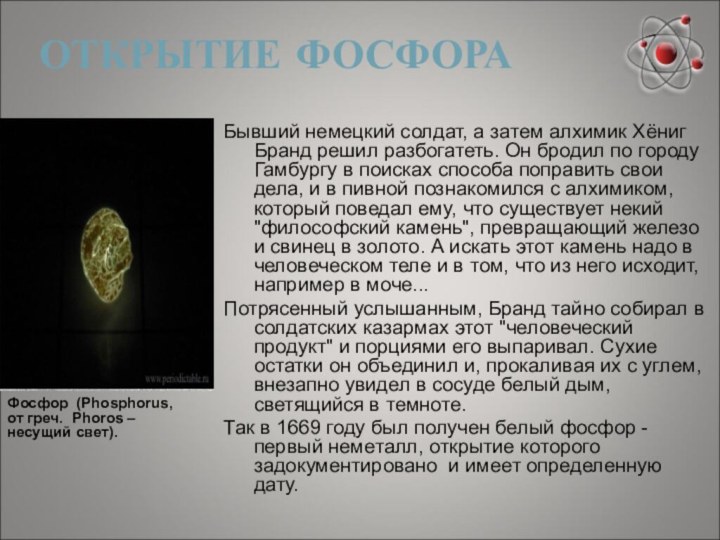
ОТКРЫТИЕ ФОСФОРА
Фосфор (Phosphorus, от греч. Phoros – несущий
свет).
Бывший немецкий солдат, а затем алхимик Хёниг Бранд решил
разбогатеть. Он бродил по городу Гамбургу в поисках способа поправить свои дела, и в пивной познакомился с алхимиком, который поведал ему, что существует некий "философский камень", превращающий железо и свинец в золото. А искать этот камень надо в человеческом теле и в том, что из него исходит, например в моче...Потрясенный услышанным, Бранд тайно собирал в солдатских казармах этот "человеческий продукт" и порциями его выпаривал. Сухие остатки он объединил и, прокаливая их с углем, внезапно увидел в сосуде белый дым, светящийся в темноте.
Так в 1669 году был получен белый фосфор - первый неметалл, открытие которого задокументировано и имеет определенную дату.
Слайд 7
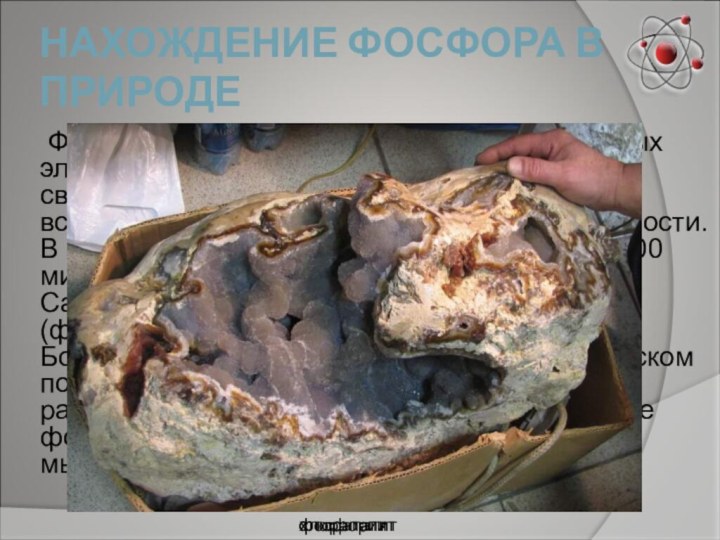
НАХОЖДЕНИЕ ФОСФОРА В ПРИРОДЕ
Фосфор -
один из наиболее распространённых элементов в земной коре (0,093%
по массе).В свободном состоянии в природе фосфор не встречается из-за высокой химической активности. В связанном виде он входит в состав около 200 минералов, главным образом апатитов Ca3(PO4)2*CaCl2 (хлорапатит), Ca3(PO4)2*CaF2 (фторапатит), а также фосфоритов Ca3(PO4)2. Большие запасы апатитов находятся на Кольском полуострове. Фосфор входит в состав растительных и животных белков. Содержание фосфора в тканях мозга составляет 0,38%, в мышцах 0,27%.фторапатит
фосфорит
хлорапатит
Слайд 8
ФИЗИЧЕСКИЕ СВОЙСТВА. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ФОСФОРА.
Черный фосфор
Красный фосфор
Белый
фосфор
Фосфор образует несколько аллотропных модификаций. Главные из них:
белый, красный и черный фосфор. Белый фосфор –кристаллический порошок, имеет молекулярную кристаллическую решетку. Он не растворяется в воде, но растворяется в органических растворителях, летуч. Белый фосфор – сильный яд. При обычных условиях окисляется кислородом воздуха, окисление фосфора сопровождается свечением, которое хорошо заметно в темноте.
Красный фосфор- порошок темно – красного цвета, он не ядовит, нелетуч. Взаимодействует с кислородом только при поджигании. Имеет атомную кристаллическую решетку. При давлении12∙108 Па переходит в черный фосфор.
Черный фосфор образуется из белого при высоком давлении. По внешнему виду он похож на графит, имеет атомную кристаллическую решетку, обладает полупроводниковыми свойствами.
Слайд 9
ХИМИЧЕСКИЕ СВОЙСТВА ФОСФОРА
Химические свойства фосфора
В химических
реакциях фосфор проявляет окислительно-восстановительную двойственность.
Фосфор взаимодействует с металлами, галогенами,
серой, кислородом. (Данные уравнения реакций будут предложены к выполнению учащимися в домашнем задании)С солями –окислителями фосфор реагирует с сильным взрывом , что может привести к несчастному случаю, его нельзя смешивать с бертолетовой солью:
6Р +5KCIO3→ 3 P2O5 +5KCI
Эта реакция используется в производстве спичек.
Составить схемы электронного баланса данных реакций.
2P0+3Ca0=Ca3+2P2–3
окислитель
восстановитель
4P0+5O20=2P2+5O5–2
восстановитель
окислитель
Слайд 10
Физические и химические свойства оксида фосфора (V).
Оксид фосфора
(V) Р2О5 –белое кристаллическое веществ . Он не может
быть получен дегидратацией фосфорной кислоты из-за высокой экзотермичности его реакции с водой. На этом основано его практическое применение как осушителя. Взаимодействует с водой при нагревании ,образуя ортофосфорную кислоту. Оксид фосфора (V) Р2О5
Сделайте сами вывод о характере этого оксида ,выберите уравнения возможных реакций, характерных для него:
Оксид фосфора (V) реагирует с :
а)водой,
б)гидрооксидом калия
в)оксидом углерода(ΙV)
г)железом
д)оксидом бария
Уравнения возможных реакций составьте в тетради.
Слайд 11
Биологическое значение фосфора.
Соединения фосфора- обязательная составляющая растений
, животных, человека. В растениях фосфор содержится главным
образом в семенах, плодах:В организме человека и животных- в скелете ,мышечной ,нервной ткани.
Слайд 12
Круговорот фосфора в природе
Растения поглощают необходимый им фосфор
из почвы. Животные получают его с растительной пищей .После
отмирания растений и животныхорганические фосфоросодержащие соединения превращаются в неорганические –фосфаты под воздействием фосфоробактерий. Недостаток фосфора в почве не восполняется естественным путем, поэтому необходимо вносить фосфоросодержащие удобрения в почву.
Слайд 14
Проверь себя:
А1 Электронная конфигурация 1S22S22P63S23P6
соответствует частице:
1) Р+3
2) Р-3
3) Р+5
4) N-3
Слайд 15
Проверь себя:
А2 С какими из перечисленных веществ не
реагирует оксид фосфора (V):
вода
оксид кальция
гидроксид натрия
4) оксид серы (VΙ)
Слайд 16
Проверь себя:
А3 Какие из приведенных суждений верны:
А
Фосфор образует несколько аллотропных модификаций:
белый, красный и черныйБ Все аллотропные модификации фосфора имеют атомные кристаллические
решетки
2) Верно только Б
3) Верны оба утверждения
4) Оба утверждения неверны
Верно только А
Слайд 17
Проверь себя:
А4 Наибольшую степень окисления имеет фосфор в
соединении:
1) Са3Р2
2) Р2О3
3) Н3РО4
4) РН3
Слайд 18
Проверь себя:
А5 Как фосфор так и азот
взаимодействуют :
с серой
с водородом
с водой
с металлическим магнием
Слайд 19
Проверь себя:
А6 Сумма коэффициентов в уравнении
реакции взаимодействия
фосфора с
кислородом равна:5
10
11
7





























