- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему: Алкины
Содержание
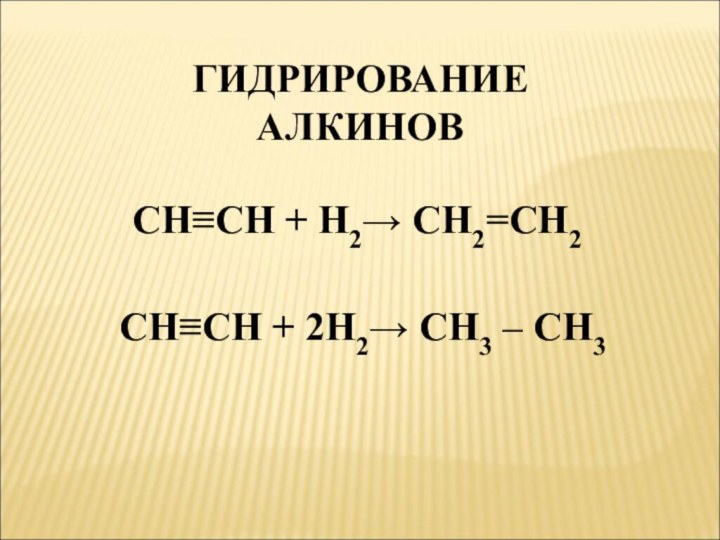
- 2. CH≡CH + H2→ CH2=CH2CH≡CH + 2H2→ CH3 – CH3ГИДРИРОВАНИЕ АЛКИНОВ
- 3. ГАЛОГЕНИРОВАНИЕ АЛКИНОВCH≡CH + Br2→ CHBr=CHBr 1,2-дибромэтенCH≡CH + 2Br2→ CHBr2 – CHBr21,1,2,2-тетрабромэтан
- 4. ГИДРОГАЛОГЕНИРОВАНИЕ АЛКИНОВCH≡CH + HCl→ CH2=CHClхлорэтен или винилхлоридCH2=CHCl + HCl→ CH3 – CHCl21,1-дихлорэтан
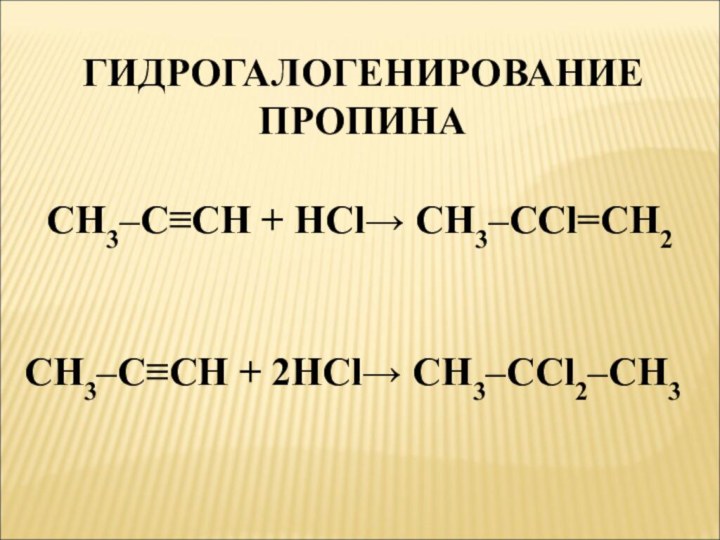
- 5. ГИДРОГАЛОГЕНИРОВАНИЕ ПРОПИНАCH3–C≡CH + HCl→ CH3–CCl=CH2CH3–C≡CH + 2HCl→ CH3–CCl2–CH3
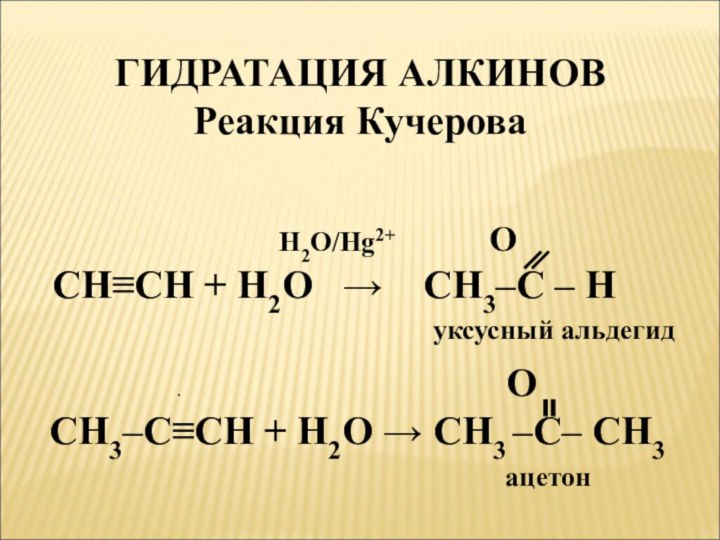
- 6. ГИДРАТАЦИЯ АЛКИНОВРеакция Кучерова
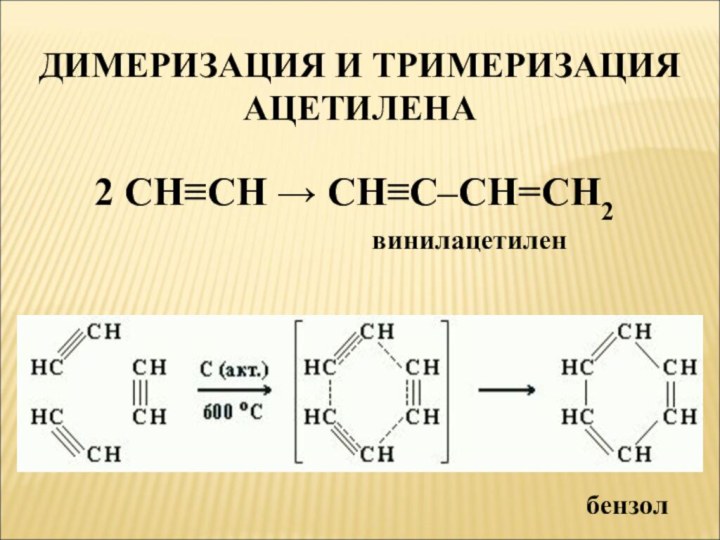
- 7. ДИМЕРИЗАЦИЯ И ТРИМЕРИЗАЦИЯ АЦЕТИЛЕНА 2 CH≡CH → CH≡C–CH=CH2винилацетиленбензол
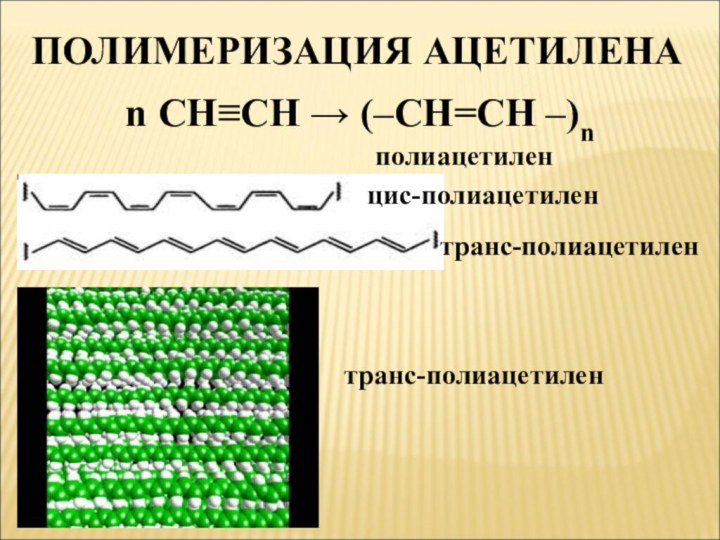
- 8. ПОЛИМЕРИЗАЦИЯ АЦЕТИЛЕНАn CH≡CH → (–CH=CH –)nполиацетиленцис-полиацетилентранс-полиацетилентранс-полиацетилен
- 9. ГОРЕНИЕ АЦЕТИЛЕНАГорение ацетилена на воздухекоптящим пламенемАцетиленовая сварка2C2H2 + 5O2 → 4CO2 + 2H2O + Q
- 10. ОКИСЛЕНИЕ АЦЕТИЛЕНОВЫХ УГЛЕВОДОРОДОВ3CH≡CH + 8KMnO4 → 3KOOC
- 11. Реакции замещения – кислотные свойства алкиновCH≡CH +
- 12. ПОЛУЧЕНИЕ АЦЕТИЛЕНАВпервые ацетилен получил в 1836 г.
- 13. В 1862 году немецкий химик Вёлер получил
- 14. Сейчас широко применяют метод получения ацетилена из
- 15. Получение ацетилена и опыты с ним
- 16. Взрыв ацетиленида серебра
- 17. Осуществить превращения:
- 19. Скачать презентацию
- 20. Похожие презентации





![Презентация по химии на тему: Алкины Реакции замещения – кислотные свойства алкиновCH≡CH + 2[Ag(NH3)2]OH→ AgC≡CAg↓ + 4NH3 +](/img/tmb/6/526170/a46e09425897492491a39570bc927368-720x.jpg)







Слайд 3
ГАЛОГЕНИРОВАНИЕ АЛКИНОВ
CH≡CH + Br2→ CHBr=CHBr
1,2-дибромэтен
CH≡CH + 2Br2→
CHBr2 – CHBr2
1,1,2,2-тетрабромэтан
Слайд 4
ГИДРОГАЛОГЕНИРОВАНИЕ АЛКИНОВ
CH≡CH + HCl→ CH2=CHCl
хлорэтен или винилхлорид
CH2=CHCl +
HCl→ CH3 – CHCl2
1,1-дихлорэтан
Слайд 6
ГИДРАТАЦИЯ АЛКИНОВ
Реакция Кучерова
H2O/Hg2+ O
CH≡CH + H2O → CH3–C – H
уксусный альдегид
. О
CH3–C≡CH + H2O → CH3 –C– CH3
ацетон
Слайд 8
ПОЛИМЕРИЗАЦИЯ АЦЕТИЛЕНА
n CH≡CH → (–CH=CH –)n
полиацетилен
цис-полиацетилен
транс-полиацетилен
транс-полиацетилен
Слайд 9
ГОРЕНИЕ АЦЕТИЛЕНА
Горение ацетилена на воздухе
коптящим пламенем
Ацетиленовая сварка
2C2H2 +
5O2 → 4CO2 + 2H2O + Q
Слайд 10
ОКИСЛЕНИЕ АЦЕТИЛЕНОВЫХ УГЛЕВОДОРОДОВ
3CH≡CH + 8KMnO4 → 3KOOC –
COOK + 8MnO2 + 2KOH + 2H2O
оксалат калия
3R-C≡C-R +
4KMnO4+ 2H2O → 3R-(C=O)-(C=O)-R + 4MnO2 + 4KOHАлкины обесцвечивают раствор перманганата калия.
Слайд 11
Реакции замещения – кислотные свойства алкинов
CH≡CH + 2[Ag(NH3)2]OH→
AgC≡CAg↓ + 4NH3 + 2H2O
ацетиленид серебра
CH≡CH + 2[Cu(NH3)2]Cl→
CuC≡CCu↓ + NH4Cl + 3NH3 + 2H2Oацетиленид меди (I)
Слайд 12
ПОЛУЧЕНИЕ АЦЕТИЛЕНА
Впервые ацетилен получил в 1836 г. Эдмунд
Дэви из карбида калия.
К2С2 + Н2О = С2Н2 +
2КОН Слайд 13 В 1862 году немецкий химик Вёлер получил карбид
кальция: СаО + 3С = СаС2 + СО
Гидролизом карбида
кальция ацетилен получают до сегодняшнего дня:СaC2 + 2H2O = Ca(OH)2 + C2H2
Сварочный
ацетиленовый
генератор.
Слайд 14 Сейчас широко применяют метод получения ацетилена из природного
газа – метана: струю метана пропускают между электродами при
температуре 1600°С и быстро охлаждают, чтобы предотвратить разложение ацетилена:2CH4 →C2H2 + 3H2
Для получения гомологов ацетилена используют ацетилениды активных металлов:
HC≡CH + 2 Na →NaC≡CNa + H2
NaC≡CNa + 2CH3Cl →CH3-C≡C-CH3 + 2NaCl
Слайд 17
Осуществить превращения:
2NaNH2 2CH3I H2O/Hg2+
Ацетилен → X → Y → Z
1. CH≡CH + 2NaNH2 → NaC≡CNa + 2NH3
2. NaC≡CNa + 2CH3I → CH3-C≡C-CH3 + 2NaI
3. CH3-C≡C-CH3 + H2O → CH3-(C=O) –CH2-CH3
Слайд 18
NaNH2 CH3I
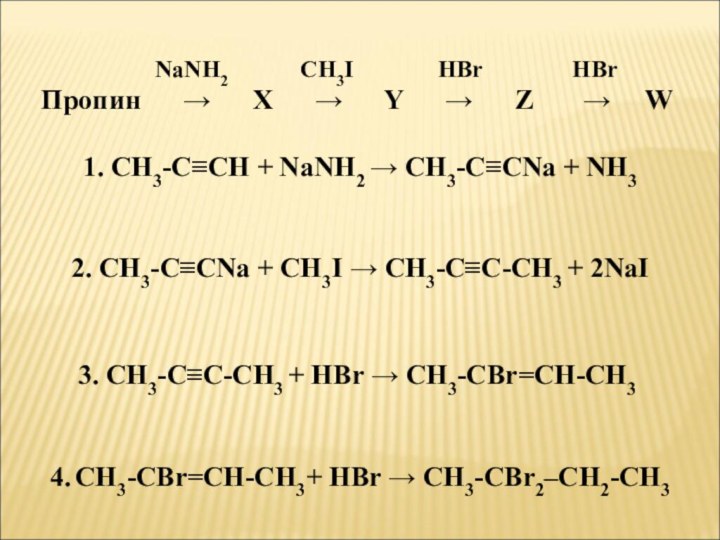
HBr HBrПропин → X → Y → Z → W
1. CH3-C≡CH + NaNH2 → CH3-C≡CNa + NH3
2. CH3-C≡CNa + CH3I → CH3-C≡C-CH3 + 2NaI
3. CH3-C≡C-CH3 + HBr → CH3-CBr=CH-CH3
4. CH3-CBr=CH-CH3+ HBr → CH3-CBr2–CH2-CH3