нормальное
плохое
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть






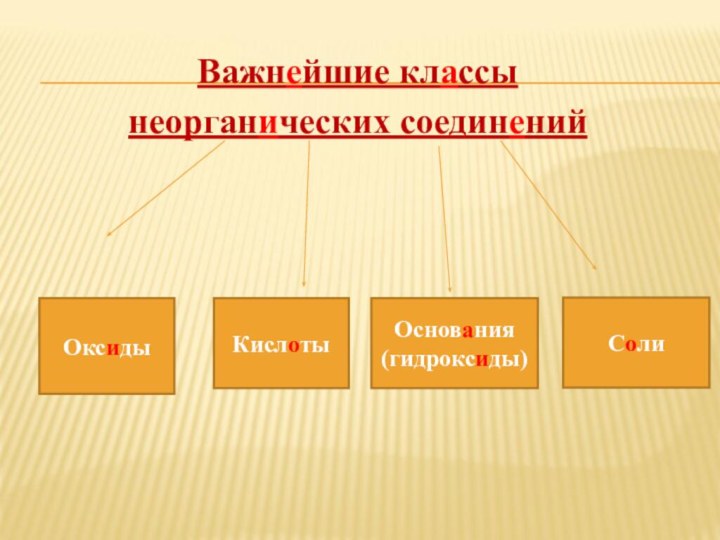





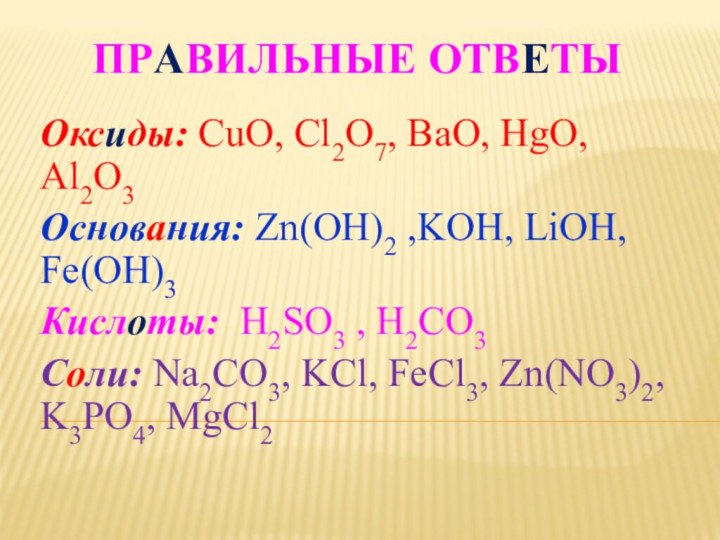








Fe O
Al(NO3)3
H2SO4
NaOH
Ca(OH)2
BaCl2
HCl
CuO
H3PO4
CO2
K2SO3
Al2(CO3)3