я не в меру, Тысячи лет до нашей эры. А
за блеск, мерцавший холодом, Люди там платили золотом!Я давно в названии века, В организме человека. Называют мной характер, Из меня почти весь трактор. Очень в яблоке полезно, И зовут меня …
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть





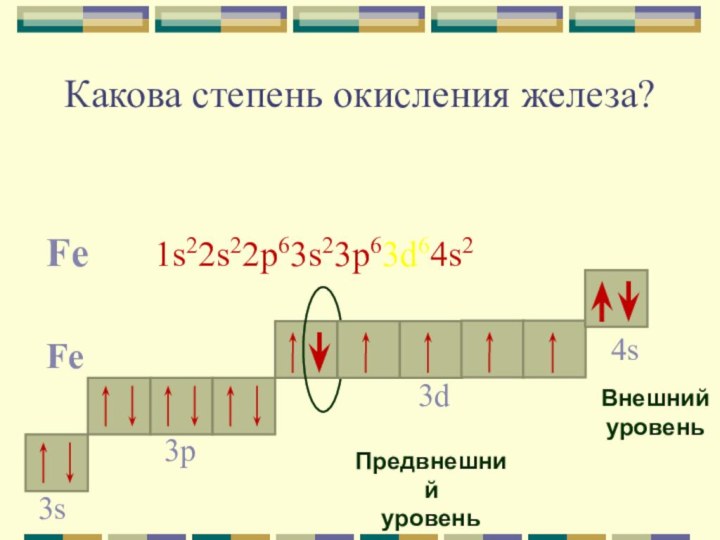



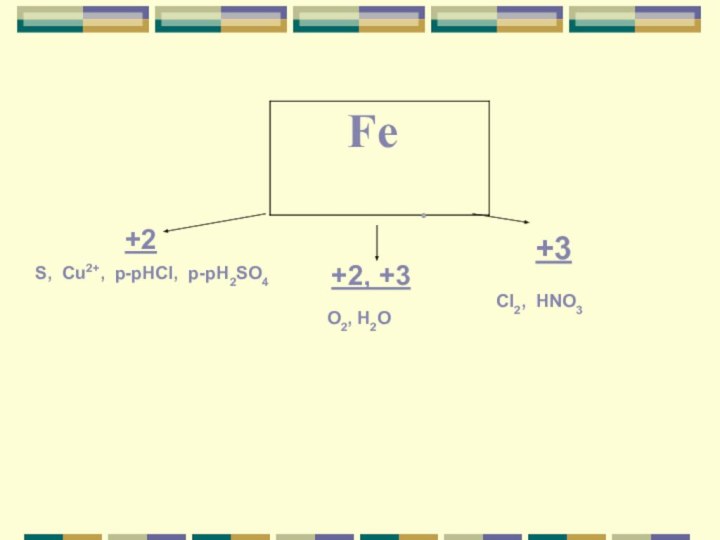









Fe3O4
(FeO*Fe2O3)
3
2
Пройдите, составив соответствующую схему реакций, от одного указанного в задании вещества к другому: