- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Окислительно-восстановительные реакции. Задание 30 ЕГЭ.
Содержание
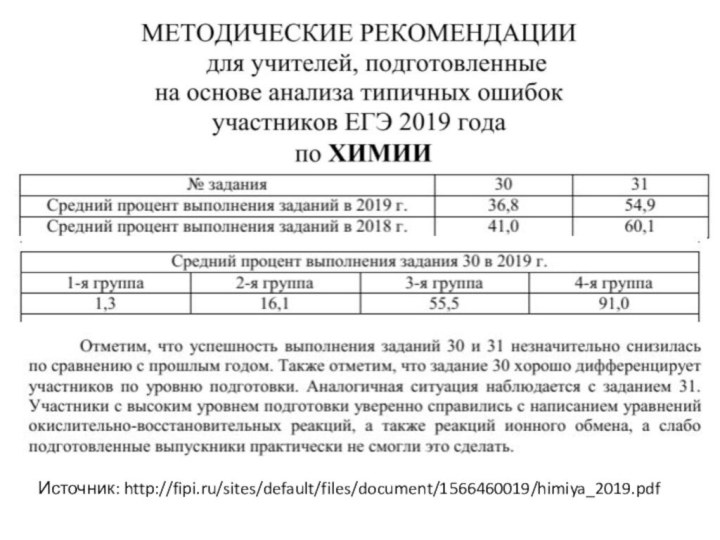
- 2. Источник: http://fipi.ru/sites/default/files/document/1566460019/himiya_2019.pdf
- 3. Возможные причины низкого процента выполнения задания 30
- 4. Цель: повысить уровень знаний учащихся в теме
- 5. Для наилучшего усвоения материала, во время просмотра презентации учащиеся заполняют таблицу по окислителям и восстановителям
- 6. Вид и формулировка задания 30:
- 8. Важнейшие окислителиCl2, Br2, O2 @;HN+5O3 @, H2S+6O4(конц.) @;KMn+7O4, Mn+4O2@;K2Cr+62O7, K2Cr+6O4@;KCl+1O, KCl+5O3 @;H2O2,соединения Fe(III)@
- 9. Простые вещества неметаллы в процессе восстановления приобретают
- 10. Изменение степени окисления азотной кислоты
- 11. Изменение степени окисления азотной кислотыAl, Fe, Cr,
- 12. Взаимодействие концентрированной азотной кислоты с неметалламиВзаимодействие с
- 13. Нитрат-ион проявляет окислительные свойства не только в
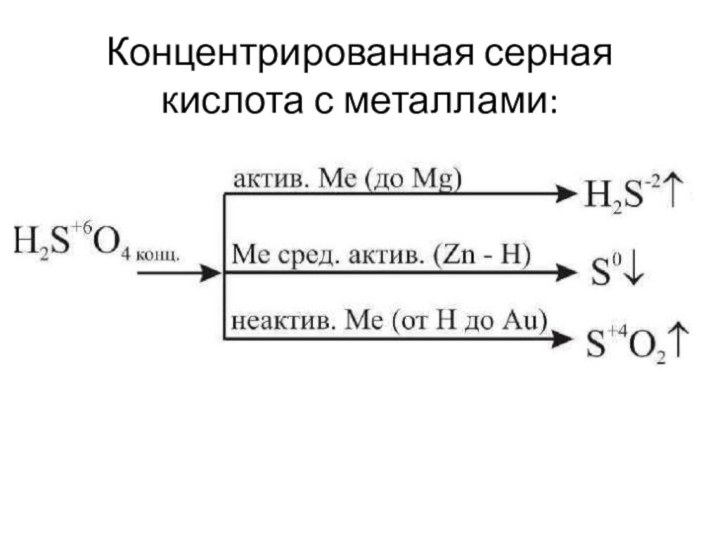
- 14. Концентрированная серная кислота с металлами:
- 15. При взаимодействии с углеродом концентрированная серная кислота
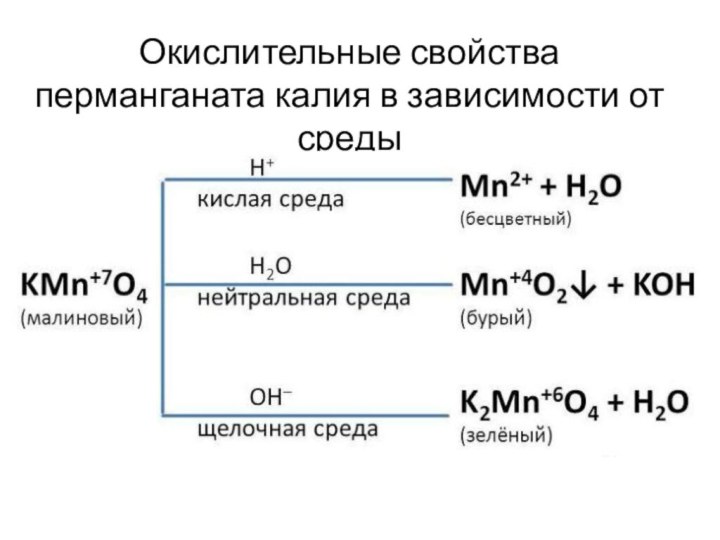
- 16. Окислительные свойства перманганата калия в зависимости от среды
- 17. Окислительные свойства Mn+4O2MnO2 + 4HCl → Cl2 + MnCl2 + H2O ⇑
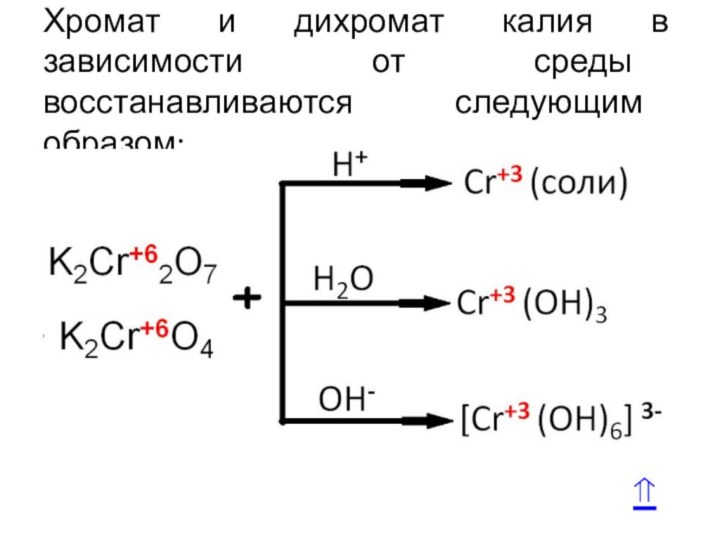
- 18. Хромат и дихромат калия
- 19. Хромат и дихромат калия в зависимости от среды восстанавливаются следующим образом:⇑
- 20. Кислородсодержащие кислоты галогенов и их соли восстанавливаются до степени окисления -1:
- 21. Окислительная способность кислот падает с возрастанием силы кислоты⇑
- 22. H2O2 – окислитель в реакциях с иодидами
- 23. Соединения железа (III)
- 24. Соединения железа (III)⇑
- 25. Важнейшие восстановителиметаллы, неметаллы: S, P, C@;Сульфиды (S-2),
- 26. Вещества, в которых элемент находится в низшей
- 27. ⇑
- 28. Окисление железа
- 29. ⇑
- 30. Азот и сера в нитритах и сульфитах приобретают высшую степень окисления⇑
- 31. ⇑
- 32. H2O-12 – окисляется до кислорода.⇑
- 33. Простые вещества неметаллы⇑
- 34. Алгоритм написания ОВР:Найти в списке возможные окислители
- 35. Примеры заданий
- 38. Для выполнения задания используйте следующий перечень веществ:
- 39. Скачать презентацию
- 40. Похожие презентации
Источник: http://fipi.ru/sites/default/files/document/1566460019/himiya_2019.pdf

































Слайд 3
Возможные причины низкого процента выполнения задания 30
Большой
объём необходимых для выполнения задания знаний;
действий при выполнении задания.Слайд 4 Цель: повысить уровень знаний учащихся в теме окислительно-восстановительные
реакции.
Задачи:
разобрать основные окислители/восстановители и продукты их восстановления/окисления, оформить
в доступной форме (в виде таблицы);Потренироваться на заданиях из тренировочных и реальных вариантов ЕГЭ разных лет;
Отработать алгоритм написания электронного баланса и расстановки коэффициентов.
Слайд 5 Для наилучшего усвоения материала, во время просмотра презентации
учащиеся заполняют таблицу по окислителям и восстановителям
Слайд 8
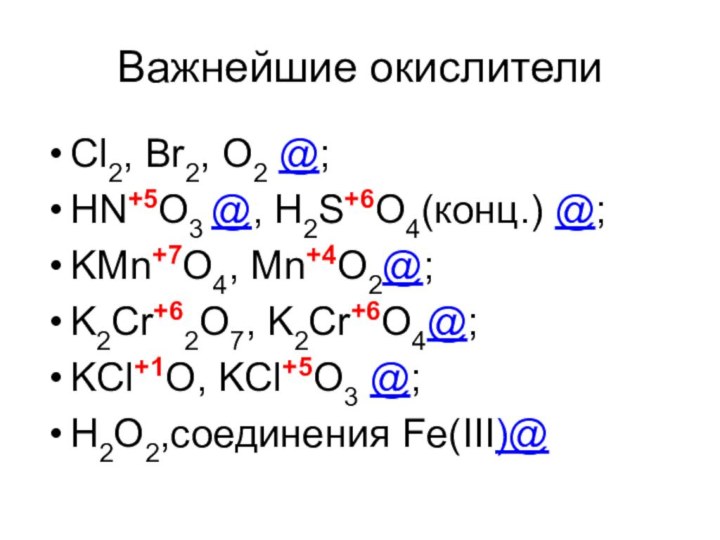
Важнейшие окислители
Cl2, Br2, O2 @;
HN+5O3 @, H2S+6O4(конц.) @;
KMn+7O4,
Mn+4O2@;
K2Cr+62O7, K2Cr+6O4@;
KCl+1O, KCl+5O3 @;
H2O2,соединения Fe(III)@
Слайд 9 Простые вещества неметаллы в процессе восстановления приобретают низшую
степень окисления:
Cl20 + 2e-→ 2 Cl-
Br20 + 2e-→ 2
Br-O20 + 4e-→ 2 O-2
⇑
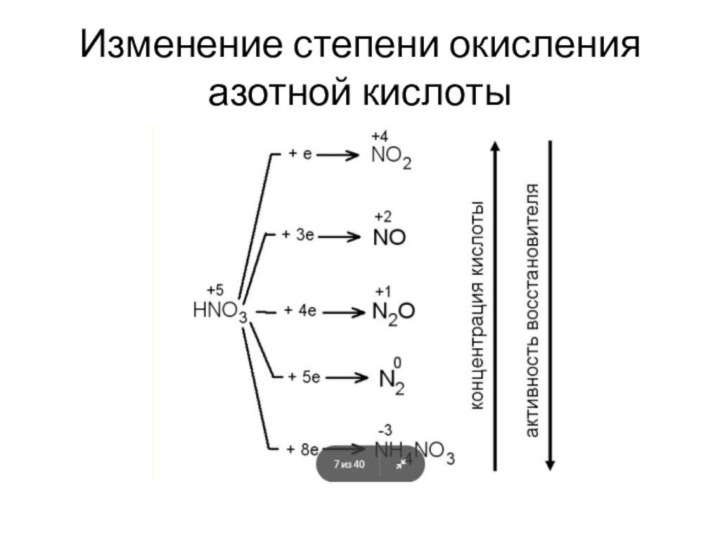
Слайд 11
Изменение степени окисления азотной кислоты
Al, Fe, Cr, Co,
Ni – в концентрированных растворах пассивируются, реакция идёт при
t;Au, Pt, Ir, Rh – реакция не идёт.
Слайд 12
Взаимодействие концентрированной азотной кислоты с неметаллами
Взаимодействие с сульфидами:
HNO3
(конц) окисляет углерод, серу и фосфор до высших кислот:
S
+ 6 HNO3 = H2SO4 + 6NO2+ 2H2O;P + 5 HNO3 = H3PO4 + 5NO2 +H2O.
Слайд 13 Нитрат-ион проявляет окислительные свойства не только в кислой,
но и щелочной среде, при этом в растворах NO3
восстанавливается активными металлами до NH3:4Zn + KNO3 + 7 KOH + H2O → 4K2[Zn(OH)4] + NH3
⇑
Слайд 15 При взаимодействии с углеродом концентрированная серная кислота реагирует
с выделением сернистого газа:
С + 2H2SO4 = CO2 +
2SO2 + 2H2O⇑
Слайд 22 H2O2 – окислитель в реакциях с иодидами (KI),
сульфидами (PbS), нитритами (KNO2), сульфитами (NaSO3), соединениями Cr+3 –
восстанавливается до H2O⇑
Слайд 25
Важнейшие восстановители
металлы, неметаллы: S, P, C@;
Сульфиды (S-2), иодиды
(I-), бромиды (Br-), а также H2S-2, HI-, HBr-, HCl-,
N-3H3,
P-3H3@;Нитриты (N+4O2), сульфиты (S+4O3);
соединения Fe(II)@, Cr(III), соединения Cr(II)@, Cu(I);
Н2, C, С+2О, H2O-12@
Слайд 26 Вещества, в которых элемент находится в низшей степени
окисления, такие как сульфиды (S-2), иодиды (I-), бромиды (Br-),
а также H2S-2, HI-, HBr-,HCl-,N-3H3, P-3H3…Восстанавливаются до 0 степени окисления, т. е. образуются простые вещества
Слайд 34
Алгоритм написания ОВР:
Найти в списке возможные окислители и
восстановители;
Определить есть ли необходимость в указании реактива среды (кислоты,
основания);Написать уравнение реакции, расставить степени окисления в окислителях, восстановителях и продуктах их взаимодействия;
Написать электронный баланс, вычислить коэффициенты, согласно отданным и принятым электронам;
Выписать окислитель и восстановитель с указанием степени окисления.