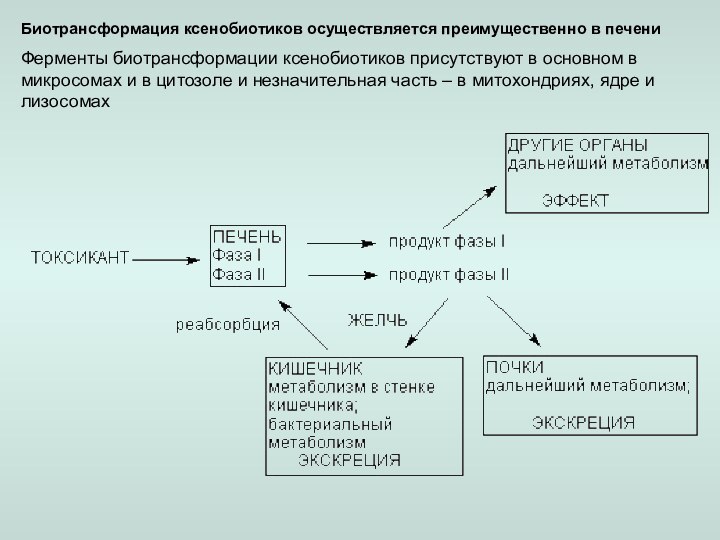
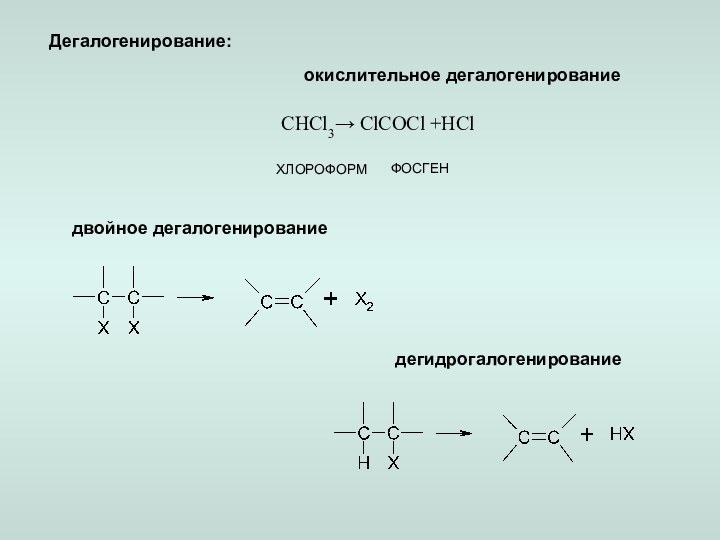
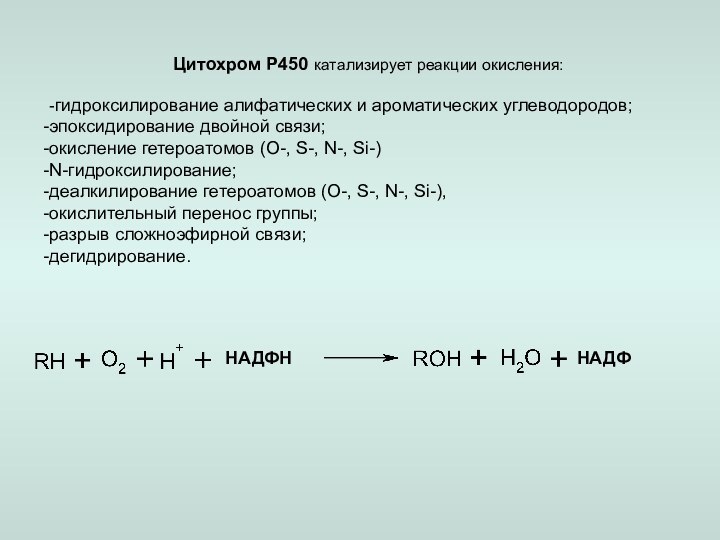
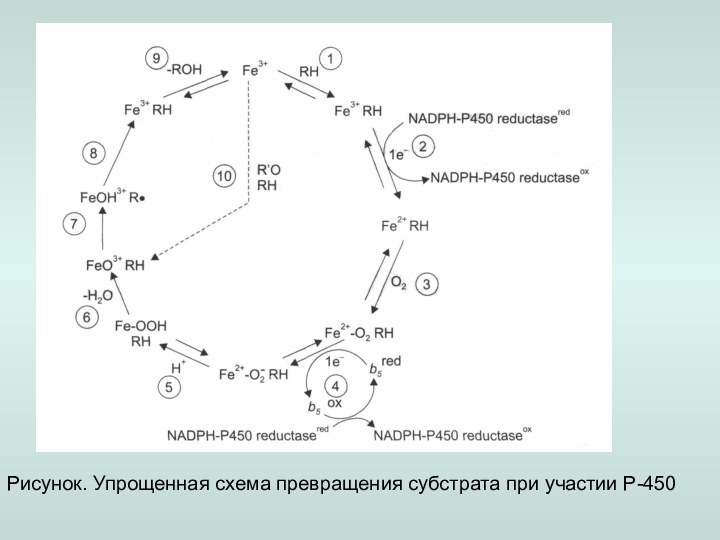
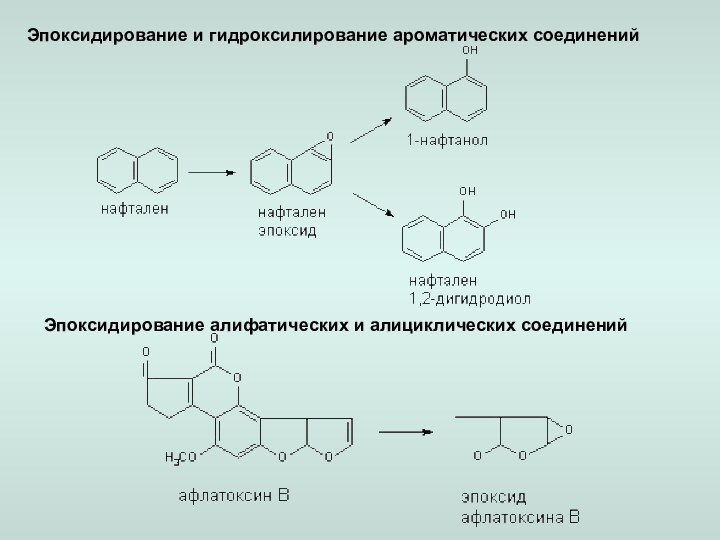
– алифатичекое или ароматическое гидроксилирование,
– эпоксидирование,
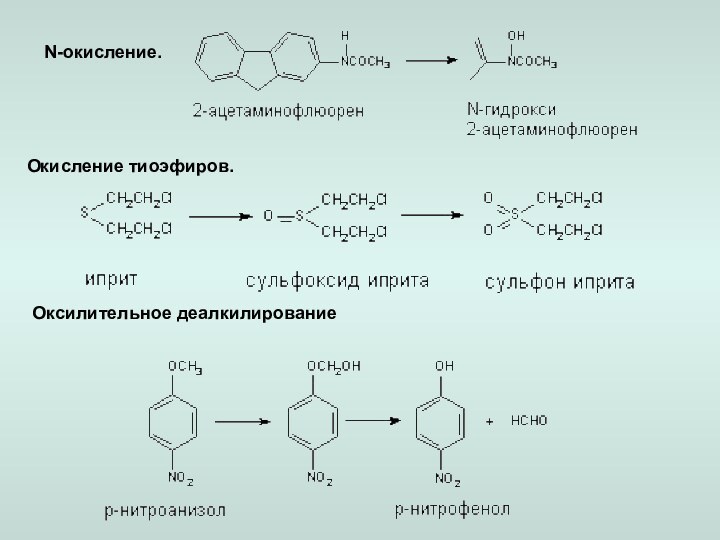
– N-гидроксилирование,
– N, S-окисление,– дезалкилирование,
– дезаминирование,
– десульфирование;
б) немикросомальное
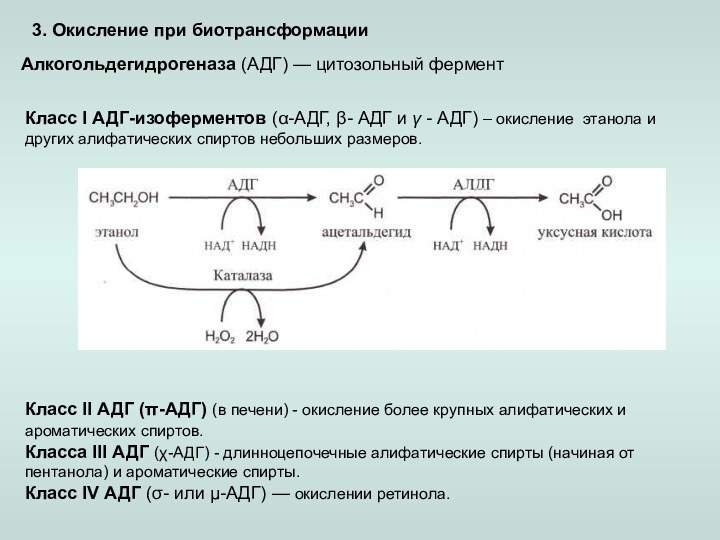
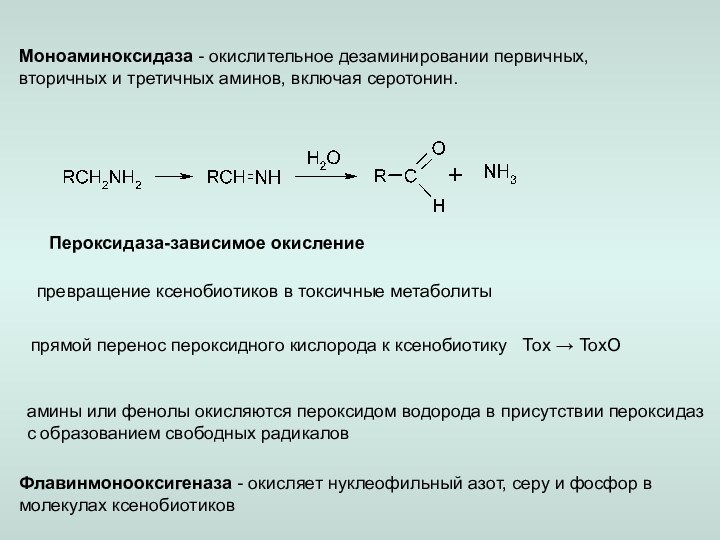
– окислительное дезаминирование,
– окисление спиртов, альдегидов,
– ароматизация алициклических соединений.
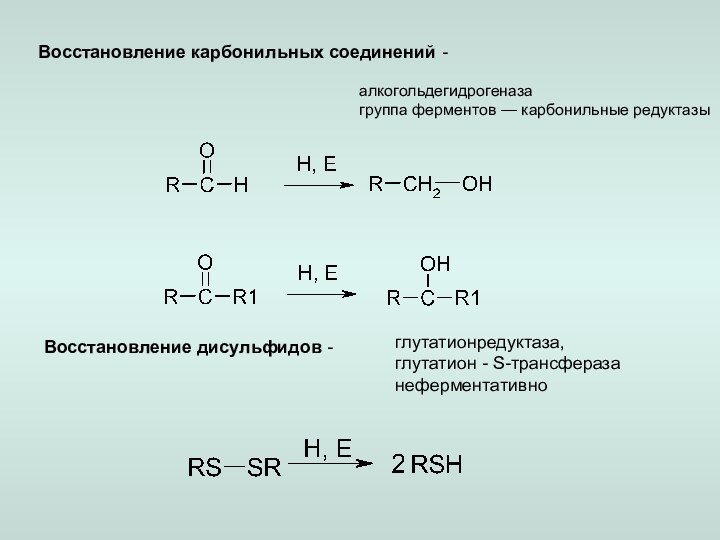
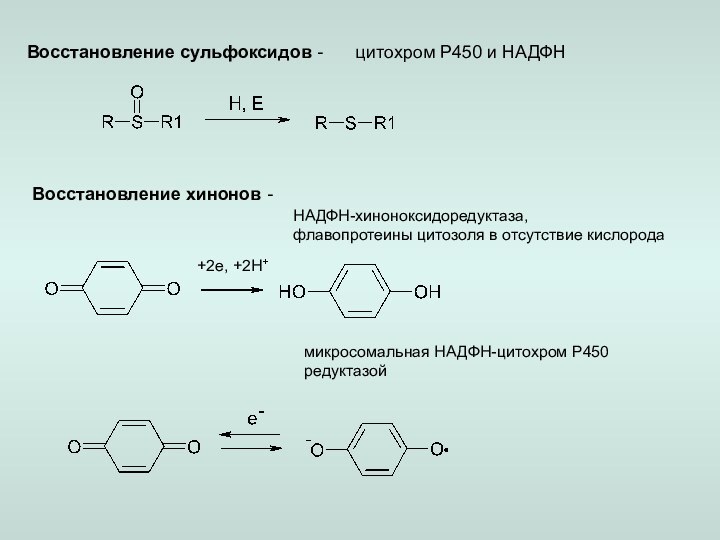
2. Восстановление:
а) восстановление нитросоединений, азотсоединений микросомальными ферментами;
б) микросомальное восстановительное галогенирование;
в) немикросоальное восстановление.
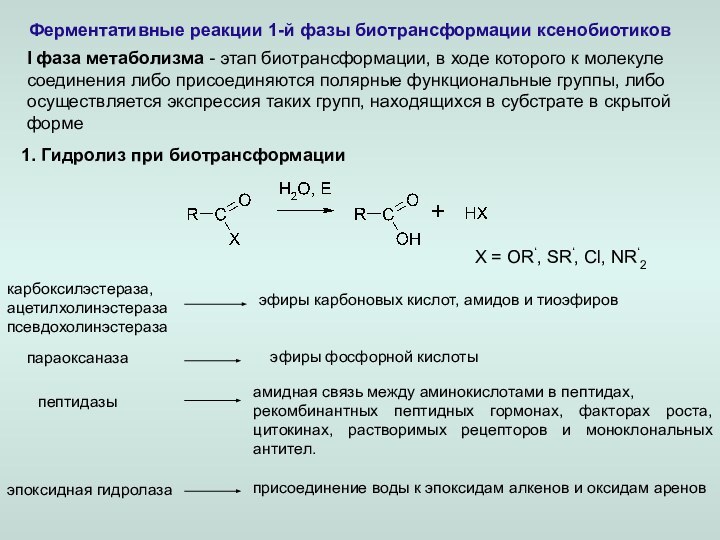
3. Гидролиз с участием микросомальных и немикросомальных ферментов.
4. Синтез (реакции коньюгирования):
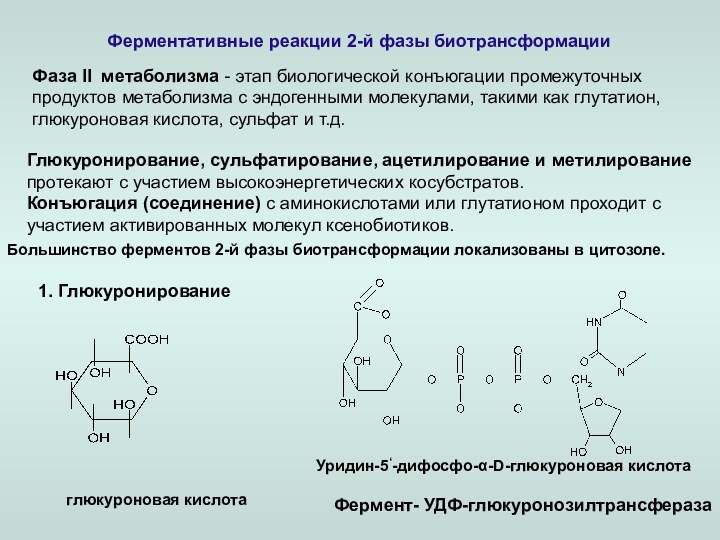
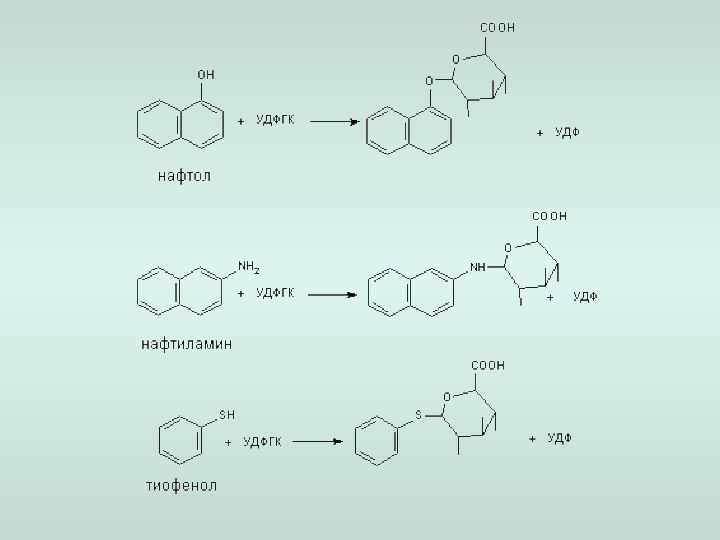
а) образование коньюгатов с глюкуроновой кислотой;
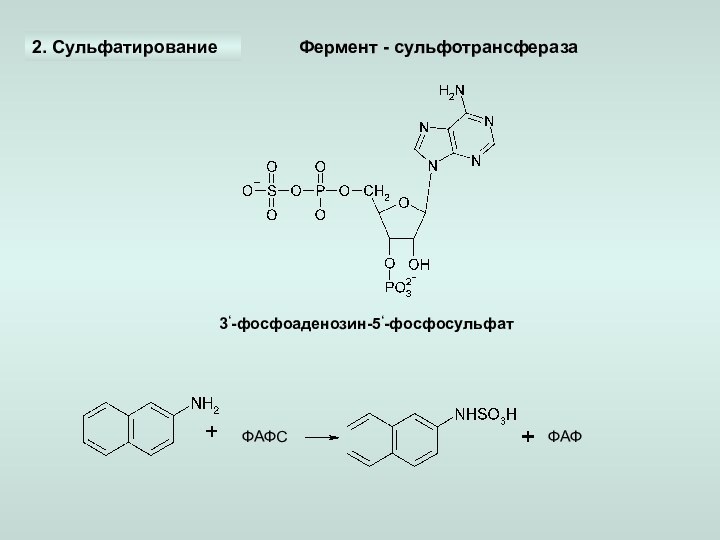
б) образование сложных эфиров с серной и фосфорной кислотами;
в) метилирование;
г) ацетилирование;
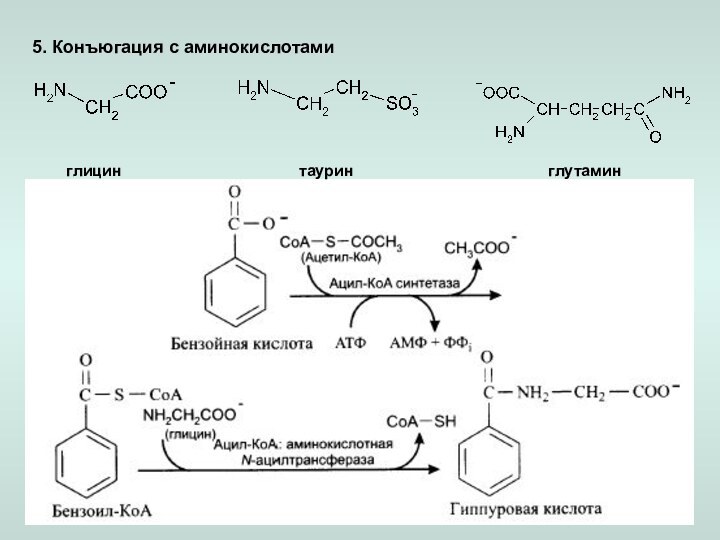
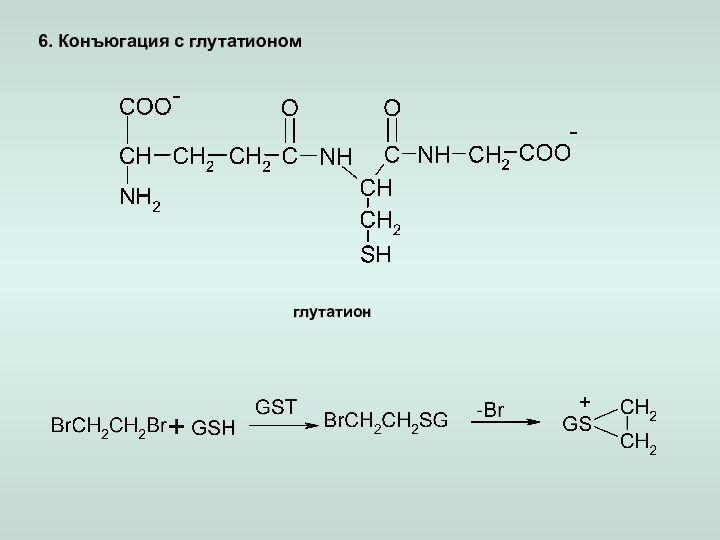
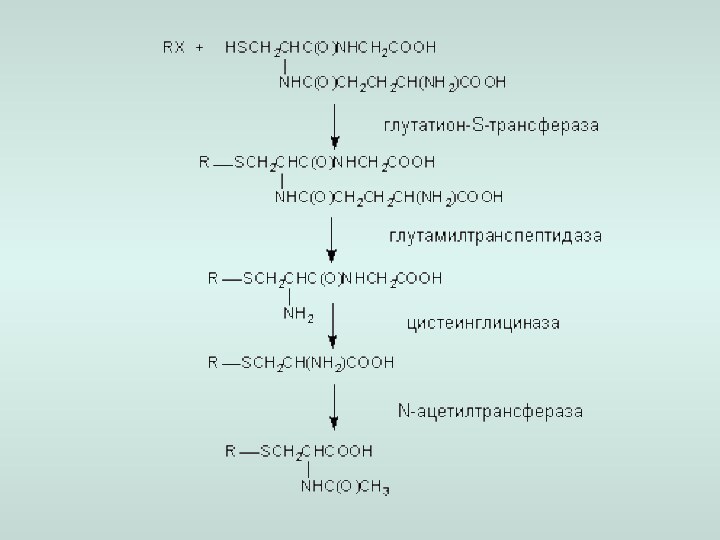
д) пептидная коньюгация.