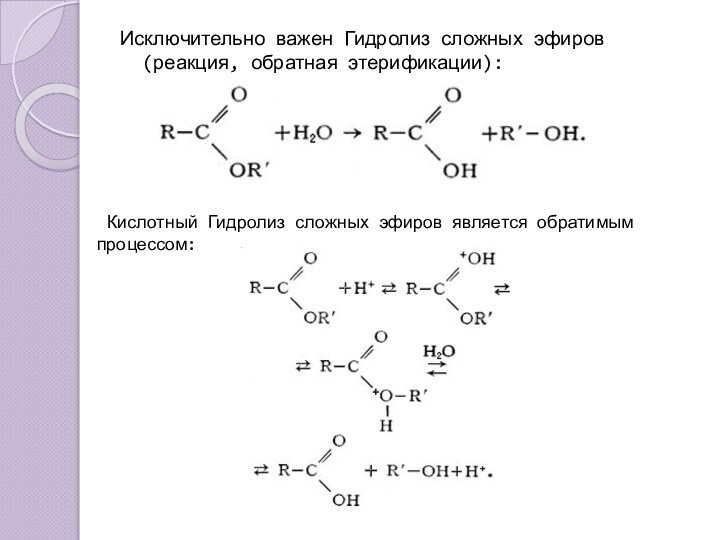
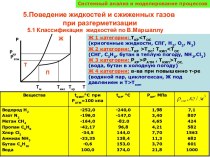
водой, приводящие
к их разложению.
Гидролизу подвергаются соединения различных классов:
соли, углеводы, белки, сложные эфиры, жиры и др.По направлению реакции гидролиза можно разделить на обратимые и необратимые
В общем виде гидролиз можно представить уравнением:
где А—В — гидролизующееся вещество, А—Н и В—ОН — продукты гидролиза