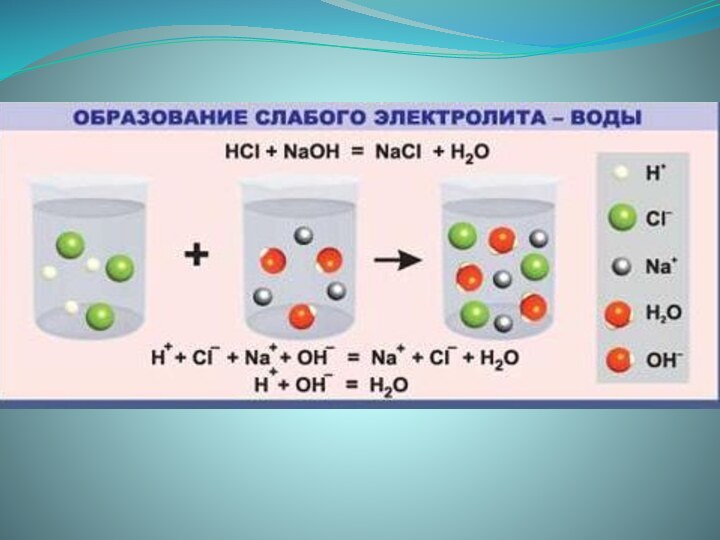
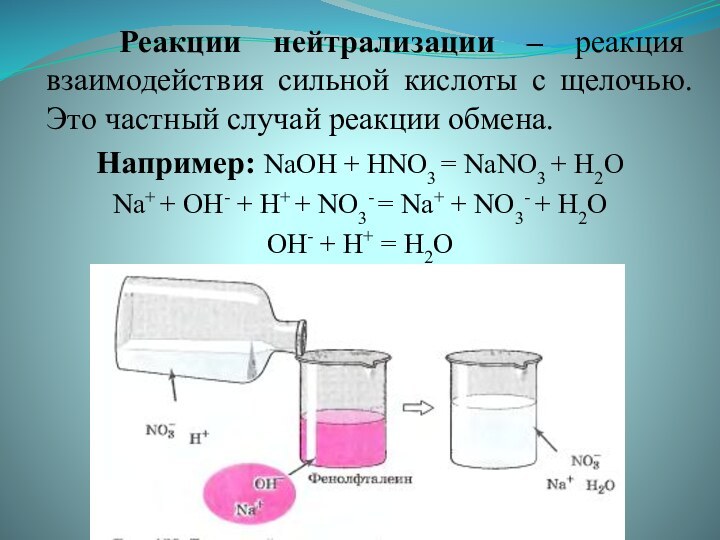
ионные реакции;
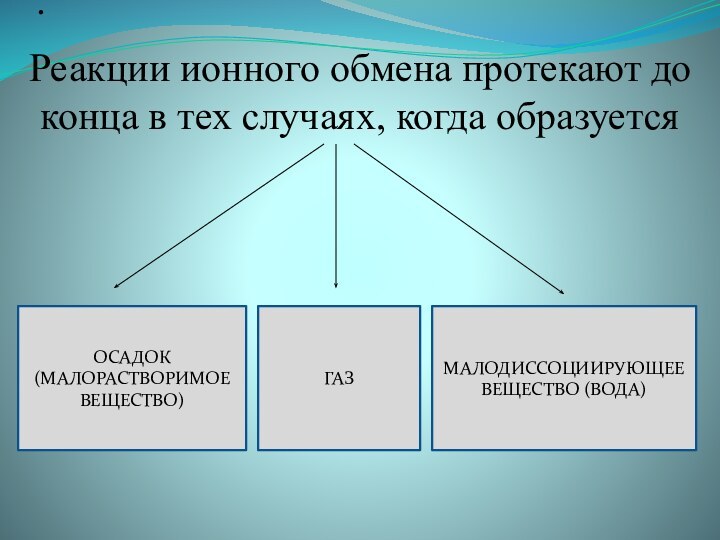
2)рассмотреть случаи, при которых реакции ионного обмена протекают
до конца;3)продолжить формирование умений составлять уравнения химических реакций;
4)развивать познавательный интерес при выполнении теоретических и практических заданий.