- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Оксиди і їх властивості
Содержание
- 2. Основні відомості:Оксиди – це складні речовини, утворені двома елементами, одним з яких обов'язково є Оксиген.
- 3. Еn Оm Де Е-елемент,n,m-валентністьФормули оксидів:
- 4. Назви оксидів:
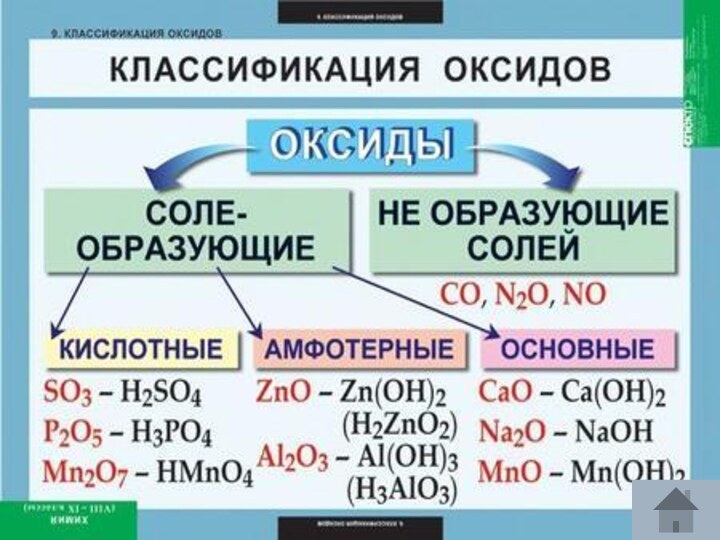
- 5. Класифікація: Са3(РО4)2,ZnSO4,Na2СО3 Класифікація:
- 6. Виділяють декілька основних фізичних властивостей оксидів: 1)
- 7. оксид алюмініюоксид хромуоксид купрумуоксид цинку
- 8. Хімічні властивості основних оксидів:1.Взаємодія з водоюОсновний оксид+вода=основа2.Взаємодія з кислотоюОсновний оксид+кислота=сіль+вода3.Взаємодія з кислотним оксидомОсновний оксид+кислотний оксид=сіль
- 9. Хімічні властивості кислотних оксидів:1.Взаємодія з водоюКислотний оксид+вода=кислота2.Взаємодія з основамиКислотний оксид+основа=сіль+вода3.Взаємодія з основним оксидомОсновний оксид+кислотний оксид=сіль
- 10. Добування:Оксиди можна одержувати різними способами.Безпосереднім сполученням елементів
- 11. Використання:Оксиди багатьох елементів дуже поширені в природі.
- 12. Для отримання скла складають шихту-суміш соди Na2CO3
- 13. Скачать презентацию
- 14. Похожие презентации
Основні відомості:Оксиди – це складні речовини, утворені двома елементами, одним з яких обов'язково є Оксиген.












Слайд 2
Основні відомості:
Оксиди – це складні речовини, утворені двома
елементами, одним з яких обов'язково є Оксиген.
Слайд 6
Виділяють декілька основних фізичних властивостей оксидів:
1) Всі
основні й амфотерні оксиди не мають запаху;
2) Оксиди можуть
бути різного кольору. Наприклад:
a. ZnO, MgO – білий; b. CuO – чорний;
3) Окремі кислотні оксиди є твердими (P2O5, SiO2 і ін.);
4) Виділяють декілька газоподібних кислотних оксидів (CO2, SO2 і ін.)
Фізичні властивості:
Слайд 8
Хімічні властивості основних оксидів:
1.Взаємодія з водою
Основний оксид+вода=основа
2.Взаємодія з
кислотою
Основний оксид+кислота=сіль+вода
3.Взаємодія з кислотним оксидом
Основний оксид+кислотний оксид=сіль
Слайд 9
Хімічні властивості
кислотних оксидів:
1.Взаємодія з водою
Кислотний оксид+вода=кислота
2.Взаємодія з
основами
Кислотний оксид+основа=сіль+вода
3.Взаємодія з основним оксидом
Основний оксид+кислотний оксид=сіль
Слайд 10
Добування:
Оксиди можна одержувати різними способами.
Безпосереднім сполученням елементів з
киснем:
2 Zn + O2 = 2ZnO
4Р + 5О2
= 2Р2О5Окисленням різних сполук киснем:
СН4 + 2О2 = СО2 + 2Н2О
2Н2S + 3О2 = 2SO2 + 2Н2О
Розкладом гідроксидів при нагріванні:
Ca(ОН)2 = СаО + Н2О
2Fe(ОН)3 = Fe2О3 + 3Н2О
Розкладом солей кисневих кислот при нагріванні:
CaCO3 = CaO + СО2
Cu2(ОН)2СО3 = CuO + СО2 + Н2О
Слайд 11
Використання:
Оксиди багатьох елементів дуже поширені в природі. Як
ти гадаєш, чому?
Наприклад, така добре відома сполука, як звичайний
річковий пісок (з деякими домішками) є оксидом з формулою SiO2 – силіцій(IV) оксид (кремнезем). Майже чистим кремнеземом є гірський кришталь.
Цей оксид разом з алюміній оксидом Al2O3 входить до складу глин та багатьох інших мінералів.
З руд, які містять алюміній оксид Al2O3, виплавляють алюміній.
Звичайний наждак – це також алюміній оксид з домішками.
Алюміній оксид з невеликим вмістом різних домішок може бути і коштовним каменем (рубін, сапфір).
Дуже поширені в природі й оксиди Феруму – це різні залізні руди. Україна має великі запаси залізних руд (Криворізьке та Керченське родовища).
До складу повітря входить карбон(IV) оксид СО2 (вуглекислий газ), об’ємна частка якого в повітрі становить 0,3 %.
Однак найпоширенішим оксидом у природі є гідроген оксид Н2О (вода).





























