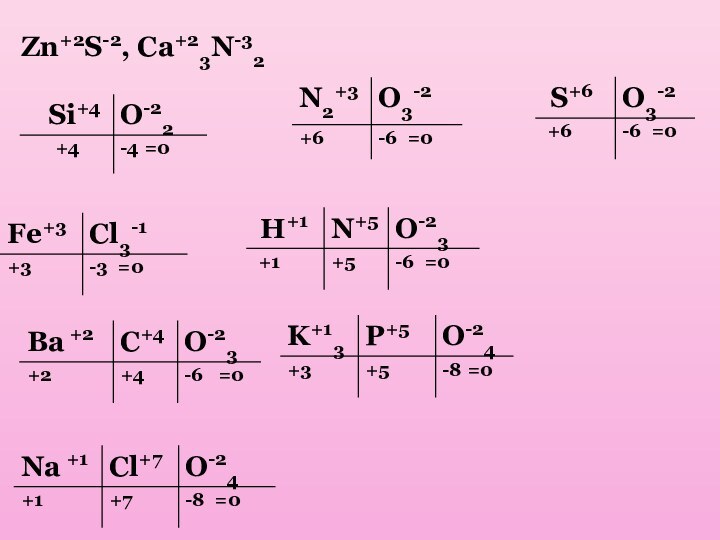степени окисления.
Глава3 – степень окисления в ионе.
Глава4 - составление
формул по степеням окисления.Глава5 – правило креста.
Глава6 – тренировочные задания.
Глава7 – правильные ответы.
Глава8 – проверочная работа, ответы.
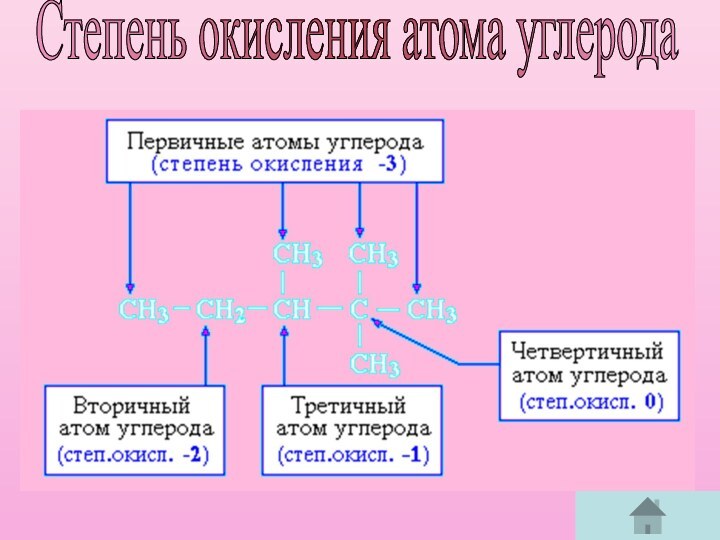
Глава9 – степень окисления углерода.