атомов химических элементов углерода и водорода.
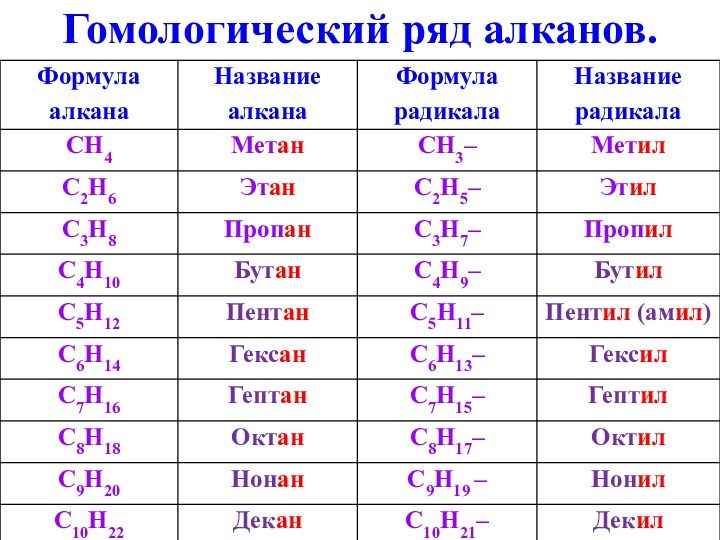
С1 – С4 –
газы.С5 – С15 – жидкости.
С16 –… – твердые вещества (парафины).
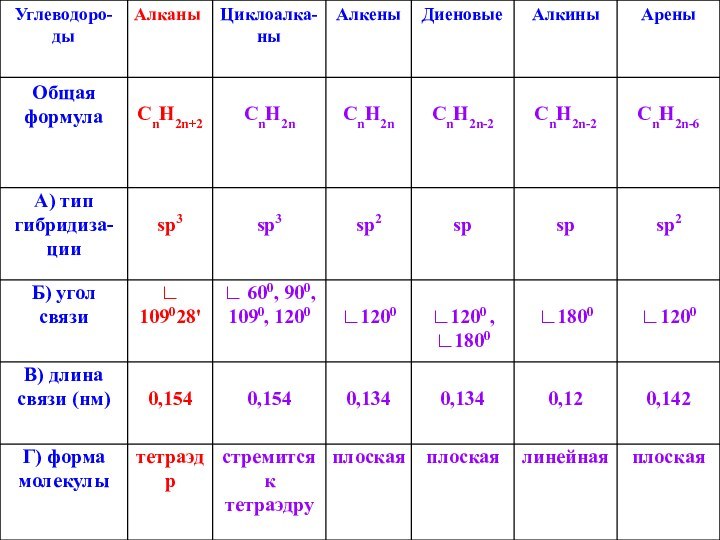
В молекулах алканов только одинарные (ϭ – связи).
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть



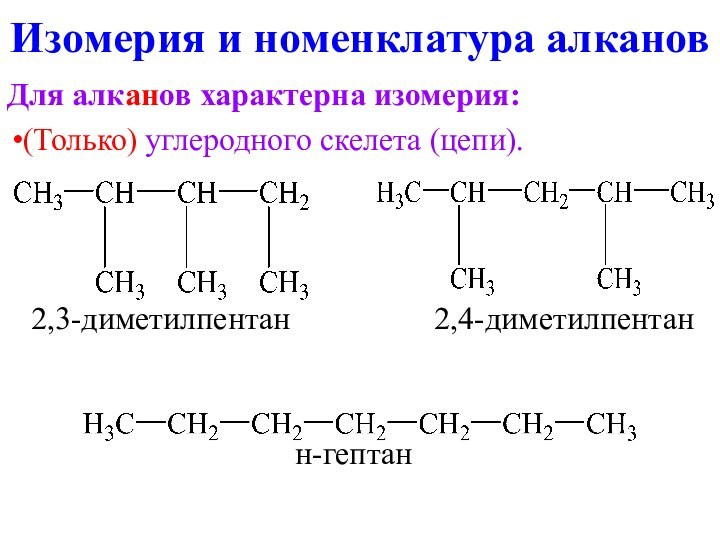
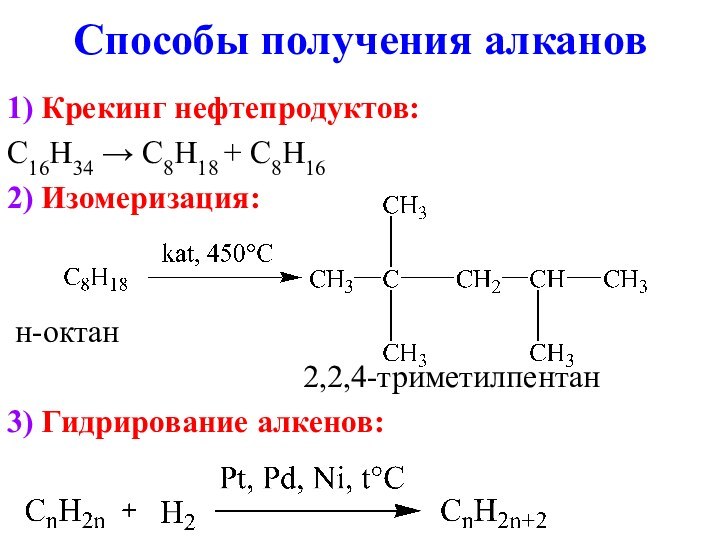

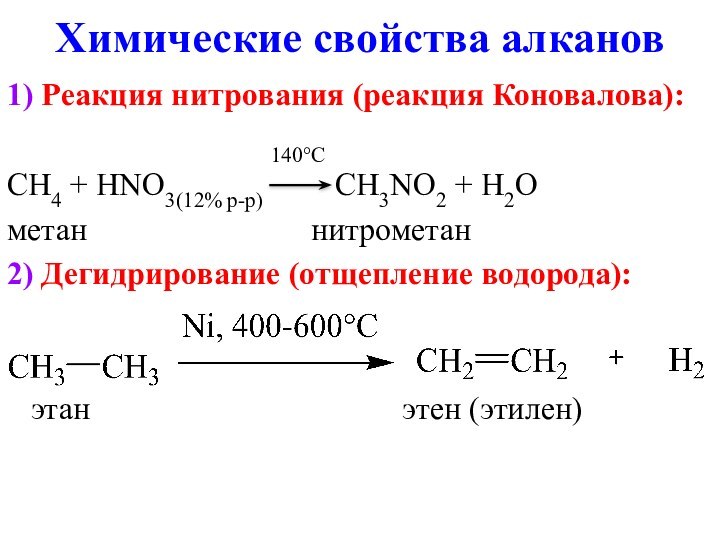


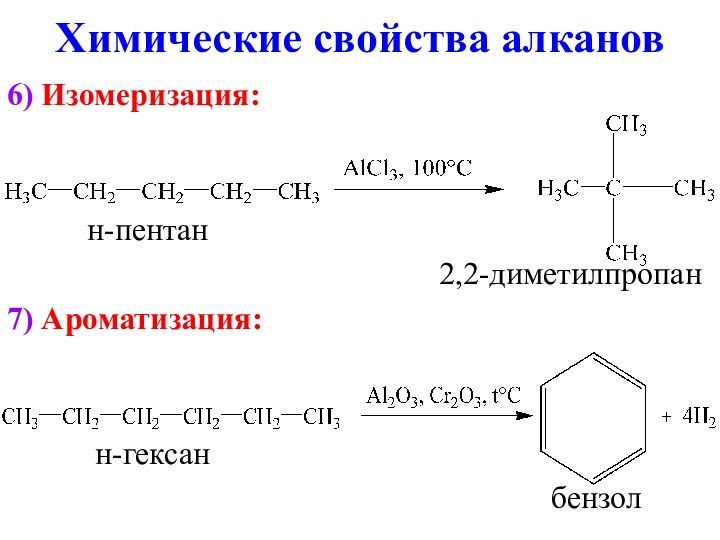

Химические свойства алканов
Химические свойства алканов