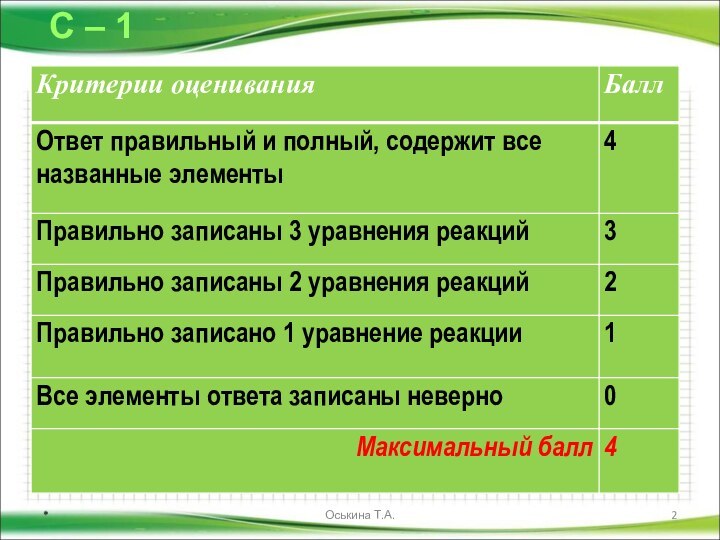
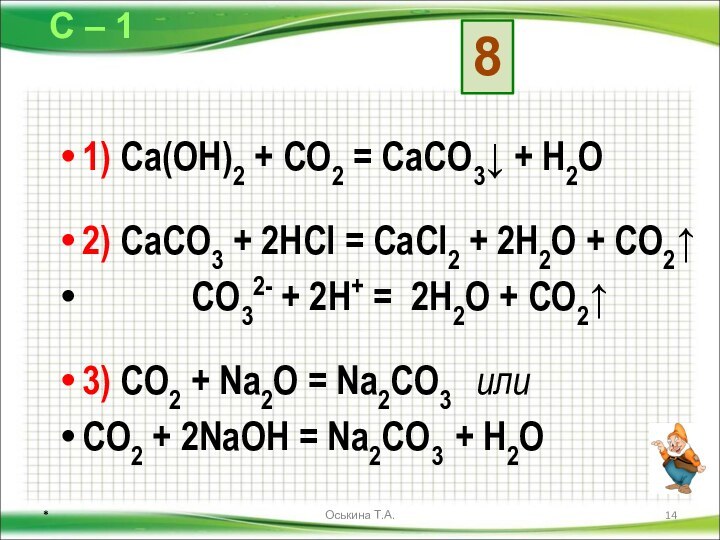
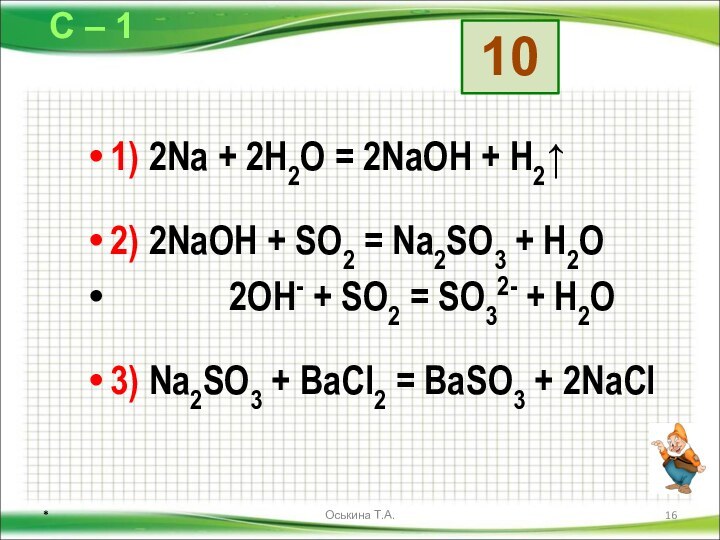
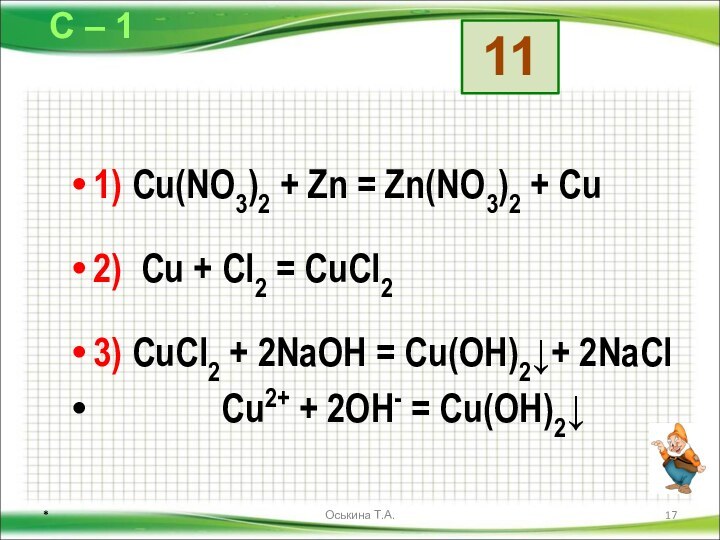
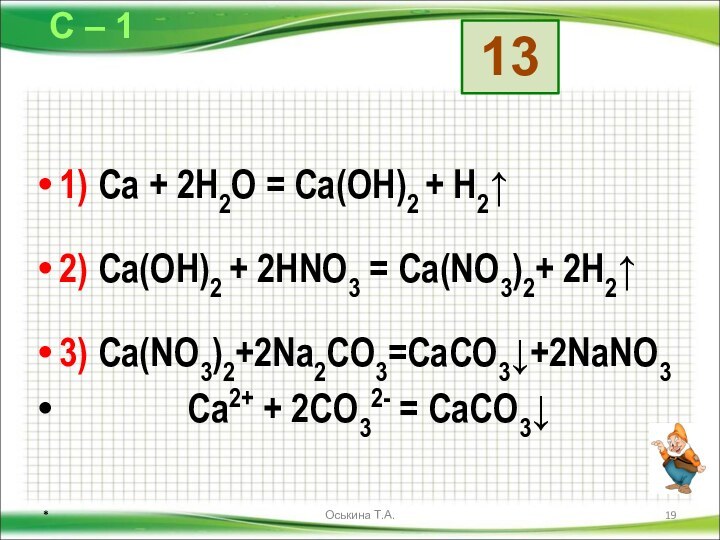
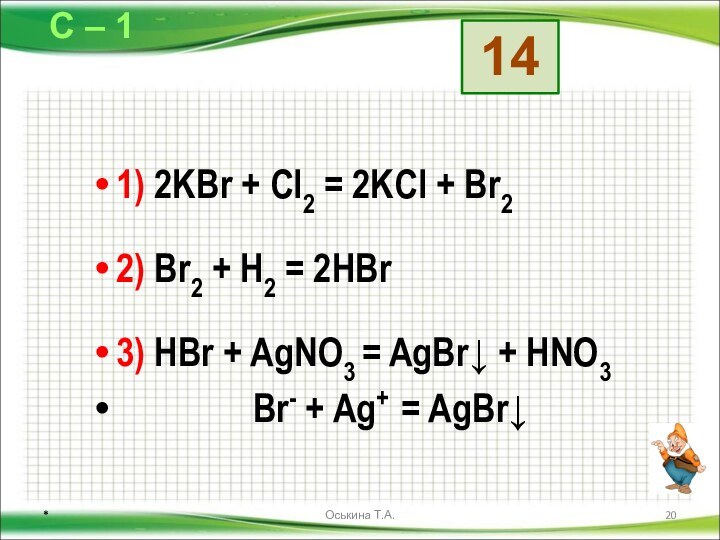
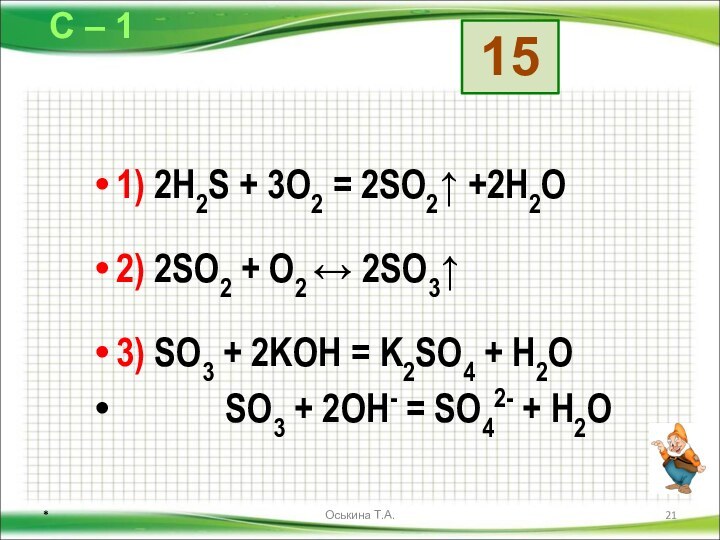
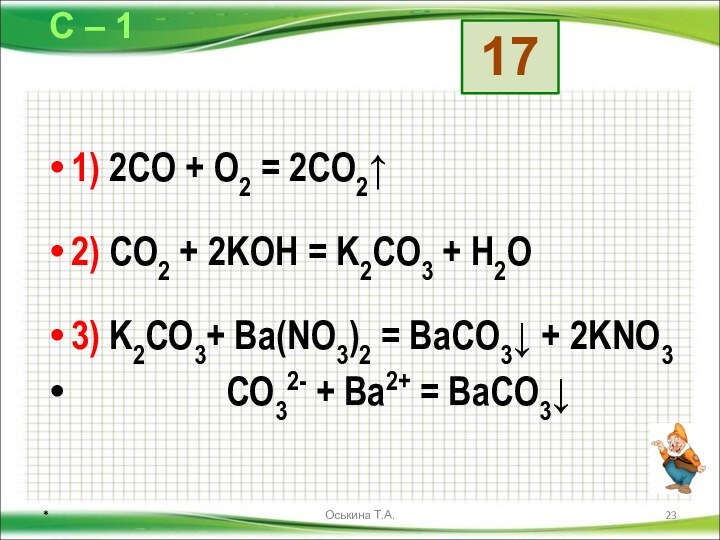
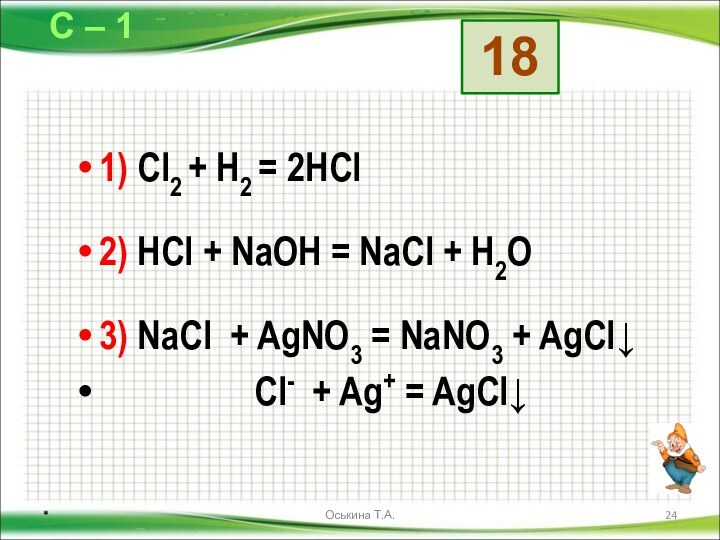
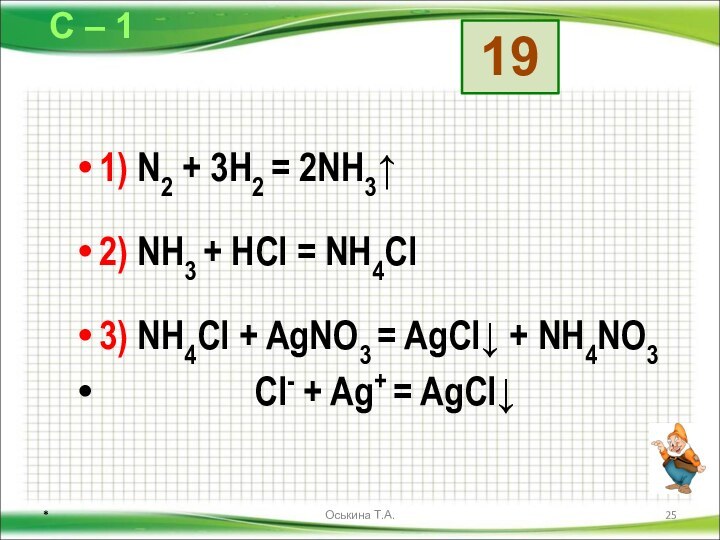
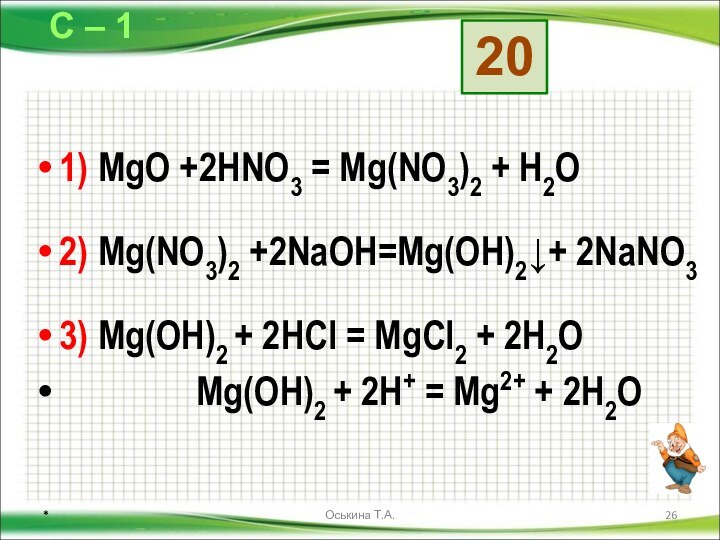
Даны схемы превращений. Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения в каждой цепочке составьте сокращённое ионное уравнение реакции.
*
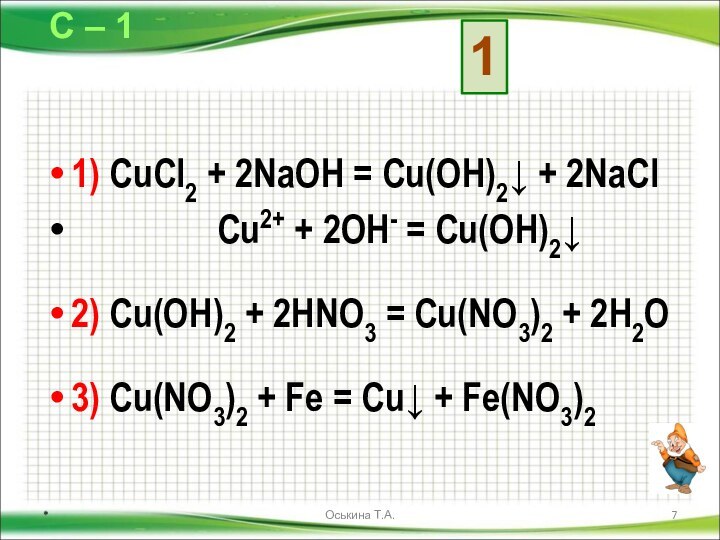
CuCl2 → X → Cu(NO3)2 → Cu
1)
Fe2(SO4)3 →X → Fe2O3 → Fe
2)
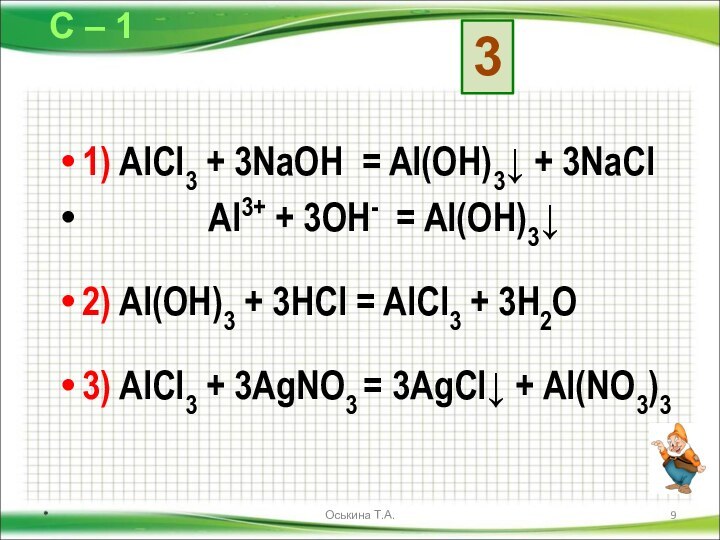
AlCl3 → Al(OH)3 → X → AgCl
3)
С – 1
Na2SO3 → X → SO3 → BaSO4
4)
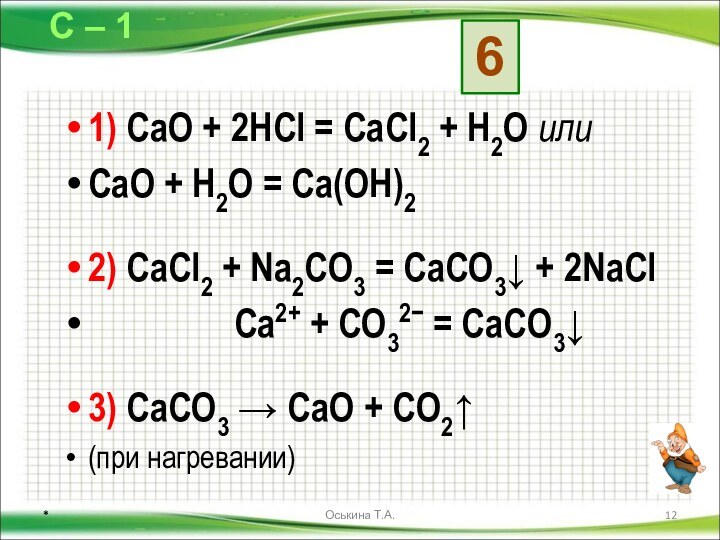
5)
Fe(OH)2 → FeCl2 → X → Fe(OH)3
Р
Е
Ш
Е
Н
И
Я
Оськина Т.А.