Слайд 2
Определение ВОЗ
Нозокомиальные инфекции ( nosocomium - лат.
nosokomeo - греч. - больница)
любое инфекционное заболевание, которое возникает
У госпитализированных больных после 48 часов пребывания в стационаре
без признаков инфекции при поступлении
если пациент не находился в инкубационном периоде
Инфекция, непосредственно связанная с предыдущей госпитализацией или обращением в стационар
Любая инфекция у сотрудника, связанная с его работой в стационаре
Слайд 3
Факторы риска НИ
Длительность нахождения в ОРИТ
Широкое использование антибиотиков
Тяжесть
состояния (APACHE II > 15)
Возраст >60 лет
Сопутствующие заболевания (ХОБЛ,
СД)
Инвазивные диагностические и лечебные процедуры
Использование антисекреторных средств
Переливание компонентов крови
Слайд 4
Vincent J-L et al, 1995
Структура НИ
EPIC
n=2064 (1417 ОРИТ, 10038 пациентов)
Колонизация
85%
инфекции 25,6%
пневмония 46,9%
МВП 17,6%
кровотока 12%
ран 6,9%
ЛОР 5,1%
КиМТ 4,8%
ЖКТ 4,5%
Бактериемия: CNS, S. aureus, Enterococcus spp
Пневмония: P. aerug., S. aureus, Enterobacter spp., K. pneum.
Хир.инфекция: Enterococcus spp., CNS, S. aureus, P. aerug.
Инф. МВП: E. coli, C. albicans, Enterococcus spp, P. aerug.
Слайд 5
При планировании антибиотикотерапии
необходимо учитывать:
Локализацию очага инфекции
Условия
возникновения
(Внебольничная, Нозокомиальная)
Тяжесть инфекции
На основании локального мониторинга антибиотикорезистентности
С учетом
современных тенденций антибиотикорезистентности
Слайд 6
Отечественные исследования
антибиотикорезистентности
РЕЗОРТ - многоцентровое проспективное микробиологическое исследование
резистентности к антимикробным препаратам бактериальных возбудителей нозокомиальных инфекций в отделениях реанимации
и интенсивной терапии России
CASCAT - многоцентровое клинико-микробиологическое исследование катетер-ассоциированных инфекций кровотока в отделениях реанимации и интенсивной терапии
СтЭнт - изучение антибиотикорезистентности грам(+) микроорганизмов: S. aureus и Enterococcus spp.
NPRS - изучение распространения и резистентности грам(-) возбудителей нозокомиальных инфекций в отделениях интенсивной терапии.
РЕВАНш - Многоцентровое исследование резистентности к антибиотикам бактериальных возбудителей нозокомиальных инфекций в отделениях с интенсивным использованием антибиотиков в стационарах России
Слайд 7
Структура возбудителей НИ в ОРИТ
(РЕВАНш 2006 г)
Enterobacteriaceae
32,0%
P. aeruginosa 27,3%
Staphylococcus spp.
18,8%
Acinetobacter baumannii 10,4%
Enterococcus spp. 5,7%
Stenotrophomonas maltophilia 1,5%
Другие 4,3%
Слайд 8
Изменение структуры Гр (-) инфекций в ОРИТ
1996 год
P.
aeruginosa
E. coli
Klebsiella
P. mirabilis
Enterobacter
Acinetobacter baumannii
2006 год
P. aeruginosa
Acinetobacter
Klebsiella
E.
coli
Enterobacter
Stenotrophomonas maltophilia
Burkholderia cepacia
Слайд 9
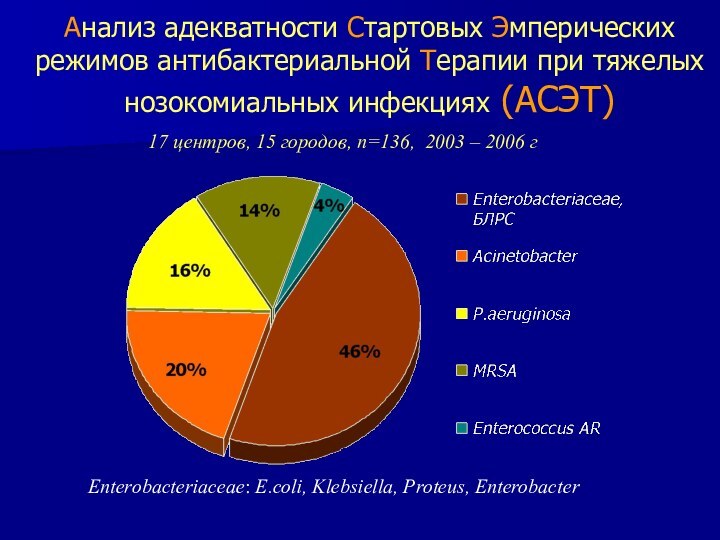
Анализ адекватности Стартовых Эмперических режимов антибактериальной Терапии при
тяжелых нозокомиальных инфекциях (АСЭТ)
17 центров, 15 городов, n=136, 2003
– 2006 г
Enterobacteriaceae: E.coli, Klebsiella, Proteus, Enterobacter
Слайд 10
Бета-лактамазы
Цеф I Цеф II Цеф III Цеф IV Карб
Класс С + + + - -
Класс А
Широкий спектр + - - - -
Расширенный спектр + + + + -
NmcA, Sme, Imi - - - - +
Класс D + + + + -
Класс В + + + + +
Слайд 11
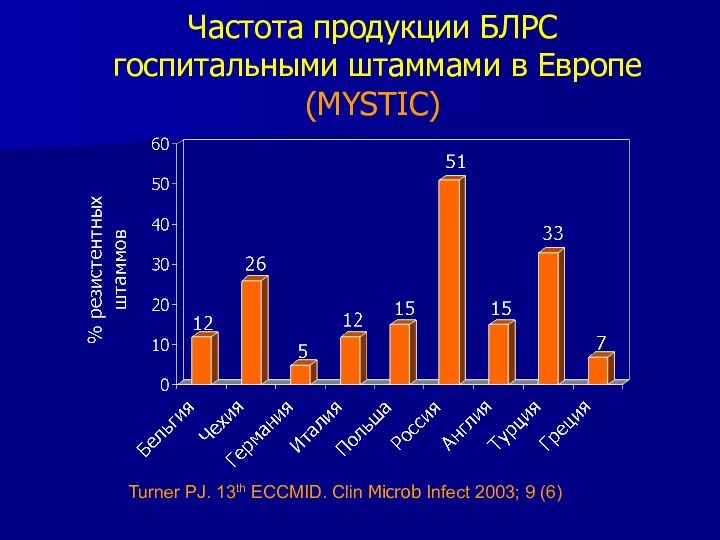
Частота продукции БЛРС
госпитальными штаммами в Европе (MYSTIC)
Turner PJ. 13th ECCMID.
Clin Microb Infect 2003; 9 (6)
Слайд 12
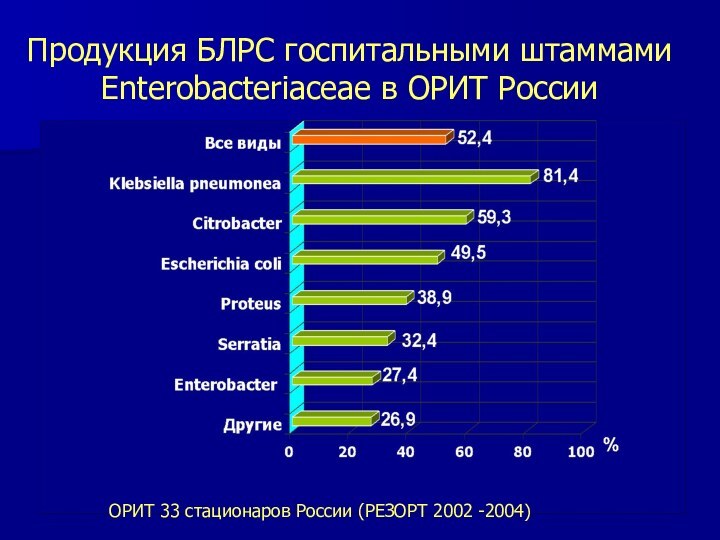
Продукция БЛРС госпитальными штаммами Enterobacteriaceae в ОРИТ России
ОРИТ
33 стационаров России (РЕЗОРТ 2002 -2004)
Слайд 13
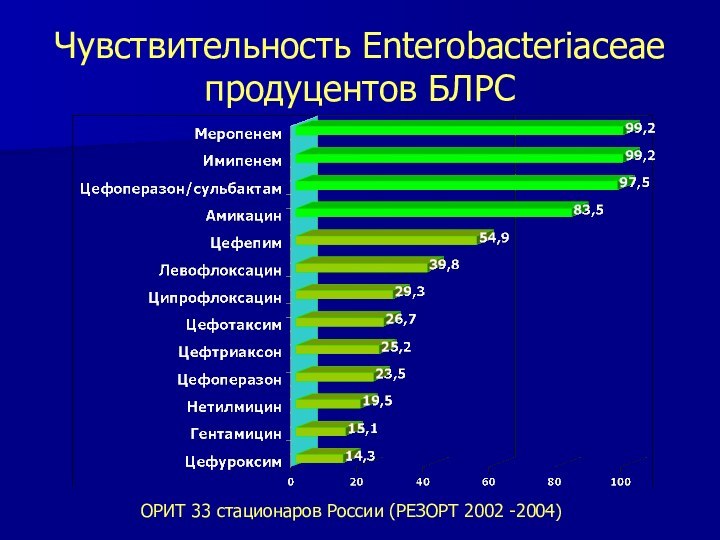
Чувствительность Enterobacteriaceae продуцентов БЛРС
ОРИТ 33 стационаров России (РЕЗОРТ
2002 -2004)
Слайд 14
Косвенные признаки:
Госпитальный штамм Klebsiella spp. или E.coli
Устойчивость in
vitro хотя бы к одному из Цефалоспоринов III
Увеличение зоны
подавления роста в присутствии клавуланата
Результат: Klebsiella pneumoniae
Ампициллин R
Амоксициллин/клавуланат R
Цефтриаксон S
Цефотаксим S 1-й признак
Цефтазидим R
Цефепим S
Цефперазон/сульбактам S
Меропенем R
Гентамицин R
Амикацин R
Ципрофлоксацин R
Цефтазидим + А/КК S 2-й признак
Клиническая интерпретация БЛРС
(Klebsiella spp., E. coli, P. mirabilis)
Слайд 15
Класс В – металлобеталактамазы
Инактивируют все бета-лактамные антибиотики
Ассоциированная
устойчивость
к аминогликозидам, фторхинолонам
Встречается преимущественно Pseudomonas spp.,
может быть
у любого представителя Enterobacteriaceae
Сохраняют активность
Азтреонам
Полимиксин
Слайд 16
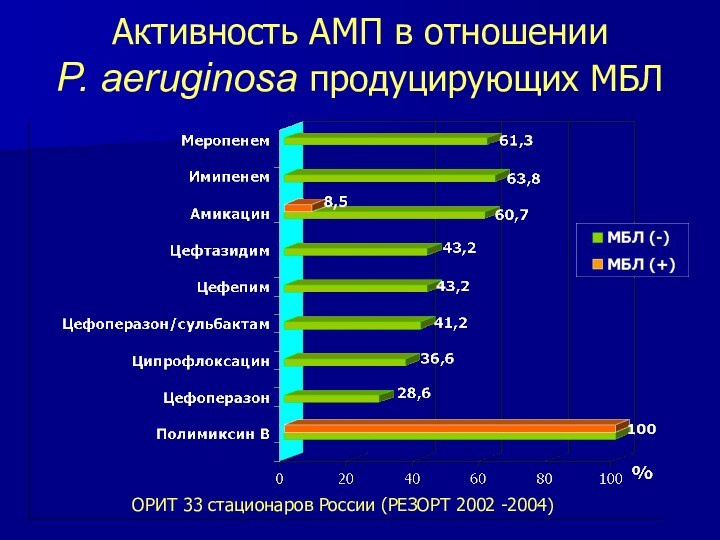
Активность АМП в отношении
P. aeruginosa продуцирующих МБЛ
ОРИТ
33 стационаров России (РЕЗОРТ 2002 -2004)
Слайд 17
Неферментирующие Гр (-) бактерии
(РЕВАНш 2006 г)
P. aeruginosa
27,3 %
Acinetobacter 10,4%
Stenotrophomonas
maltophilia 1,5%
Другие 5,7%
Слайд 18
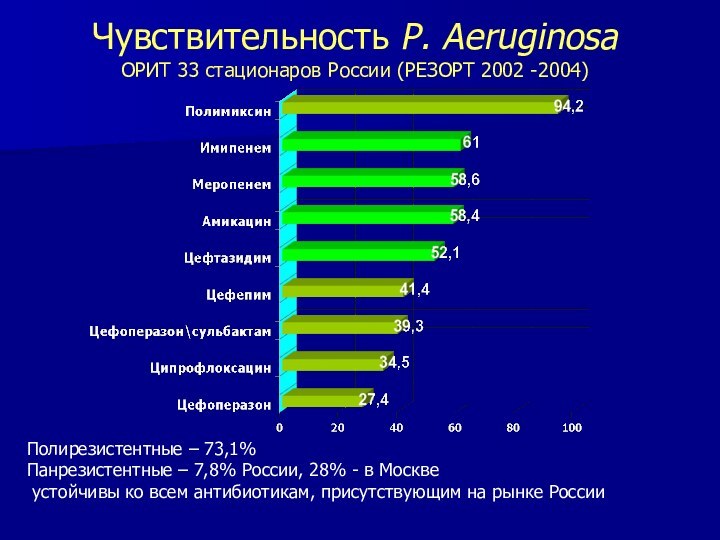
Чувствительность P. Aeruginosa
ОРИТ 33 стационаров России (РЕЗОРТ 2002
-2004)
Полирезистентные – 73,1%
Панрезистентные – 7,8% России, 28% - в
Москве
устойчивы ко всем антибиотикам, присутствующим на рынке России
Слайд 19
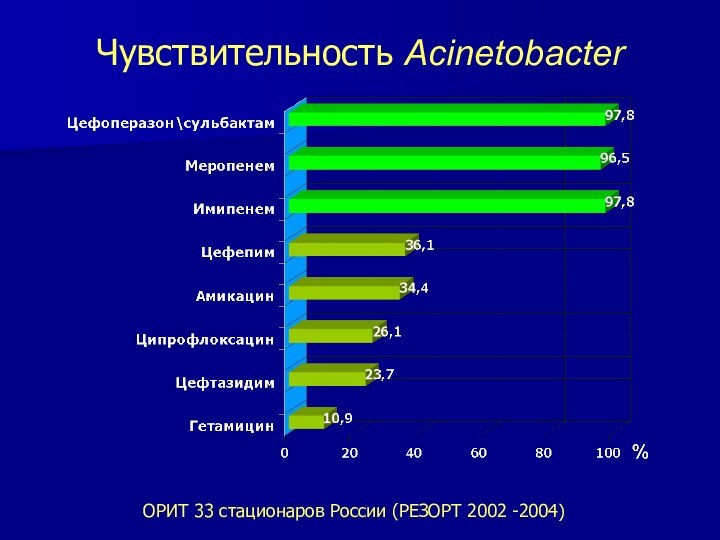
Чувствительность Acinetobacter
ОРИТ 33 стационаров России (РЕЗОРТ 2002
-2004)
Слайд 20
Другие неферментирующие ГР(-) бактерии
Burkholderia cepacia
• Режимы терапии недостаточно
изучены.
Меропенем, цефепим, пиперациллин, ко-тримоксазол, хлорамфеникол.
Приобретенная резистентность: достаточно часто встречаются
штаммы, устойчивые ко всем приведенным препаратам.
Stenotrophomonas maltophilia
• Препарат выбора: Ко-тримоксазол
Альтернативные средства:
тикарциллин/клавуланат,
цефтазидим, цефоперазон/сульбактам, моксифлоксацин.
однако режимы использования перечисленных препаратов недостаточно обоснованы.
Приобретенная резистентность: Ко всем альтернативным препаратам достаточно часто встречается устойчивость.
Слайд 21
Резистентный стафилококк
Оксациллин
Цефазолин
Цефтриаксон
Имипинем
Гентамицин
Клиндомицин
Ванкомицин
Линезолид
R
R
S R
S
R
R
S R
S
S
Methicillin (Oxacillin)
Resistant
Staphylococcus
Aureus
Механизм устойчивости: модификация мишени действия всех бета-лактамных антибиотиков – пенициллинсвязывающего белка
MRSA – устойчивы ко всем беталактамным антибиотикам
Ассоциированная устойчивость
Аминогликозиды
Линкозамины
Макролиды
Тетрациклины
Слайд 22
Распространение МRSA в России при нозокомиальных инфекциях
Диапазон В среднем
1995
– 1996 0 – 40% 9.5%
[С.В. Сидоренко]
2000 – 2001 0 – 89.5% 33.5%
[А.В. Дехнич]
2004 – Москва 64.9%
[Сидоренко и соавт]
В настоящее время в ОРИТ России – 41%
При выделении из крови – 63%
Слайд 23
Лечение стафилококковых инфекций
MSSA
Наиболее эффективны
Оксациллин
Цефазолин
Равноэффективны
Цефуроксим
Цефепим
Клиндамицин
Амоксициллин/Клавуланат
Тиенам
MRSA
Доказанная эффективность
Ванкомицин
Линезолид
Мупироцин (местно)
Предполагаемая эффективность
Ципрофлоксацин
Ко-тримоксазол
Рифампицин
Фузидин
Ванкомицин менее эффективен против MSSA Летальность при лечении MSSA-бактериемии
Клоксациклин
0/10
Ванкомицин 8/17 (47%)
Gonzalez C. e.a.CID 1999;
Слайд 24
Антибиотикорезистентность энтерококков
Распространение ванкомицин- резистентных энтерококков (VRE)
Северная Америка, Европа
- 27.5%
Россия – 3,8%
Первый штамм – 2002 г,
К
настоящему времени выделено более 250 штаммов
VRE не выявляются обычными микробиологическими методами
Доказанная эффективность
Ампициллин
Ванкомицин
Линезолид
Предполагаемая эффективность
Левофлоксацин
Моксифлоксацин
А/С, А/КК
Тиенам
Слайд 25
Микробиологическая диагностика: к чему следует
быть готовым?
Стафилококки со сниженной чувствительностью к ванкомицину (VISA)
Ванкомицин-резистентные энтерококки
Энтеробактерии,
резистентные в карбапенемам – МБЛ
Панрезистентные неферментирующие бактерии
Слайд 26
Сдерживание резистентности
Контроль и рационализация использования антибиотиков в стационаре
Эпидемиологический
контроль
Новые антибиотики
Слайд 27
Контроль антибиотикорезистентности
Максимальная терапия с учетом разумной достаточности
Де-эскалация
Исключить профилактическое
лечение
Не лечить колонизацию
Сокращение длительности курсов АБ терапии
Интраоперационная профилактика
в хирургии
Своевременное удаление инородных тел (катетеры)
Контроль переноса инфекций, эпид. мероприятия
Фармакодинамическое обоснование режимов дозирования
Формуляр и химиотерапевтическая служба
Мониторинг возбудителей и их резистентности в конкретном отделении
Реальное взаимодействие микробиологической службы и клиницистов
Слайд 28
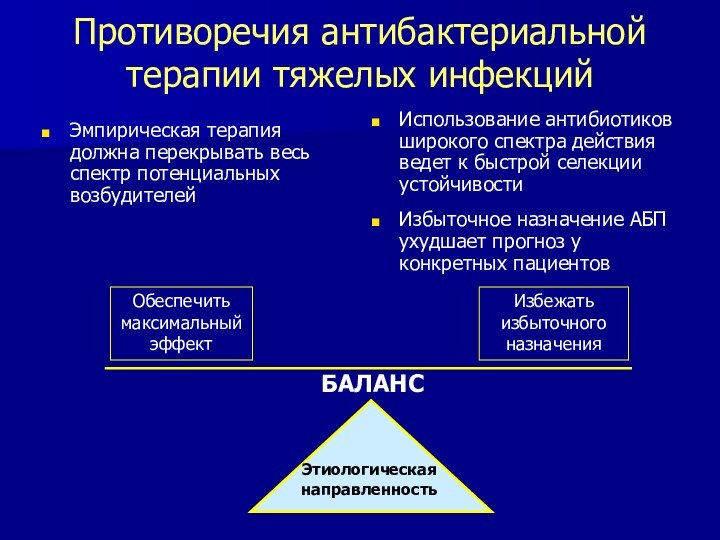
Противоречия антибактериальной терапии тяжелых инфекций
Эмпирическая терапия должна перекрывать
весь спектр потенциальных возбудителей
Использование антибиотиков широкого спектра действия ведет
к быстрой селекции устойчивости
Избыточное назначение АБП ухудшает прогноз у конкретных пациентов
Обеспечить
максимальный
эффект
Избежать
избыточного
назначения
БАЛАНС
Этиологическая
направленность
Слайд 29
Практические рекомендации по диагностике и антибактериальной терапии нозокомиальных
инфекций (Россия)
Нозокомиальная пневмония в хирургии 2004 г.
Сепсис 2005 г.
Нозокомиальная
пневмония 2005 г.
Перитонит 2006 г.