Слайд 2
ВОЗБУДИТЕЛИ ВНЕБОЛЬНИЧНЫХ ИНФЕКЦИЙ
Streptococcus pneumonia. Резистентность пневмококков к бензилпенициллину
-3-4%, к макролидам - 2-4%, тетрациклину - 56-63%. Почти
все пневмококки сохраняют чувствительность к цефалоспоринам, защищенным аминопенициллинам.
Streptococcus pyogenes. Высокая чувствительность к В - лактамным антибиотикам, резистентность к макролидам 8-11%, к тетрациклину более 60%.
Hemophilus influenzae. Резистентность к ампициллину 11-14%, защищенным аминопенициллинам 0,5-0,7%, хлорамфениколу 3-9%, макролидам 14-28% (кроме азитромицина ).
Moraxella catarralis - большинство штаммов продуцирует В- лактамазы, резистентность к бензилпенициллину 77-89%, ампициллину 39-68%, эритромицину 19-27%.
Слайд 3
ВОЗБУДИТЕЛИ ВНЕБОЛЬНИЧНЫХ ИНФЕКЦИЙ
Escherichia coli. Резистентность к пиперациллину -
44%, ампициллину 40%, гентамицину 13%, амикацину 1%, имипенему 0%,
ципрофлоксацину 1%, норфлоксацину 3%, ко-амоксиклаву 27%, пиперациллину+тазобактаму 11%, цефуроксиму 19%, цефотаксиму 6%, цефтриаксону 4%, цефтазидиму3%, цефепиму 1%
Spigella flexneri- резистентность к ампициллину 95-98%, уназину 95%, хлорамфениколу 93%, ципрофлоксацину 1-4%, налидиксовой кислоте 1-2%, цефтриаксону 1-2%.
Shigella zonne - резистентность к ампициллину 8-34%, уназину 8-28%, цефтриаксону 0%, ципрофлоксацину 0%, хлорамфениколу 33-39%.
Salmonella sp.p.-резистентность к ампициллину 6%, уназину 3-4%, цефотаксиму 0%, тетрациклину 10%, хлорамфениколу 10%, налидиксовой кислоте 3%.
Слайд 4
ВОЗБУДИТЕЛИ ГОСПИТАЛЬНЫХ ИНФЕКЦИЙ
S.aureus и коагулазонегативные стафилококки.
Устойчивость к оксациллину встречается у коагулазонегативных стафилококков в
66%, у S. aureus в 40%. Все резистентные к оксациллину стафилококки чувствительны к ванкомицину и тейкопланину. Большая часть MRSA чувствительны к фузидиевой кислоте и рифампицину.
Enterococcus spp . E. Faecalis - резистентность к ампициллину 14%, гентамицину 25%, ванкомицину 3-8%, хлорамфениколу 39%, рифампицину 88%.
Е. faecium- резистентность к ампициллину 77%,гентамицину 64%, ванкомицину 6-9%, хлорамфениколу 54%.
Klebsiella pneumoniae - резистентность к тазоцину 17%, ко-амоксиклаву 50%, цефуроксиму 52%, цефотаксиму 33%, цефтриаксону 32%, цефепиму 16%, имипинему 0%, гентамицину 58%, амикацину 0%, ципрофлоксацину 2%.
Слайд 5
ВОЗБУДИТЕЛИ ГОСПИТАЛЬНЫХ ИНФЕКЦИЙ
Proteus s.p.p. - резистентность к тазоцину
1%, цефтриаксону 10%, цефтазидиму 3%, цефепиму 2%, имипинему 0%,
ципрофлоксацину 15%, амикацину 1%, гентамицину 58%, ко-амоксиклаву 50%.
Enterobacter s.p.p.- резистентность к тазоцину 63%, цефуроксиму 82%, цефотаксиму 60%, цефтриаксону 57%, цефтазидиму 55%, цефепиму 5-11%, имипинему 0%, гентамицину 42%, амикацину 4%, ципрофлоксацину 5%.
Acinetobacter s.p.p.- резистентность к тазоцину 82%, ко-амоксиклаву 73-75%, цефотаксиму 85%, цефепиму 13-27%, имипинему 0%, гентамицину 91%, амикацину 7%, ципрофлоксацину 53%, меропенему 0 %.
Pseudomonas aerugenosa - резистентность к тазоцину 40%, ко-амоксиклаву 100%, цефтриаксону 95-98%, цефтазидиму 11%, цефепиму 3-4%, имипинему 10-11%, меропенему 6-8%, гентамицину 75-77%, амикацину 7%, ципрофлоксацину 15%.
Слайд 6
ПУТИ ПРЕОДОЛЕНИЯ АНТИБАКТЕРИАЛЬНОЙ
РЕЗИСТЕНТНОСТИ В ПЕДИАТРИИ
Синтез антибиотиков новых
химических структур, не подверженных разрушению бета-лактамазами.
Поиск новых бета-лактамных
антибиотиков, устойчивых к гидролитическому действию бета-лактамаз.
Синтез ингибиторов бета-лактамаз.
Слайд 7
АНТИБИОТИКИ
вещества, избирательно подавляющие жизнедеятельность микроорганизмов.
Это действие определяется специфичностью по отношению к возбудителям инфекционного
процесса.
Слайд 8
КЛАССИФИКАЦИЯ
АНТИМИКРОБНЫХ ПРЕПАРАТОВ
ПО МЕХАНИЗМУ ДЕЙСТВИЯ
Нарушение синтеза клеточной
стенки (пенициллины, цефалоспорины, гликопептиды),
Нарушение структуры клеточных мембран (полимиксины),
Нарушение метаболизма
фолиевой кислоты (рифампицин, сульфаниламиды, триметоприм),
Ингибирование синтеза белка в рибосомах (обратимо-макролиды, тетрациклины, хлорамфеникол, фузидин, линкосамиды), (необратимо-аминогликозиды),
Нарушение репликации ДНК - ингибиторы ДНК - гиразы (хинолоны и фторхинолоны),
Нарушение синтеза ДНК (нитрофураны, производные хиноксалина, нитроимидазола и 8-оксихинолина).
Слайд 9
КЛАССИФИКАЦИЯ
АНТИМИКРОБНЫХ ПРЕПАРАТОВ
Бета-лактамы
ПЕНИЦИЛЛИНЫ
ЦЕФАЛОСПОРИНЫ
КАРБАПЕНЕМЫ
МОНОБАКТАМЫ
Слайд 10
КЛАССИФИКАЦИЯ
АНТИМИКРОБНЫХ ПРЕПАРАТОВ
КОМБИНИРОВАННЫЕ ПРЕПАРАТЫ –
амоксициллин + клавулановая
кислота
тикарциллин + клавулановая кислота
ампициллин + сульбактам
цефаперазон + сульбактам
пиперациллин +
тазобактам
АМИНОГЛИКОЗИДЫ - амикацин, гентамицин, нетилмицин, тобрамицин, сизомицин
ТЕТРАЦИКЛИНЫ - доксициклин, тетрациклин
МАКРОЛИДЫ - азитромицин, кларитромицин, мидекамицин, рокситромицин, спирамицин, эритромицин, джосамицин.
ЛИНКОСАМИДЫ - линкомицин, клиндамицин
ГЛИКОПЕПТИДЫ - ванкомицин. тейкопланин
РИФАМПИЦИНЫ - рифампицин
ПОЛИМИКСИНЫ - полимиксин В, полимиксин Е
Слайд 11
КЛАССИФИКАЦИЯ
АНТИМИКРОБНЫХ ПРЕПАРАТОВ
ИНГИБИТОРЫ ДНК –ГИРАЗЫ
Хинолоны - налидиксовая кислота,
пипемидиевая кислота
Фторхинолоны - норфлоксацин, пефлоксацин, ципрофлоксацин, офлоксацин, помефлоксацин, спарфлоксацин,
левофлоксацин, моксифлоксацин
ОКСАЗОЛИДИНОНЫ -линезолид
НИТРОФУРАНЫ - фурагин, фуразолидон, нитрофурантоин
НИТРОМИДАЗОЛЫ - метронидазол, тинидазол, орнидазол
ПРОИЗВОДНЫЕ ХИНОКСАЛИНА - диоксидин, хиноксидин
СУЛЬФАНИЛАМИДЫ С ТРИМЕТОПРИМОМ - ко-тримоксазол
Слайд 12
КЛАССИФИКАЦИЯ
АНТИМИКРОБНЫХ ПРЕПАРАТОВ
ДРУГИЕ АНТИМИКРОБНЫЕ ПРЕПАРАТЫ - хлорамфеникол, фузидиевая
кислота, спектиномицин, фосфомицин
ПРОТИВОГРИБКОВЫЕ ПРЕПАРАТЫ - амфотерицин В, интраконазол, кетоконазол,
клотримазол, миконазол, нистатин, флуконазол, флуцитозин
ПРОТИВОТУБЕРКУЛЕЗНЫЕ СРЕДСТВА - изониазид, метазид. Парааминосалициловая кислота (ПАСК), пиперазинамид, рифабутин, рифампицин, стрептомицин, фтивазид, циклосерин, этамбутол, этионамид.
Слайд 13
Классификация пенициллинов
Природные:
Бензилпенициллин (пенициллин), натриевая и калиевая соли
Феноксиметилпенициллин
Бициллин
Слайд 14
Классификация пенициллинов
Полусинтетические:
Изоксазолилпенициллины Оксациллин
Аминопенициллины Ампициллин, Амоксициллин
Карбоксипенициллины Карбенициллин,Тикарциллин
Уреидопенициллины Азлоциллин, Пиперациллин
ингибиторозащищенные пенициллины
Амоксициллин/клавуланат
Ампициллин/сульбактам
Тикарциллин/клавуланат
Пиперациллин/тазобактам
Слайд 15
Механизм действия
Пенициллины (и все другие β-лактамы) обладают
бактерицидным эффектом.
Мишень действия - пенициллиносвязывающие белки бактерий, которые
выполняют роль ферментов на завершающем этапе синтеза клеточной стенки бактерий. Блокирование синтеза пептидогликана приводит к гибели бактерии.
Слайд 16
Спектр активности
Грамположительные бактерии
Streptococcus spp.
Staphylococcus spp.
Bacillus spp.
в меньшей
степени - Enterococcus spp.
листерии (L.monocytogenes),
большинство коринебактерий (C.diphtheriae)
Грамотрицательные бактерии
Neisseria spp., P.multocida и H.ducreyi.
Большинство анаэробных бактерий (актиномицеты, Peptostreptococcus spp., Clostridium spp.)
спирохеты (Treponema, Borrelia, Leptospira)
Слайд 17
Фармакокинетика
Бензилпенициллин, карбоксипенициллины и уреидопенициллины применяются только парентерально. Феноксиметилпенициллин,
оксациллин и аминопенициллины - внутрь.
Наилучшим всасыванием в ЖКТ характеризуется
амоксициллин (75% и более), еще лучше (93%) имеют специальные растворимые таблетки (флемоксин солютаб). Хуже всасываются ампициллин (35-40%) и оксациллин (25-30%).
Всасывание ингибитора β-лактамаз клавуланата -75% и под влиянием пищи несколько увеличивается. Большинство пенициллинов экскретируется почками.
Их период полувыведения -около 1 ч и значительно возрастает при почечной недостаточности. Оксациллин и уреидопенициллины имеют двойной путь выведения - почками и печенью.
Слайд 18
Нежелательные реакции
Аллергические реакции: крапивница, сыпь, отек Квинке, анафилактический
шок
ЦНС: головная боль, тремор, судороги , психические расстройства
.
ЖКТ: боль в животе, тошнота, рвота, диарея, псевдомембранозный колит.
Нарушения электролитного баланса: гиперкалиемия , гипернатриемия
Местные реакции: инфильтрат при в/м введении, флебит - при в/в.
Печень: повышение активности трансаминаз.
Гематологические реакции:анемия, нейтропения, тромбоцитопатия.
Почки: транзиторная гематурия у детей.
Сосудистые осложнения: синдром Онэ - ишемия и гангрена конечностей при введении в артерию, синдром Николау - эмболия сосудов - при введении в вену.
Другие: неаллергическая сыпь, которая может исчезнуть без отмены препарата, кандидоз.
Слайд 19
Классификация хинолонов
I поколение:
Налидиксовая кислота
Оксолиновая кислота
Пипемидовая (пипемидиевая) кислота
II
поколение:
Ломефлоксацин
Норфлоксацин
Офлоксацин
Пефлоксацин
Ципрофлоксацин
III поколение:
Левофлоксацин
Спарфлоксацин
IV поколение:
Моксифлоксацин
Слайд 20
Механизм действия хинолонов
Оказывают бактерицидный эффект. Ингибируя два жизненно
важных фермента микробной клетки - ДНК-гиразу и топоизомеразу IV, нарушают
синтез ДНК.
Слайд 21
Спектр активности
Фторхинолоны активны в отношении грамположительных аэробных
бактерий (Staphylococcus spp.), большинства штаммов грамотрицательных, Е.coli (включая энтеротоксигенные
штаммы), Shigella spp., Salmonella spp., Enterobacter spp., Klebsiella spp., Proteus spp., Serratia spp., Citrobacter spp., M.morganii, Haemophilus spp., Neisseria spp., Pseudomonas spp., Legionella spp., Brucella spp., Listeria spp.
Слайд 22
Фармакокинетика хинолонов
Хорошо всасываются в ЖКТ. Пища не оказывает
существенного влияния на биодоступность. Максимальные концентрации в крови -
через 1-3 ч.
Проходят плацентарный барьер, и в небольших количествах проникают в грудное молоко.
Выводятся преимущественно почками. Частично выводятся с желчью.
Период полувыведения у различных фторхинолонов колеблется от 3-4 ч (норфлоксацин) до 12-14 ч (пефлоксацин, моксифлоксацин) и даже до 18-20 ч (спарфлоксацин).
Слайд 23
Нежелательные реакции
Общие для всех хинолонов
ЖКТ: изжога, боль
в эпигастрии, тошнота, рвота, диарея.
ЦНС: ототоксичность, сонливость, бессонница, головная
боль, головокружение, парестезии, тремор, судороги.
Аллергические реакции: сыпь, зуд, отек Квинке.
Характерные для хинолонов I поколения
Гематологические реакции: тромбоцитопения, лейкопения; при дефиците Г-6-ФДГ - гемолиз.
Печень: холестатическая желтуха, гепатит.
Характерные для фторхинолонов
Опорно-двигательный аппарат: артропатия, артралгия, миалгия.
Почки: кристаллурия, транзиторный нефрит.
Сердце: удлинение интервала QT на ЭКГ.
Другие: кандидоз слизистых, псевдомембранозный колит.
Слайд 24
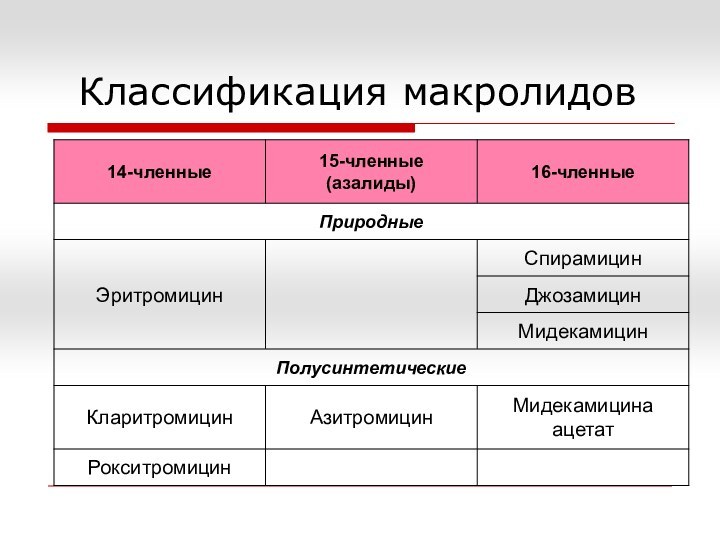
Макролиды
- класс антибиотиков, основу химической структуры которых
составляет макроциклическое лактонное кольцо.
В зависимости от числа атомов
углерода в кольце макролиды подразделяются на 14-членные (эритромицин, рокситромицин, кларитромицин), 15-членные (азитромицин) и 16-членные (мидекамицин, спирамицин, джозамицин).
Относятся к числу наименее токсичных антибиотиков.
Слайд 26
Механизм действия
Антимикробный эффект обусловлен нарушением синтеза белка
на рибосомах микробной клетки. Как правило, макролиды оказывают бактериостатическое
действие, но в высоких концентрациях способны действовать бактерицидно на БГСА, пневмококк, возбудителей коклюша и дифтерии. Макролиды проявляют ПАЭ в отношении грамположительных кокков.
Слайд 27
Спектр активности макролидов
Активны в отношении грамположительных кокков: S.pyogenes,
S.pneumoniae, S.aureus (кроме MRSA). Отмечено нарастание резистентности, но 16-членные
макролиды могут сохранять активность в отношении пневмококков и пиогенных стрептококков, устойчивых к 14- и 15-членным препаратам.
Действуют на возбудителей коклюша и дифтерии, моракселлы, легионеллы, кампилобактеры, листерии, спирохеты, хламидии, микоплазмы, уреаплазмы, анаэробы (исключая B.fragilis).
Слайд 28
Фармакокинетика
Наибольшее связывание с белками плазмы - у
рокситромицина (более 90%), наименьшее - у спирамицина (менее 20%).
Хорошо распределяются в организме, создавая высокие концентрации в различных тканях и органах, проникают внутрь клеток и создают высокие внутриклеточные концентрации.
Плохо проходят через ГЭБ.
Проходят через плаценту и проникают в грудное молоко.
Метаболизируются в печени, метаболиты выводятся преимущественно с желчью. Период полувыведения колеблется от 1 ч (мидекамицин) до 55 ч (азитромицин). При почечной недостаточности у большинства макролидов (кроме кларитромицина и рокситромицина) этот параметр не изменяется.
Слайд 29
Нежелательные реакции
ЖКТ: боль или дискомфорт в животе,
тошнота, рвота, диарея (чаще их вызывает эритромицин, реже всего
- спирамицин и джозамицин).
Печень: транзиторное повышение активности трансаминаз, холестатический гепатит.
ЦНС: головная боль, головокружение, нарушения слуха (редко при в/в введении больших доз эритромицина).
Сердце: удлинение интервала QT на электрокардиограмме (редко).
Местные реакции: флебит и тромбофлебит при в/в введении (макролиды нельзя вводить в концентрированном виде и струйно, они вводятся только путем медленной инфузии).
Аллергические реакции (сыпь, крапивница и др.) .
Слайд 30
Ингибиторозащищенные аминопенициллины
Антимикробный спектр (амоксициллин/клавуланат, ампициллин/сульбактам) расширен за
счет Klebsiella spp., P.vulgaris, C.diversus, а также анаэробов группы B.fragilis,
которые синтезируют хромосомные β-лактамазы класса А.
Активны в отношении микрофлоры с приобретенной резистентностью, обусловленной продукцией β-лактамаз: стафилококков, гонококков, M.catarrhalis, Haemophilus spp., E.coli, P.mirabilis.
Слайд 32
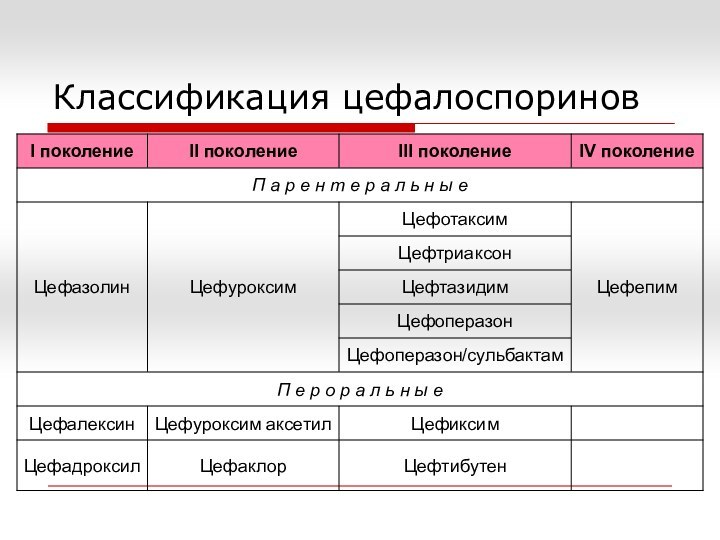
Цефалоспорины I поколения
Антибиотики активны в отношении Streptococcus spp.
(S.pyogenes, S.pneumoniae) и метициллиночувствительных Staphylococcus spp. По уровню антипневмококковой активности
цефалоспорины I поколения уступают аминопенициллинам и большинству более поздних цефалоспоринов.
Цефалоспорины I поколения устойчивы к действию стафилококковых β-лактамазЦефалоспорины I поколения устойчивы к действию стафилококковых β-лактамаз, но отдельные штаммы могут проявлять к ним умеренную устойчивость. Пневмококки проявляют полную ПР к цефалоспоринам I поколения и пенициллинам.
Слайд 33
Цефалоспорины II поколения
Спектр действия в отношении грамотрицательных
микроорганизмов шире, чем у представителей I поколения. Препараты активны в
отношении Neisseria spp., но клиническое значение имеет только активность цефуроксима в отношении гонококков. Цефуроксим активенее в отношении M. catarrhalis и Haemophilus spp., в то время как цефаклор частично разрушается ферментами.
Из семейства Enterobacteriaceae чувствительны E.coli, Shigella spp., Salmonella spp., P.mirabilis, Klebsiella spp., P.vulgaris, C.diversus. Цефуроксим и цефаклор разрушаются БЛРС. Псевдомонады, анаэробы группы B.fragilis устойчивы к цефалоспоринам II поколения.
Слайд 34
Цефалоспорины III поколения
Цефиксим и цефтибутен отличаются от цефотаксима
и цефтриаксона следующим:
отсутствие активности в отношении Staphylococcus spp.;
цефтибутен малоактивен в
отношении пневмококков и зеленящих стрептококков;
оба препарата неактивны в отношении Enterobacter spp., Serratia spp., M.morganii, P.rettgeri.
Слайд 35
Группа линкозамидов
В группу линкозамидов входят природный АМП
линкомицин и его полусинтетический аналог клиндамицин, обладающие узким спектром
активности. Используются при инфекциях, вызванных грамположительными кокками и неспорообразующей анаэробной флорой.
У микрофлоры, особенно стафилококков, довольно быстро развивается резистентность к линкозамидам, перекрестная к обоим препаратам.
Слайд 36
Механизм действия
Линкозамиды оказывают бактериостатическое действие, которое обусловлено
ингибированием синтеза белка рибосомами. В высоких концентрациях они могут
проявлять бактерицидный эффект.
Слайд 37
Спектр активности
К линкозамидам наиболее чувствительны стафилококки (кроме MRSA),
стрептококки, пневмококки и неспорообразующие анаэробы - пептококк, пептострептококки, бактероиды
(включая B.fragilis).
Клиндамицин умеренно активен в отношении некоторых простейших - токсоплазм, пневмоцист, P.falciparum.
Слайд 38
Фармакокинетика
После приема внутрь быстро всасываются из ЖКТ, причем
клиндамицин всасывается значительно лучше, чем линкомицин, его биодоступность (90%)
не зависит от приема пищи.
Линкозамиды распределяются в большинстве тканей и сред организма, за исключением СМЖ. Высокие концентрации достигаются в бронхолегочном секрете, костной ткани, желчи. Проходят через плаценту и проникают в грудное молоко.
Метаболизируются в печени, выводятся преимущественно ЖКТ, почками экскретируется 10-30%. Период полувыведения линкомицина - 4-6 ч, клиндамицина - несколько меньше.
Слайд 39
Нежелательные реакции
ЖКТ: боль в животе, диарея, тошнота,
рвота, псевдомембранозный колит.
Аллергическая реакция: сыпь, покраснение кожи, зуд.
Гематологические реакции:
нейтропения, тромбоцитопения.
Слайд 40
Группа гликопептидов
К гликопептидам относятся природные антибиотики -
ванкомицин и тейкопланин. В последнее время интерес к гликопептидам
возрос в связи с увеличением частоты нозокомиальных инфекций, вызванных грамположительными микроорганизмами.
В настоящее время – это препараты выбора при инфекциях, вызванных MRSA, MRSE, а также энтерококками.
Слайд 41
Механизм действия
Гликопептиды нарушают синтез клеточной стенки бактерий.
Оказывают бактерицидное действие, однако в отношении энтерококков, некоторых стрептококков
и КНС действуют бактериостатически.
Слайд 42
Спектр активности
Гликопептиды активны в отношении грамположительных аэробных
и анаэробных микроорганизмов: стафилококков (включая MRSA, MRSE), стрептококков, пневмококков,
энтерококков, пептострептококков, листерий, коринебактерий, клостридий (включая C.difficile). Грамотрицательные микроорганизмы устойчивы к гликопептидам.
Слайд 43
Фармакокинетика
Гликопептиды не всасываются при приеме внутрь. Биодоступность тейкопланина
при в/м введении - около 90%.
Гликопептиды не метаболизируются, выводятся
почками в неизмененном виде. Препараты не удаляются при гемодиализе.
Период полувыведения ванкомицина - 6-8 ч, тейкопланина - от 40 ч до 70 ч. Длительный период полувыведения тейкопланина дает возможность назначать его один раз в сутки
Слайд 44
Нежелательные реакции
Почки: обратимое нарушение функции почек при
использовании ванкомицина отмечается в 5-40%. Риск увеличивается при сочетанном
применении с аминогликозидами, фуросемидом или этакриновой кислотой.
ЦНС: головокружение, головная боль.
Ототоксичность: понижение слуха, вестибулярные нарушения.
Местные реакции: боль, жжение в месте введения, флебит.
Аллергические реакции: сыпь, крапивница, анафилактический шок (редко).
Гематологические реакции: лейкопения, тромбоцитопения.
ЖКТ: тошнота, рвота, диарея.
Печень: транзиторное повышение трансаминаз, щелочной фосфатазы.
Слайд 45
Карбоксипенициллины
Карбоксипенициллины действуют на представителей семейства Enterobacteriaceae (за
исключением Klebsiella spp., P.vulgaris, C.diversus), а также на P.aeruginosa. Следует
учитывать - многие штаммы синегнойной палочки в настоящее время устойчивы.
Эффективность карбоксипенициллинов ограничивается способностью многих бактерий к выработке различных β-лактамаз.
Слайд 46
Уреидопенициллины
Азлоциллин и пиперациллин обладают сходным спектром активности.
По действию на грамположительные бактерии они превосходят карбоксипенициллины.
Уреидопенициллины высокоактивны
в отношении всех важнейших грамотрицательных бактерий: семейства Enterobacteriaceae, P.aeruginosa, других псевдомонад и неферментирующих микроорганизмов (S.maltophilia).
Однако клиническое значение уреидопенициллинов ограничено, что объясняется их лабильностью к действию подавляющего большинства β-лактамаз стафилококков и грамотрицательных бактерий.
Слайд 47
Аминопенициллины и ингибиторозащищенные аминопенициллины
Антимикробный спектр ингибиторозащищенных аминопенициллинов
(амоксициллин/клавуланат, ампициллин/сульбактам) расширен за счет грамотрицательных бактерий - Klebsiella spp.,
P.vulgaris, C.diversus, а также анаэробов группы B.fragilis.
Ингибиторозащищенные аминопенициллины активны в отношении микрофлоры с продукцией β-лактамаз: стафилококков, гонококков, M.catarrhalis, Haemophilus spp., E.coli, P.mirabilis.
Слайд 48
Карбоксипенициллины и ингибиторозащищенные карбоксипенициллины
Эффективность ограничивается способностью бактерий
к выработке β-лактамазЭффективность ограничивается способностью бактерий к выработке β-лактамаз.
Негативный эффект этих ферментов (класс А) не проявляется в отношении ингибиторозащищенного производного тикарциллина - тикарциллин/клавуланата. Однако наличие ингибитора β-лактамаз не всегда обеспечивает активность в отношении ряда грамотрицательных бактерий.
Тикарциллин/клавуланат не имеет преимуществ перед тикарциллином по действию на P.aeruginosa.
Слайд 49
Цефалоспорины I поколения
Основным показанием для применения цефазолина
в настоящее время является периоперационная профилактика в хирургии. Он
используется также для лечения инфекций кожи и мягких тканей.
Слайд 50
Цефалоспорины III поколения
Базовые АМП - цефотаксим и
цефтриаксон, практически идентичны по своим антимикробным свойствам. Активны в
отношении Streptococcus spp., пневмококков, менингококков, гонококков, H.influenzae и M.catarrhalis, зеленящих стрептококков, S.aureus, кроме MRSA, кроме MRSA, в меньшей степени - в отношении КНС. Коринебактерии, как правило, чувствительны.
Высоко активны в отношении всего семейства Enterobacteriaceae, включая микроорганизмы с β-лактамазами широкого спектра.
Цефтазидим и цефоперазон сходны с цефотаксимом и цефтриаксоном. Их отличает следующее:
выраженная активность в отношении P.aeruginosa и других неферментирующих микроорганизмов;
меньшая активность в отношении стрептококков;
высокая чувствительность к гидролизу БЛРС.
Слайд 51
Ингибиторозащищенные цефалоспорины
Единственным представитель этой группы - цефоперазон/сульбактам.
По сравнении с цефоперазоном спектр действия расширен за счет
анаэробных микроорганизмов, препарат также активен в отношении большинства энтеробактерий, продуцирующих β-лактамазы широкого и расширенного спектров.
Данный АМП высокоактивен в отношении Acinetobacter spp.
Слайд 52
Цефалоспорины IV поколения
Цефепим по многим параметрам близок
к цефалоспоринам III поколения, но лучше проникает через внешнюю мембрану
грамотрицательных бактерий.
Относительной устойчив к гидролизу β-лактамазами класса С, поэтому
высоко активен в отношении P.aeruginosa и неферментирующих микроорганизмов;
активен в отношении гиперпродуцентов β-лактамаз класса С, таких как: Enterobacter spp., C.freundii, Serratia spp., M.morganii;
более устойчив к гидролизу БЛРС.
Слайд 53
Показания
Тяжелые, нозокомиальные, инфекции, вызванные полирезистентной микрофлорой:
инфекции НДП (пневмония,
абсцесс легкого и т.д.):
осложненные инфекции МВП;
инфекции кожи, мягких тканей,
костей и суставов;
интраабдоминальные инфекции;
сепсис.
Инфекции на фоне нейтропении и других иммунодефицитных состояний.
Слайд 54
Группа монобактамов
Из монобактамов, или моноциклических β-лактамов, в
клинической практике применяется один антибиотик - азтреонам. Он имеет
узкий спектр антибактериальной активности и используется для лечения инфекций, вызванных аэробной грамотрицательной флорой
Слайд 55
Механизм действия
Азтреонам обладает бактерицидным эффектом, который связан
с нарушением образования клеточной стенки бактерий.
Слайд 56
Спектр активности
Клиническое значение имеет активность азтреонама в
отношении Enterobacteriaceae (E.coli, энтеробактер, клебсиелла, протей, серрация, цитробактер, морганелла)
и P.aeruginosa, в том числе в отношении нозокомиальных штаммов, устойчивых к аминогликозидам, в том числе в отношении нозокомиальных штаммов, устойчивых к аминогликозидам и цефалоспоринам.
Слайд 57
Фармакокинетика
Азтреонам применяется только парентерально. Проходит через ГЭБ при
воспалении оболочек мозга, через плаценту и проникает в грудное
молоко.
Очень незначительно метаболизируется в печени, экскретируется преимущественно почками, на 60-75% в неизмененном виде.
Период полувыведения составляет 1,5-2 ч, при циррозе печени может увеличиваться до 2,5-3,5 ч, при почечной недостаточности - до 6-8 ч.
Слайд 58
Группа карбапенемов
Механизм действия
Мощное бактерицидное действие, обусловленное нарушением
образования клеточной стенки бактерий.
По сравнению с другими β-лактамами
быстрее проникают через наружную мембрану грамотрицательных бактерий и оказывают выраженный ПАЭ.
Слайд 59
Спектр активности карбапенемов
Действуют на стафилококки (кроме MRSA), стрептококки,
включая S.pneumoniae, гонококки, менингококки. Имипенем действует на E.faecalis.
Высокоактивны в
отношении Enterobacteriaceae (кишечная палочка, клебсиелла, протей, энтеробактер, цитробактер, ацинетобактер), в том числе в отношении штаммов, резистентных к цефалоспоринам III-IV поколения и ингибиторозащищенным пенициллинам. Большинство штаммов P.aeruginosa изначально чувствительны, но затем отмечается нарастание резистентности.
Карбапенемы высокоактивны в отношении спорообразующих и неспорообразующих (включая B. fragilis) анаэробов.
Слайд 60
Фармакокинетика
Карбапенемы применяются только парентерально. Хорошо распределяются в
организме. При воспалении оболочек мозга проникают через ГЭБ, создавая
высокие концентрации в СМЖ.
Карбапенемы не метаболизируются, выводятся преимущественно почками в неизмененном виде, поэтому при почечной недостаточности возможно значительное замедление их элиминации.
Слайд 61
Нежелательные реакции
Аллергические реакции: сыпь, крапивница, отек Квинке,
анафилактический шок.
Местные реакции: флебит, тромбофлебит.
ЖКТ: глоссит, тошнота, рвота, в
редких случаях , псевдомембранозный колит.
ЦНС: головокружение, нарушения сознания, тремор, судороги.
Другие: гипотензия (чаще при быстром внутривенном введении).
Слайд 63
Механизм действия
Аминогликозиды оказывают бактерицидное действие, которое
связано с нарушением синтеза белка рибосомами.
Степень антибактериальной активности аминогликозидов
зависит от их максимальной (пиковой) концентрации в сыворотке крови.
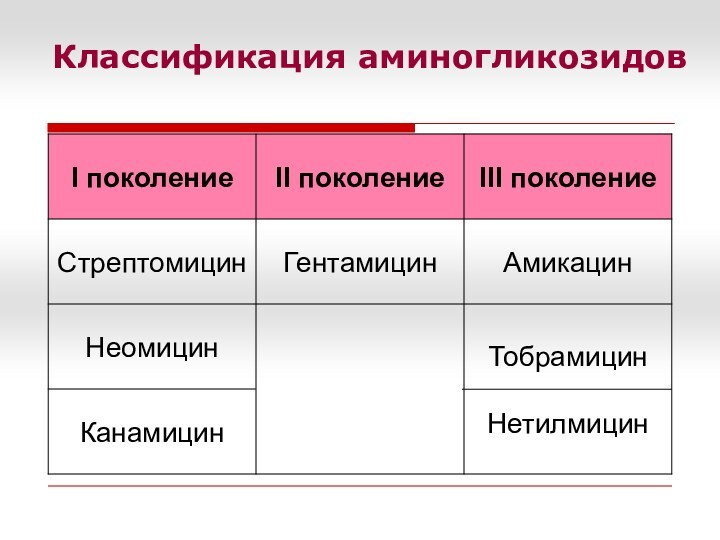
Слайд 64
Спектр активности
Аминогликозидов II и III поколения дествуют на Enterobacteriaceae
(E.coli, Proteus spp., Klebsiella spp., Enterobacter spp.и др.), а также на грамотрицательные
палочки (P.aeruginosa, Acinetobacter spp.). Аминогликозиды активны в отношении стафилококков, кроме MRSA.
Стрептомицин и гентамицин действуют на энтерококки.
Аминогликозиды неактивны в отношении S.pneumoniae, S.maltophilia, анаэробов. Более того, резистентность их к аминогликозидам используется при идентификации этих микробов.
Слайд 65
Фармакокинетика
При приеме внутрь аминогликозиды не всасываются и применяются
парентерально. Всасываются быстро и полностью. Пиковые концентрации - через
30 мин после окончания в/в инфузии и 0,5-1,5 ч после в/м введения.
Аминогликозиды распределяются во внеклеточной жидкости, включая сыворотку крови, экссудат абсцессов, асцитическую, перикардиальную, плевральную, синовиальную, перитонеальную жидкости. Способны создавать высокие концентрации в печени, легких, почках.
выводятся почками в неизмененном виде.
Период полувыведения у новорожденных - 5-8 ч, у детей - 2,5-4 ч. При почечной недостаточности - до 70 ч и более.