Слайд 2
Словарик
Хромосомные болезни – наследственные заболевания, обусловленные изменением числа

или структуры хромосом. Частота Хромосомных болезней среди новорождённых детей
около 1%. Многие изменения хромосом несовместимы с жизнью и являются частой причиной спонтанных абортов и мертворождений. При спонтанных абортах обнаружено около 20% эмбрионов с аномальными кариотипами (хромосомными наборами). Изменение числа хромосом происходит в результате нерасхождения их в мейозе или при делении клеток на ранней стадии развития оплодотворённого яйца. Нерасхождению хромосом при первых делениях оплодотворённого яйца способствует, например, высокий возраст матери. Хромосомные аберрации обусловливаются физическими (ионизирующее излучение) и химическими (например, лекарственные препараты с мутагенным эффектом) факторами; вирусами (краснухи, вирусного гепатита, ветряной оспы и др.), антителами и различными расстройствами метаболизма. Хромосомные болезни могут быть связаны с излишком генетического материала (полисемия - наличие одной или нескольких добавочных хромосом; полиплоидия; дупликация); с утратой части генетического материала (нуллисомия, моносомия, делеция); с хромосомными перестройками (транслокация; различные перестановки участков хромосом). Различают также группы Х. б., обусловленных изменениями половых и неполовых хромосом.
Трисомия (от греч. tri-, в сложных словах - три и soma - тело) – наличие в хромосомном наборе диплоидного организма одной или нескольких лишних хромосом, не гомологичных друг другу. Организмы (или клетки), у которых одна, две или большее число хромосом представлены тремя гомологами, называются простыми, двойными и т.д. трисомиками. Т. - результат нерасхождения хромосом при делении клетки. Т. по отдельным хромосомам приводит к тяжёлым заболеваниям.
Слайд 3
Моносомия - отсутствие в хромосомном наборе диплоидного организма

одной хромосомы. Клетку или организм, у которых та или
иная гомологичная хромосома представлена в единственном числе, называют моносомиком. Моносомия - результат нарушений при расхождении гомологичных хромосом, что чаще происходит в половых клетках (при мейозе), но возможно и в клетках тела - соматических (при митозе). Например, больные синдромом Шерешевского-Тернера - моносомики по половой Х-хромосоме.
Делеция (от лат. deletio - уничтожение) – потеря участка хромосомы. Делеция может быть следствием разрыва хромосомы или результатом неравного кроссинговера. Делеции подразделяются на интерстициальные (потеря внутреннего участка) и терминальные (потеря концевого участка).
Нуллисомия (от лат. nullus - никакой, несуществующий и греч. sōma - тело) – тип геномной мутации, заключающийся в отсутствии в клетках организма какой-либо пары хромосом, в норме присущей данному виду. Организмы с нуллисомией называются нуллисомиками. Нуллисомия, в особенности у высших животных, обычно ведёт к гибели организма.
Транслокация – в генетике тип хромосомной перестройки (мутации), заключающейся в обмене участками хромосом; часто приводит к снижению плодовитости животных и растений.
Полиплоидия - наследственное изменение, связанное с кратным увеличением основного числа хромосом в клетках организма. Полиплодия широко распространена у растений. Обычно у полиплоидных растений более крупные размеры, повышенное содержание ряда веществ, лучшая устойчивость к неблагоприятным условиям внешней среды и т.п. Различают два типа полиплоидов: аутополиплоиды и аллополиплоиды.
Дупликация - разновидность хромосомных перестроек, при которых какой-либо участок хромосомы в гаплоидном наборе оказывается представленным два раза. Гетерозиготные по дупликации особи несут две дозы дуплицированных генов, гомозиготные - четыре. Различают внутрихромосомную и межхромосомную дупликации
Слайд 4
Типы наследственности
1. Аутосомно-доминантный тип наследования:
а. При достаточном

числе потомков признак обнаруживается в каждом поколении
б. Редкий
признак наследуется примерно половиной детей
в. Потомки мужского и женского пола наследуют этот признак одинаково
г. Оба родителя в равной мере передают этот признак детям
2. Аутосомно-рецессивный тип наследования:
а. Признак может передаваться через поколение даже при достаточном числе потомков
б. Признак может проявиться у детей в отсутствие его у родителей. Обнаруживается тогда в 25% случаев у детей
в. Признак наследуется всеми детьми, если оба родителя больны
г. Признак в 50% развивается у детей, если один из родителей болен
д. Потомки мужского и женского пола наследуют этот признак одинаково
3. Наследование, сцепленное с Х хромосомой, если ген, контролирующий проявления признака, - рецессивный:
а. Мужчины наследуют чаще, чем женщины
б. Наследуют такой признак девочки только от отца
в. В браках, где оба супруга здоровы, могут родиться дети, имеющие его, при этом он наследуется 50% сыновей и 100% здоровых дочерей
г. Прослеживается чередование больных мужчин в поколениях: где их больше, где - меньше
4. Наследование, сцепленное с Х хромосомой, если ген, контролирующий проявления признака, - доминантный:
а. Мужчины наследуют реже, чем женщины
б. Если признак только у супруги, то наследуют его все дети (мать гомозиготная), или половина детей (мать гетерозиготная)
в. Если только у супруга, то наследуют все лица женского пола
5. Наследование, сцепленное с Y хромосомой:
а. Страдают только сыновья, в каждом поколении проявляется, если отец болен.
Слайд 5
Наследственные заболевания:
Хромосомные болезни
Болезни обмена веществ
Нарушения иммунитета
Болезни с преимущественным
поражением эндокринной системы
Болезни крови
Нарушение функций почек
Болезни нервной системы
Поражения глаз
Болезни
пищеварительной системы
Слайд 6
Хромосомные болезни:
Синдром Патау
Синдром Дауна
Синдром Эдвардса
Синдром Шершевского-Тернера
Синдром «кошачьего крика»
Синдром
Клайнфельтера
Синдром дубль-Y
Трисомия Х
Слайд 7
Синдром Шершевского-Тернера
Известно, что пол женщины и мужчины определяется

наличием двух половых хромосом: у женщины - ХХ, у
мужчины - ХY хромосом. Половая мужская Y-хромосома наиболее чувствительна к влияниям окружающей среды, являясь «проводником экологической информации в геном». Воздействие рентгеновских и ультрафиолетовых лучей вызывают мутации и делеции (удаления) генов. По данным ряда исследователей у современных мужчин Y-хромосома значительно меньше Х-хромосомы и похожа на маленькую букву “v”. Если Х-хромосома содержит около 3000-4000 генов, то мужская половая Y-хромосома состоит всего из 26-33 генов (изначально она содержала более 1500 генов). Продолжающееся уменьшение Y-хромосомы, а затем и ее полное разрушение может привести к сильной модификации мужского пола и появлению сначала в большом количестве гомосексуалистов, бесплодных мужчин и мужчин с женским типом поведения, в связи с доминированием Х-хромосомы, а затем недоразвитых женоподобных существ, которые не способны к родам, т.е. людей с одной Х-хромосомой (ХО). Дегенерация Y-хромосомы была выявлена у 5-15% бесплодных мужчин. Поэтому даже микроструктурные изменения в половых хромосомах могут привести к бесплодию. Люди с одной Х-хромосомой уже есть: это люди с синдромом Шершевского-Тернера, который встречается как у мужчин, так и у женщин. У людей с этим синдромом верхняя часть туловища такая же, как у мужчин, нижняя – как у женщин. в настоящее время этот синдром встречается у 1 из 3000 мужчин. Также есть опасения, что из-за постепенного разрушения Y-хромосомы и нарушения сперматогенеза, резко снизится процент рождения мальчиков. А в конечном счете мальчики и вовсе перестанут рождаться.
Изменения в половых хромосомах наблюдается и у женщин. Неблагоприятные антропогенные факторы могут привести к быстрому разрушению, а потом и исчезновению одной из Х-хромосом и к появлению сначала в большом количестве лесбиянок, бесплодных и мужеподобных женщин как результат разрушения генов в Х-хромосоме, а затем все тех же недоразвитых женщин, т.е. людей с одной Х-хромосомой (синдром Шершевского-Тернера: ХО). Процесс разрушения генов в половых хромосомах у женщин идет медленнее, чем у мужчин. количество мутаций генов у женских особей как человека, так и животных происходит в 4-6 раз меньше, чем у мужских. Одна из причин более медленной дегенерации, возможно, связана с наличием двух Х-хромосом, которые дублируют друг друга. У мужчин любые изменения в Y-хромосоме проявляются в следующем поколении мальчиков.
Слайд 8
Синдром Шершевского-Тернера
Слайд 9
Синдром Патау
(синдром 13-трисомии)
Встречается примерно в одном случае

на 25 тыс. живорожденных детей. Риск увеличивается пропорционально возрасту
беременной женщины. В 75% случаев синдром Патау возникает, когда плод получает три 13-е хромосомы вместо двух. Около 20% случаев связаны с транслокацией избыточной хромосомы. Унаследованная транслокация увеличивает вероятность повторения синдрома в следующем поколении. Хромосомы обоих родителей необходимо исследовать, чтобы установить, является ли транслокация унаследованной.
СИМПТОМЫ. Дети с синдромом Патау имеют сходные физические особенности: маленькая голова, покатый профиль, маленькие глаза, поражения кожи или лысины на голове, ненормальные уши, расщепленные верхняя губа и нёбо, лишние пальцы на руках или ногах (полидактилия). Многие дети с синдромом Патау имеют врожденные пороки сердца и мочеполовой системы.
Большинство детей умирает в течение первого года жизни, некоторые доживают до двух лет. Выжившие отстают в умственном и физическом развитии и часто страдают эпилептическими расстройствами.
ЛЕЧЕНИЕ. Исправить хромосомные нарушения невозможно. Комплексная работа группы различных специалистов заключается в постоянном контроле за состоянием здоровья больного и поддержке семьи.
Слайд 11
Синдром Эдвардса
(синдром 18-трисомии)
Встречается в одном случае на 6600

живорожденных, почти 80% пораженных — девочки. Риск его появления
увеличивается пропорционально возрасту беременной женщины. В 95% случаев синдром Эдвардса появляется, если вместо двух 18-х хромосом ребенком унаследовано три. В остальных 5% случаев синдром Эдвардса вызван транслокацией, в которой избыточная 18-я хромосома присоединяется к другой хромосоме. В случае унаследованной транслокации риск повторения синдрома Эдвардса в следующем поколении достаточно велик. Для того чтобы определить, является ли транслокация унаследованной, необходимо исследовать хромосомы обоих родителей.
СИМПТОМЫ. Дети с синдромом Эдвардса обычно рождаются переношенными, но с значительным отставанием в развитии и маленькими относительно возраста плода. Физические проявления синдрома Эдвардса включают удлиненную голову со значительным выпячиванием черепа у основания, маленькие широко расставленные глаза, маленькие рот и подбородок, низко расположенные и деформированные уши, короткую грудину. Наиболее характерная черта — сжатый кулак с указательным пальцем, перекрывающим другие пальцы; большой палец часто недоразвит или отсутствует, ногти на руках и ногах также бывают недоразвитыми. При синдроме Эдвардса нередко встречаются пороки сердца и почек, легких и диафрагмы, а также грыжи.
Обычна сильная умственная отсталость. Значительное число детей живет не более нескольких месяцев, а большинство — не больше года. Немногие доживают до подросткового возраста.
ЛЕЧЕНИЕ. Способа исправить хромосомные нарушения нет. Работа группы различных специалистов направлена на то, чтобы обеспечить постоянный контроль за состоянием здоровья ребенка и поддержку семьи.
Слайд 13
Синдром Дауна
(синдром 21-трисомии)
Встречается в одном случае на 7—10

тыс. живорожденных детей обоих полов во всем мире. Вероятность
его появления увеличивается в зависимости от возраста беременной-женщины, а иногда и отца. Синдром Дауна — наиболее распространенное генетическое заболевание, вызывающее умственную отсталость. При синдроме Дауна плод наследует три 21-е хромосомы вместо двух. Это называется трисомией-21. 95% всех людей с синдромом Дауна имеют классическую трисомию, т. е. каждая клетка тела содержит три 21-е хромосомы. Примерно 4% всех людей с синдромом Дауна имеют транслокации. Это означает, что избыточная 21-я хромосома присоединена к какой-либо другой хромосоме. Некоторые люди с синдромом Дауна имеют мозаичный набор хромосом, т. е. часть клеток содержат нормальное число хромосом — 46, а другие — 47. Если транслоцированная хромосома или комбинация хромосом унаследована от одного из родителей, вероятность повторного появления транслокации в следующем поколении колеблется от 3 до 15%. Для определения унаследованной транслокации необходимо исследовать хромосомы обоих родителей. Вероятность повторения классической трисомии составляет 1—2%.
СИМПТОМЫ: Плоское лицо, монголоидный разрез глаз, открытый рот, короткий нос, плоская переносица, косоглазие, пигментные пятна по краю радужки; увеличение поперечного размера головы при относительном уменьшении продольного размера; плоский затылок; деформированные низко посаженные уши; аркообразное небо, зубные аномалии, бороздчатый язык; короткая широкая шея, кожная складка на шее у новорожденных; короткие конечности, повышенная подвижность суставов; деформация грудной клетки (килевидная или воронкообразная; мышечная слабость; врожденные пороки сердца; поперечная ладонная складка; умственная отсталость.
Умственная отсталость может быть выражена в разной степени. Поведение и психическое развитие также варьируют. Люди с синдромом Дауна склонны к болезням органов слуха и дыхательных путей. Кроме того, у них в 20 раз чаще, чем обычно, развивается лейкемия.
ЛЕЧЕНИЕ. Хромосомные нарушения устранить невозможно. Наблюдение группы специалистов, хирургическое вмешательство с целью исправить врожденные пороки и антибиотики с целью лечения инфекционных заболеваний могут существенно продлить жизнь людей с синдромом Дауна. Раннее вмешательство и постоянная забота о здоровье, а также специальное воспитание очень важны, чтобы помочь больным людям наиболее полно развить свои способности.
Слайд 15
А теперь немного о мало известных хромосомных заболеваниях
человека...
Слайд 16
Синдром «кошачьего крика»
Синдром кошачьего крика (5р-) обусловлен делецией
короткого плеча 5-й хромосомы. Популяционная частота синдрома -примерно 1:45
000.
Для данного синдрома наиболее характерны специфический плач, напоминающий кошачье мяуканье, лунообразное лицо, мышечная гипотония, умственное и физическое недоразвитие, микроцефалия, низко расположенные, иногда деформированные ушные раковины, эпикант, антимонголоидный разрез глазных щелей, косоглазие. Иногда наблюдаются атрофия зрительного нерва и очаги депигментации сетчатки. Как правило, выявляются пороки сердца. Наиболее постоянный признак синдрома - "кошачий крик" - обусловлен изменениями гортани: сужением, мягкостью хрящей, отечностью или необычной складчатостью слизистой оболочки, уменьшением надгортанника. Изменения других органов и систем неспецифичны.
Продолжительность жизни у больных с этим синдромом значительно снижена, только около 14% из них переживают возраст 10 лет.
Слайд 18
Синдром Клайнфельтера
Синдром Клайнфельтера включает случаи полисомии по половым

хромосомам, при которых имеется не менее двух Х-хромосом и
не менее одной Y-хромосомы. Наиболее часто встречающийся и типичный по клинической картине синдром – это синдром Клайнфельтера с набором 47,ХХY. Этот синдром встречается с частотой 1:500 – 1:750 новорождённых мальчиков. Варианты полисомии с большим числом Х- и Y-хромосом встречаются редко. Клинически они также относятся к синдрому Клайнфельтера. Присутствие Y-хромосомы определяет формирование мужского пола. До периода полового созревания мальчики. развиваются почти нормально, лишь с небольшим отставанием в психическом развитии Генетический дисбаланс в связи с добавочной Х-хромосомой клинически проявляется в период полового созревания в виде недоразвития яичек и вторичных мужских половых признаков. Семенные канальцы часто атрофируются, а сперматозоиды не вырабатываются, что является причиной стерильности. У мужчин с синдромом Клайнфельтера регистрируется повышенный уровень характерного для женщин фолликулостимулирующего гормона, который выделяется с мочой; молочные железы увеличены, однако к лактации они не способны, так как состоят из плотной соединительной ткани. В процессе возмужания у больных с этим синдромом складывается евнухоидный тип строения тела: узкие плечи и грудная клетка, широкий таз, слабо развитые мускулатура и волосяной покров на лобке, подмышками, слабое оволосение лица. Больные обычно имеют высокий рост. Люди с синдромом Клайнфельтера обычно безынициативны и редко способны к творческой деятельности. Они легко поддаются внушению и эмоционально неустойчивы. Интеллект нередко при этом не страдает, хотя в некоторых случаеях отмечается задержка умственного развития, порой приводящая к дебильности. Почти всегда умственная отсталость выявляется у больных с хромосомным набором ХХХY или даже с ХХХХY. Внешне таких людей можно четко идентифицировать как мужчин, однако они стерильны и обладают внешностью евнухов. Несколько сгладить проявление синдрома Клайнфельтера можно с помощью инъекций аналога мужского полового гормона метилтестостерона, которые врачи рекомендуют начинать делать в возрасте 10 – 11 лет. Поэтому очень важно вовремя идентифицировать таких больных, что можно сделать в результате анализа их клеток.
Слайд 20
Синдром дубль-Y
Синдром XYY характеризуется кариотипом 47, XYY. Он

впервые описан в 1960 г. Частота синдрома по среднестатистическим данным
составляет среди новорожденных около 1:1000. Иногда приводятся значительно более высокие данные— 1:250.
Наиболее частым признаком является высокий рост, который у взрослых больных составляет в среднем 186 см. Однако этот признак не является абсолютным, так как в литературе имеются описания мужчин с кариотипом 47, XYY среднего роста. У части больных отмечаются нерезко выраженные евнухоидные черты телосложения и диспластические признаки: неправильное строение зубов, увеличение нижней челюсти, аномальный прикус, девиация коленных и локтевых суставов, радиоульнарный синостоз. У некоторых больных обнаруживается повышение уровня андрогенов и лютеинизирующего гормона. Половая функция не нарушена. Наличие добавочной Y-хромосомы может и не сопровождаться клинической патологией, но, несомненно, оно коррелирует как с интеллектуальным недоразвитием, так и с эмоционально-волевыми нарушениями.
При цитогенетическом исследовании с помощью люминесцентной микроскопии в буккальных мазках обнаруживается Y-хроматин. При анализе кариотипа выявляется дополнительная Y-хромосома.
Слайд 21
Трисомия Х
Частота трисомии-Х составляет среди новорожденных девочек и

женщин 1:1000, среди умственно отсталых — 0,59 %. Большинство
девочек и женщин с трисомией-Х выявлены среди больных психиатрических больниц.
Трисомию-Х иногда называют синдромом трипло-Х, однако это не является обоснованным: трисомия-Х не обусловливает четкого постоянного симптомокомплекса.
Клинические проявления весьма полиморфны, а у части пациентов с трисомией-Х вообще не обнаруживается каких-либо отклонений в физическом и психическом развитии. Вместе с тем одним из частых проявлений трисомии-Х является неглубокая умственная отсталость, которая отмечается у 75 % больных. Особое внимание привлекает частота заболевания шизофренией. У многих больных с трисомией-Х наблюдаются задержка физического развития, негрубые диспластические признаки: эпикант, высокое твердое небо, клинодактилия мизинцев. Реже встречаются больные высокого роста. У некоторых пациентов отмечается бесплодие, обусловленное недоразвитием фолликулов.
Диагноз ставят только при цитогенетическом исследовании: выявляют 47 хромосом и двойной половой хроматин. Описано также много случаев так называемой полисомии-Х: тетрасомия (ХХХХ) и пентасомия (ХХХХХ) с соответствующим увеличением количества телец полового хроматина. В этих случаях степень психического недоразвития выражена грубее и коррелирует с количеством дополнительных Х-хромосом.
Слайд 22
Болезни обмена веществ:
Гомоцистинурия
Гистидинемия
Нарушения обмена триптофана
Глюкоцереброзидозы
Финелкетонурия
Слайд 23
Глюкоцереброзидозы
Болезнь Гоше – это наиболее часто встречающаяся наследственная

болезнь нарушения накопления, при которой имеется дефицит лизосомного фермента,
расщепляющего церамидглюкозу, что приводит к образованию так называемых клеток Гоше.
Клиническая картина болезни: отмечается преобладающее увеличение паренхиматозных органов, особенно селезенки. При этом спленомегалия сопровождается гипоспленизмом с тромбоцитопенией, анемией и лейкопенией. Наиболее часто поражаются дистальные части трубчатых костей, 75% больных имеют остеопороз. Костные кризы могут протекать с острой болью.
Болезнь Фабри - наследуется сцепленно с Х-хромосомой. Причиной заболевания является дефект фермента a-галактозидазы А.
Образующиеся в результате дефекта фермента продукты (тригексозил- и дигалактозилцерамид) накапливаются в почечных канальцах, в сердечной мышце, в скелетных мышцах, в нейронах головного мозга, в эндотелии всех сосудов. В пораженных тканях обнаруживают пенистые клетки и суданофильные гранулы.
Накопление гликолипида вызывает характерные симптомы: быструю утомляемость, снижение остроты зрения, повышение артериального давления. У детей возникают приступы лихорадки, боли в руках и ногах, протеинурия, ангиокератомы. Продолжающееся накопление липидов приводит к почечной и сердечной недостаточности в возрасте 30-40 лет.
Слайд 24
Фенилкетонурия
Фенилкетонурия (ФКУ) - тяжелое наследственное заболевание, наступающее вследствие

врожденного дефекта фермента, отвечающего в организме человека за нормальный
обмен фенилаланина (одной из незаменимых аминокислот, входящих в состав белка).
При заболевании нарушаются обменные процессы, особенно важные для развивающегося мозга ребенка. В крови и других жидкостях организма накапливается в большом количестве фенилаланин и повышено образуются такие вещества как фенилпировиноградная, фенилмолочная и фенилуксусная кислоты, которые выделяются в повышенных количествах с мочой. Следствием нарушенного обмена в мозге является тяжелое психическое недоразвитие. Если не предпринято своевременное лечение, то больные на всю жизнь остаются глубокими инвалидами.
Поступающий в организм фенилаланин идет на построение белковой цепи или превращается в тирозин. Отсутствие в печени фермента фенилаланингидроксидазы препятствует нормальному превращению фенилаланина пищи в тирозин. Поэтому фенилаланин используется лишь при синтезе белка, а избыток накапливается в клетках печени и попадает в кровоток, где количество фенилаланина является токсичным для клеток мозга. Почки не справляются с его реабсорбцией, в результате чего он выводится с мочой. Именно наличие этого фенилкетона в моче дало основание назвать соответствующее патологическое состояние фенилкетонурией.
Слайд 25
Гомоцистинурия
Заболевание наследуется по аутосомно-рецессивному типу. Частота гомоцистинурии составляет

1:200 000 новорожденных. В основе заболевания лежит отсутствие или
снижение активности фермента цистатионинсинтетазы, что ведет к нарушению обмена метионина. Кофактором цистатионсинтетазы является витамин В6. Поэтому наблюдается пиридоксинчувствительная и пиридоксинрезистентная формы. У родителей и родственников больных часто обнаруживают шизофрению. Рядом авторов отмечается фенотипическое сходство с болезнью Марфана. Однако, при гомоцистинурии в отличие от болезни Марфана более выражены изменения нервной системы, снижение интеллекта и судорожный синдром.
Формы заболевания: классическая; связанная с дефицитом утилизации витамина В6; обусловленная нарушением метаболизма фолиевой кислоты.
Клинически дети, больные классической формой, при рождении выглядят здоровыми. Возможны лишь задержка роста и развития. Диагноз обычно устанавливается после 3-х лет, когда выявляется подвывих хрусталика. Основной рентгенологический признак - генерализованный остеопороз. При гомоцистинурии наблюдается клинический полиморфизм.
Слайд 26
Гистидинемия
Заболевание возникает в результате отсутствия или недостаточности активности

фермента гистидазы. Наследуется аутосомно-рецессивно. Для детей первого года жизни
гистидин – незаменимая аминокислота. При недостатке гистидина в этом возрасте отмечается нарушение ретенции азота, выявляется дефицит массы тела, появляются шелушение кожи и экзематозные высыпания. При гистидинемии происходит нарушение самого эффективного активного пути катаболизма – превращение гистидина в уроканиновую кислоту (этим путем в норме катаболизируется большая часть гистидина). В результате метаболического блока происходит накопление в крови и моче гистидина. Увеличение активности трансаминирования и усиленный перевод гистидина в имидазолпировиноградную, имидозолмолочную и имидозолуксусную кислоты является компенсаторно-приспособительной реакцией организма.
Симптомы: от тяжелой умственной отсталости до полного отсутствия каких-либо симптомов. Снижение интеллекта выявляется лишь у 50% больных детей. Больные гистидинемией имеют светлый цвет волос, голубые глаза. На первый план у таких детей выступает поражение нервной системы: снижение интеллекта, нарушение речи, судороги. А у детей с нормальным интеллектом можно выявить особенности психики при гистидинемии: эмоциональную лабильность, агрессивность.
Слайд 27
Нарушения обмена триптофана
Болезнь Гартнепа. Аутосомно-рецессивный тип наследования. При

данном заболевании наблюдается генетическое изменение транспортной функции клеток слизистой
оболочки кишечника и проксимальных отделов почечных канальцев. Для болезни Гартнепа характерны кожная фоточуствительность, пеллагроподобный дерматит, мозжечковая атаксия с вовлечением в процесс пирамидных путей, нарушение функции желудочно-кишечного тракта. У некоторых детей выявляется умственная отсталость.
Индиканурия. В основе заболевания лежит нарушение всасывания триптофана в кишечнике с образованием избыточного количества индола, который всасывается, окисляется, сульфатируется и выделяется в виде индикана. Последний окисляется под влиянием воздуха до голубого индикана, окрашивающего пеленки в синий цвет (болезнь "голубых пеленок").При индиканурии наблюдается гиперкальциемия, нефрокальциноз, периодическая гипертермия.
Синдром Тада. Аутосомно-рецессивный тип наследования. При синдроме Тада наблюдается недостаток фермента триптофанпирролазы, катализирующего превращение триптофана в кинуренин. Нарушения связаны с эндогенным дефицитом никотиновой кислоты и избытком индольных соединений. При синдроме Тада отмечается глубокая умственная отсталость, нанизм, мозжечковая атаксия.
Синдром Прайса. Генетический дефект кинуренингидроксилазы. Наблюдается избыточное выделение с мочой кинуренина за счет блока фермента. Основное проявление синдрома Прайса – склеродермия.
Слайд 28
Нарушения иммунитета
Агаммаглобулинемия
Слайд 29
Агаммаглобулинемия
АГАММАГЛОБУЛИНЕМИЯ (греч.отриц. приставка а- + гамма-глобулин + греч.

haima кровь; син.: пангипогамма-глобулинемия, болезнь Брутона) - наследственное заболевание,
характеризующееся отсутствием или резким снижением содержания в крови гамма-глобулинов. При этом снижается или становится невозможной выработка антител, в связи с чем больные с агаммаглобулинемией чрезвычайно подвержены инфекционным болезням.
Агаммаглобулинемия - редкое заболевание (частота 1:1 000 000). Тип наследования - рецессивный, сцепленный с X-хромосомой. Встречается только у мальчиков, обычно в возрасте до 6 лет. Начинается заболевание обычно со 2-го года жизни, но первые его признаки могут появиться уже в конце 1-го года. Клинически агаммаглобулинемия характеризуется рецидивирующими бактериальными инфекциями, в то время как вирусные переносятся обычно удовлетворительно. Инфекционные болезни при агаммаглобулинемии протекают длительно, с частыми обострениями и тяжелыми осложнениями. Отмечаются повторные пневмонии, отиты, пиодермии, сепсис.
Слайд 30
Болезни с преимущественным поражением эндокринной системы
Синдром Бёрьесона
Муковисцидоз
Кретинизм
Лепречаунизм
Слайд 31
Синдром Бёрьесона
Бёрьесона-Форсмана-Лемана синдром – наследственная форма слабоумия с
ожирением. Психика характеризуется умственным недоразвитием степени идиотии и наличием
эпилептиформных припадков, агрессивными тенденциями, аффективными вспышками. Соматически - малый или карликовый рост, genu valgum, гипотиреоз, диспластические черты в строении лица и черепа (башенный череп, узкие глазные щели, кожа и подкожная основа в области лба и щек отечны, ушные раковины увеличены). Ожирение равномерное, несколько больше выраженное в области молочных желез. Гипогенитализм. Чаще болеют мужчины. Заболевание наследственное, тип наследования рецессивный, сцепленный с полом.
Слайд 32
Муковисцидоз
Муковисцидоз - (от латинского mucus - слизь, viscidus

- вязкий) самое распространенное наследственное заболевание, при котором поражаются
все органы, которые выделяют секреты. Это бронхолегочная система, поджелудочная железа, печень, потовые железы, слюнные железы, железы кишечника, половые железы. Из-за дефекта (мутации) гена секреты во всех органах вязкие, густые, поэтому их выделение затруднено. В легких из-за вязкого, часто гнойного секрета, трудноотделяемого и скапливающегося в бронхах, довольно быстро (иногда уже в первые месяцы жизни) развиваются воспалительные процессы - повторные бронхиты и/или пневмонии с постепенным формированием хронического бронхолегочного процесса. У детей отмечаются постоянный раздражающий (иногда коклюшеподобный) кашель, одышка. Из-за недостатка ферментов поджелудочной железы у больных муковисцидозом плохо переваривается пища, поэтому такие дети, несмотря на повышенный аппетит, отстают в весе, у них обильный, жирный, зловонный стул. Из-за застоя желчи у некоторых детей развивается цирроз печени, могут сформироваться камни в желчном пузыре.
Муковисцидоз заложен в генах и передается по наследству. Каждый 20-й житель планеты является носителем дефектного гена. Муковисцидоз возникает у ребенка в том случае, если он от обоих родителей (и от мамы, и от папы) получил по гену с мутацией. Никакие природные катаклизмы, болезни родителей, их курение или прием алкогольных напитков, стрессовые ситуации значения не имеют. Муковисцидоз одинаково часто встречается как у мальчиков, так и у девочек.
Слайд 33
Кретинизм
КРЕТИНИЗМ - (от франц. cretin - слабоумный, кретин),

эндокринное заболевание - недостаточная функция щитовидной железы, задержка физического
и психического развития; главным образом в горных районах с недостатком йода в воде или как наследственная патология.
Причины развития кретинизма связаны с природным (экзогенным) дефицитом йода в воде и пище или эндогенной недостаточностью его. Средний рост взрослых больных кретинизмом: мужчин 146,7см, женщин 140см. У страдающих кретинизмом короткие конечности, кривые ноги, широкие кисти с короткими пальцами; череп круглый, лицо с низким лбом, одутловатое, нос седловидный, глазные впадины глубокие, уши большие, язык широкий, не помещающийся во рту, короткие редкие зубы. Кожа бледная, сухая, оволосение бедное. Часты пупочные и паховые грыжи, увеличение щитовидной железы; половые органы недоразвиты. Существенно нарушен обмен веществ; температура тела снижена. Постоянным и выраженным расстройством является снижение слуха (нередко глухонемота). Психическая отсталость при выраженном кретинизме достигает степени идиотии. Больные медлительны, сонливы, речь их задержана; усвоение знаний и трудовых навыков затруднено и замедлено. Лечение - компенсирующие недостаточность щитовидной железы препараты. При лечении с раннего детства многие больные кретинизмом приобретают навыки к самообслуживанию и способны выполнять несложные однотипные работы. Профилактика - йодирование воды и пищи.
Слайд 34
Лепречаунизм
Лепречаунизм (leprechaunismus; ирланд. leprechaun гном; син. Донохью синдром)
- наследственная болезнь женщин, обусловленная нарушениями развития и дисфункцией
эндокринной системы; характеризуется гипотрофией, малыми размерами лица, гирсутизмом, увеличением молочных желез, клитора и малых половых губ, гиперплазией яичников и островкового аппарата поджелудочной железы, накоплением гликогена и железа в печени, кальцинозом почек; наследуется по аутосомно-рецессивному типу, ограниченному полом.
Слайд 35
Болезни крови
Гемоглобинопатии
Серповидноклеточная анемия
Талассемия
Гемофилия
Тромбофилии
Слайд 36
Гемоглобинопатии
Гемоглобинопатии (от гемоглобин и греч. páthos - страдание,

болезнь), гемоглобинозы – состояния, обусловленные присутствием в красных кровяных
тельцах (эритроцитах) одного или нескольких аномальных (патологических) гемоглобинов. Выделено свыше 50 патологических разновидностей гемоглобина, возникших в результате врождённого, передаваемого по наследству дефекта образования белковой части гемоглобина - глобина. При аномалиях гемоглобина нарушаются физико-химические свойства эритроцитов, обменные процессы в них; эритроциты становятся менее устойчивыми к различным гемолизирующим факторам. При передаче гемоглобинопати от одного из родителей (гетерозиготный тип наследования) носители патологического гемоглобина могут быть практически здоровыми людьми; при передаче гемоглобинопатии от обоих родителей (гомозиготный тип наследования) у детей возникает картина тяжёлого гемолиза. Наиболее распространены и отличаются тяжестью проявлений серповидноклеточная (дрепаноцитарная) анемия и талассемия.
Слайд 37
Серповидноклеточная анемия
Серповидноклеточная анемия (HbS) связана с наличием в
эритроцитах патологического гемоглобина S. При этой форме гемоглобинопатии эритроциты
в условиях снижения парциального давления кислорода в окружающей среде приобретают форму серпа. При увеличении в крови количества серповидных эритроцитов нарастает вязкость крови, замедляется кровоток, происходит разрушение серповидных эритроцитов, развиваются тромбозы в различных органах. У практически здоровых носителей HbS серповидность эритроцитов и появление признаков заболевания могут наступить лишь в условиях гипоксии. Поэтому всем носителям HbS противопоказаны служба в авиации, а также полёты на самолётах без достаточного кислородного обеспечения.
Слайд 38
Талассемия
Талассемия - заболевание, распространённое в средиземноморских странах. Характеризуется
значительным повышением содержания HbF в крови. Полагают, что при
этом образование нормального гемоглобина HbA подавлено. Нарушено также образование железосодержащей части гемоглобина (гема). Различают большую, малую и минимальную талассемию. При гетерозиготном наследовании развиваются малая, или минимальная, талассемия, при гомозиготном - большая. Для всех форм талассемии характерно наличие в крови "мишеневидных" эритроцитов, в которых гемоглобин расположен в центре клетки в виде мишени.
Признаки серповидноклеточной анемии и талассемии (задержка общего развития, анемия, желтушность, увеличение печени, селезёнки, изменения костей скелета) появляются с раннего детства. Осложнением серповидноклеточной анемии являются тромбозы сосудов кишечника, пигментные камни в жёлчных путях.
Слайд 39
Гемофилия
Гемофилия – Рецессивно наследуемое заболевание, сцепленное с Х-

хромосомой. Гемофилия А - нарушение синтеза фактора VIII (антигемофильного
глобулина А). Гемофилия В, или болезнь Кристмаса, - Нарушение синтеза фактора IX (антигемофильного глобулина В). Гемофилия С – аутосомно-рецессивно наследуемая болезнь, обусловленная нарушением синтеза фактора XI (антигемофильного глобулина С). Гемофилия А и В встречается у мужчин, женщины являются кондукторами болезни; гемофилия С поражает оба пола. Среди больных с наследственными коагулопатиями на гемофилию А приходится 68-79 %, на гемофилию В – 6-13 %, гемофилию С – 1-2 %. Дефицит факторов приводит к замедлению образования кровяного сгустка (тромба), который должен выполнить защитную роль, останавливая кровотечение из микрососудов (Диаметром более 100мкм).
Клиническая картина. Кровотечение и кровоточивость проявляются с детства (длительное кровотечение и плохое заживление пупочной ранки, подкожные, межмышечные, внутрисуставные гематомы, кровотечения после травм и операций, при смене молочных зубов, желудочно-кишечные и почечные кровотечения). Геморрагии особенно часты и выражены у больных с тяжелой формой болезни ( уровень антигемофильного фактора – от 0,5 до 2%); у больных со средними и легкими формами ( антигемофильный фактор – от 2,5 до 30%), а также у больных с гемофилией С спонтанная кровоточивость менее характерна. Для таких больных опасны любые оперативные вмешательства, осложняющиеся обильными и длительными кровотечениями. Повторяющиеся кровоизлияния в локтевые, голеностопные суставы, межмышечные и внутримышечные гематомы ( гематомный тип кровоточивости) ведут к хроническим артрозам, контрактурам, атрофии мышц, псевдоопухолям брюшной полости, суставах, мышцах бедра. Последствия кровотечений и частых трансфузий приводят к аутоиммунным синдромам: появление антител к VIII и IX факторам (ангибиторная форма гемофилии), развитие вторичного ревматоидного синдрома, амилоидоз почек, аутоиммунная анемия.
Слайд 40
Тромбофилии
ТРОМБОФИЛИИ ГЕМАТОГЕННЫЕ – состояния, характеризующиеся наклонностью к развитию

рецидивирующих тромбозов кровеносных сосудов (преимущественно вен) разной локализации вследствие
нарушений состава и свойств крови.
Этиология, патогенез. Различают две основные группы гематогенных тромбофилий:
связанные преимущественно с изменениями реологических свойств и клеточного состава крови;
обусловленные первичными нарушениями в системе гемостаза.
В первой группе выделяют формы, связанные с избытком клеток крови и ее сгущением (полицитемия, эритроцитозы, тромбоцитемии и др.), с нарушениями формы и деформабельности эритроцитов (например, множественные тромбозы и инфаркты при серповидноклеточной анемии), с повышением вязкости плазмы.
Во второй группе выделяют формы:
связанные с повышением афегационной функции тромбоцитов (в том числе вследствие нарушения равновесия между стимуляторами и ингибиторами афегации в плазме крови);
связанные с гиперпродукцией и гиперактивностью фактора Виллебранда;
связанные с дефицитом или аномалиями основных физиологических антикоагулянтов-антитромбина III, белков С и S;
связанные с дефицитом или аномалиями факторов свертывания крови и компонентов фибринолитической и калликреинкининовой системы (дефицит фактора XII, плазменного прекалликреина, высокомолекулярного кининогена, активатора плаэминогена, ряд молекулярных аномалий фибриногена и др.).
Все эти нарушения могут быть наследственными, т. е. генетически обусловленными, и приобретенными (симптоматическими).
Слайд 41
Нарушение функций почек
Фосфат-диабет
Наследственный нефрит
Слайд 42
Фосфат-диабет
ФОСФАТ-ДИАБЕТ – доминантно сцепленное с Х-хромосомой заболевание с

глубокими нарушениями фосфорно-кальциевого обмена, которые не удается восстановить обычными
дозами витамина D. В связи с этим появилось другое название болезни - рахит, резистентный к витамину D; однако в действительности речь идет не о рахите, но о рахитоподобном заболевании.
Этиология, патогенез. Предполагают, что при фосфат-диабете нарушены энзиматические процессы преобразования витамина D в активные гормоноподобные субстанции или снижена чувствительность рецепторов эпителия кишечника к действию этих метаболитов. Характерными биохимическими признаками являются фосфатурия, гипофосфатемия, повышение активности паращитовидных желез, высокая активность щелочной фосфатазы крови. Реабсорбция кальция в кишечнике снижена.
Клиническая картина. Фосфат-диабет имеет сходные черты с обычным D-дефицитным рахитом, но и отличается от него тем, что при данном заболевании отсутствуют признаки общей интоксикации, общее состояние остается удовлетворительным. В отличие от рахита процессы остеомаляции и остеоидной гиперплазии выражены преимущественно в костях нижних конечностей (искривление длинных трубчатых костей или деформация коленных и голеностопных суставов). Клинически фосфат-диабет проявляется не в первые месяцы жизни, а во втором полугодии жизни, после того как дети начинают вставать на ножки.
Содержание фосфора в крови больных снижено до 15-20 мг/л, уровень кальция не изменен. Значительное повышение экскреции фосфатов с мочой (в 4-5 раз выше нормы) наблюдается непостоянно и зависит от активности патологического процесса.
Слайд 43
Наследственный нефрит
НАСЛЕДСТВЕННЫЙ НЕФРИТ. Этиология, патогенез не изучены. Предполагается,

что заболевание связано с мутацией гена, контролирующего синтез структурных
белков почечной ткани, а также других органов. Существует два варианта наследственного нефрита - синдром Альпорта и гематурический нефрит. Более тяжелое течение болезни наблюдается у лиц мужского пола, что свидетельствует о возможности наследования по доминантному типу, частично сцепленному с полом.
Клиническая картина. Гематурический вариант начинается незаметно, мочевой синдром выявляется случайно. Отеки и артериальная гипертензия отсутствуют, но появляются при развитии почечной недостаточности, как правило, в подростковом возрасте или у взрослых. Мочевой синдром характеризуется эритроцитурией различной степени - от незначительного увеличения количества эритроцитов до макрогематурии. Обнаруживают также умеренную протеинурию и у некоторых детей - преходящую лейкоцитурию. Бактериурии, как правило, не бывает. Биохимическое исследование крови не выявляет выраженных сдвигов, у некоторых детей может наблюдаться нерезкая диспротеинемия и гиперлипидемия. Парциальные функции почек в течение длительного периода остаются ненарушенными, иногда выявляется гипераминоацидурия перегрузочного или ренального типа. Более тяжелые проявления характеризуют синдром Альпорта, при котором имеется сочетание поражения почек, глаз и тугоухости. В связи с тем что тугоухость развивается в поздних стадиях болезни, раннее дифференцирование синдрома Альпорта может оказаться затруднительным. Поражение слуха обусловлено поражением слухового нерва или кохлеарного аппарата и у некоторых больных выявляется только при аудиометрическом исследовании. У большинства детей с наследственным нефритом обнаруживаются стигмы дизэмбриогенеза в виде анатомических аномалий строения мочевой системы, а также внешние стигмы (гипертелоризм, аномалии строения ушных раковин, пальцев рук и ног). Для тяжелых форм наследственного нефрита характерно прогредиентное течение с постепенным развитием хронической почечной недостаточности.
Слайд 44
Болезни нервной системы
Эпилепсия
Миопатия
Лейкодистрофии
Торсионная дистония
Атаксия Фридрейха
Болезнь Верднига-Гоффманна
Слайд 45
Эпилепсия
ЭПИЛЕПСИЯ – хроническое заболевание головного мозга, характеризующееся повторными

приступами, которые возникают в результате чрезмерной нейронной активности и
сопровождаются различными клиническими и параклиническими проявлениями. В основе эпилепсии лежит повышенная нейронная активность с высоковольтными гиперсинхронными разрядами (эпилептический очаг). Наиболее часто эпилептические приступы встречаются в детском возрасте. Приступы у детей характеризуются не только высокой частотой, но и большей степенью выраженности. Именно в период, когда идет интенсивное развитие мозга, приступы могут привести к вторичным изменениям со стороны психики ребенка. У детей различные судорожные состояния встречаются в 5-10 раз чаще, чем у взрослых, В происхождении эпилепсии основное значение имеет взаимодействие наследственной предрасположенности и поражения головного мозга. При большинстве форм эпилепсии отмечается полигенная наследственность, причем в одних случаях она имеет большую, в других - меньшую значимость. Наследственность является важным фактором в развитии эпилепсии. При анализе наследственности нужно учитывать прежде всего явные признаки болезни, придавая определенное значение и таким ее проявлениям, как заикание, учитывать характерологические особенности личности (конфликтность, злобность, педантизм, назойливость). К предрасполагающим факторам относятся органические церебральные дефекты перинатального или приобретенного (после нейроинфекций или черепно-мозговой травмы) характера.
Слайд 46
Миопатия
Миопатия (от mio и греч. páthos - страдание,
болезнь) – прогрессирующие мышечные дистрофии; относятся к наследственным заболеваниям.
Миопатии могут передаваться по аутосомно-рецессивному, доминантному и сцепленному с полом типам. В основе развития миопатии лежат нарушение обмена в мышечных клетках, изменение синтеза нуклеиновых кислот, значительное преобладание ускоренного распада белков мышц над измененным их синтезом. Мышцы при миопатии истончены, часть волокон замещена жировой тканью; при электронной микроскопии обнаруживают изменение структуры мембран мышечных клеток. Основные признаки миопатии - нарастающая мышечная слабость, симметричная атрофия мышц, снижение сухожильных рефлексов, в поздних стадиях - деформация костей и суставов. Постоянно выражены вегетативнотрофические расстройства.
Слайд 47
Лейкодистрофии
Метахроматическая лейкодистрофия (лейкодистрофия Шольца-Гринфилда) относится к болезням накопления

липидов. Основным патогенетическим механизмом дебюта и эволюции МЛ является
генетически детерминированное снижение активности лизосомной арилсульфатазы А. Это редкое (встречается с частотой 1:40000) наследственное аутосомно-рециссивное заболевание характеризуется хроническим прогредиентным течением. Симптомы появляются на втором или третьем году жизни ребенка. Основные признаки МЛ: расстройства сна, нарушения осанки, постепенное исчезновение речевой способности, прогрессирующие амавроз и глухота, спастические парезы (постепенно переходящие в децеребрационную регидность), умственная отсталость. В финале болезни у пациентов МЛ летальный исход наступает через 1-3 года. При гистоморфологическом исследовании нервной ткани выявляется метахромазия миелиновых оболочек, жировая дистрофия нервных клеток, главным образом отложения липидов в зубчатом ядре, но и в других группах ядер головного и спинного мозга.
Болезнь Краббе-Бенеке – наследуемая энцефалопатия детского возраста с быстро прогрессирующей церебральной дегенерацией, демиелинизацией, проявляющаяся повышением мышечного тонуса, приступами гиперпирексии и нарушениями интеллекта. Обычно дебютирует в возрасте 3-6 мес. Этиология и патогенез. Недостаточность галэктозилцерамид|3-галактозидазы приводит к накоплению галактозил-сфингозина в мозге, периферических нервах, почках, выраженному астроцитарному глиозу, инфильтрации белого вещества мозга характерными многоядерными клетками, демиелинизации.
Клиническая картина: ранняя инфантильная форма (начало в 3-6 мес.); I стадия: повышенная возбудимость ребёнка, двигательная реакция (тонические судороги) на звук, свет и т.д.; повышение мышечного тонуса, замедление развития, приступы гиперпирексии; II стадия: развитие опистотонуса с тоническим разгибанием рук и ног, утрата всех навыков, миоклонии, судорожные припадки, гипо- или арефлексия, приступы гиперпирексии; III стадия: децеребрация, бульварные расстройства, судороги; поздняя инфантильная форма: раннее развитие амавроза, постепенное нарушение интеллекта и движений.
Слайд 48
Торсионная дистония
ТОРСИОННАЯ ДИСТОНИЯ – наследственное заболевание нервной системы,

характеризующееся нарушением мышечного тонуса и своеобразными двигательными расстройствами -
вращательными гиперкинезами.
В основе заболевания лежит поражение клеток подкорковых образований головного мозга и зубчатого ядра мозжечка. Чаще наблюдаются единичные случаи болезни, но иногда заболевают несколько членов одной семьи. Характерные для заболевания гиперкинезы и судороги могут быть симптомом других заболеваний - эпидемического энцефалита, гепатоцеребральной дистрофии, опухоли мозга и др.
Заболевание чаще начинается в возрасте 10-15 лет. В мышцах туловища и конечностей появляются медленные тонические спазмы, приводящие к искривлению тела с вращением его вокруг продольной оси (торсионный спазм, вращательный спазм). Эти спазмы охватывают мышцы спины, шеи, туловища, тазового пояса и конечностей, приводя к причудливым позам: развивается искривление спины, туловище выгибается в сторону или вперед, голова запрокидывается назад, руки отводятся назад или с силой приводятся к туловищу. Эти гиперкинезы наступают пароксизмально и резко усиливаются при всякой попытке к движению, в результате чего больные с большим трудом ходят и даже стоят. В состоянии покоя спазмы уменьшаются, во сне исчезают. Остальные функции нервной системы и психика обычно остаются сохранными.
Помимо генерализованных форм, наблюдаются и локальные формы торсионной дистонии., при которых спазмы охватывают отдельные мышцы шеи (спастическая кривошея) или только одной конечности по типу писчего спазма. Локальная торсионная дистония начинается в более позднем возрасте и протекает более благоприятно.
Слайд 49
Атаксия Фридрейха
Наследственное прогрессирующее заболевание нервной системы, характеризующееся нарушением

координации, спастическими явлениями и изменениями скелета. В основе болезненного
процесса лежит дегенерация проводящих путей задних и боковых столбов спинного мозга, реже мозжечка.
Клиническая картина. Первым проявлением болезни является постепенное нарушение походки: она становится неуверенной, шатающейся. Чтобы не упасть, больной идет, широко расставив ноги. Позже неустойчивость появляется и в положении стоя. Со временем атаксия распространяется на мышцы рук и языка. Речь становится скандированной. Мышечный тонус вначале снижен, сухожильные рефлексы отсутствуют или вызываются с трудом. Позже в процесс вовлекаются пирамидные пути и возникает картина нижнего спастического парапареза с характерной гиперрефлексией, повышением тонуса мускулатуры, патологическими рефлексами. Обнаруживаются признаки поражения мозжечка — дисметрия, адиадохокинез, нистагм. Снижены глубокие виды чувствительности, главным образом на ногах, при сохранении болевой и тактильной чувствительности. Больные жалуются на боли, парестезии. Характерны деформации скелета — кифо-сколиоз и так называемая стопа Фридрейха (высокий свод, в разогнутом положении основные фаланги при согнутом положении концевых).
Часто наблюдается постепенное снижение психических функций. Кровь и цереброспинальная жидкость не изменены. Интеркуррентные заболевания ухудшают состояние больных.
Слайд 50
Болезнь Вердинга-Гоффмана
(амиотрофия наследственная спинальная)
Аутосомно-рецессивное наследственное заболевание нервно-мышечной системы.
Происходит дегенерация клеток передних рогов спинного мозга.
Клиническая картина.
Ребенок перестает опираться на ноги, утрачивает способность сидеть, удерживать игрушки. Слабость с последующей атрофией распространяется одновременно на проксимальные и дистальные отделы конечностей. В положении сидя возникает выраженный кифоз вследствие слабости мышц спины. Отмечается раннее симметричное выпадение сухожильных и надкостничных рефлексов. Характерны фасцикулярные подергивания мышц, особенно мышц языка.
Прогноз. При ранней детской форме амиотрофии болезнь быстро прогрессирует, приводя к полной обездвиженности. При поздней детской форме дети не теряют способности к передвижению. Ухудшают прогноз частые бронхиты, пневмонии.
Слайд 51
Поражения глаз
Синдром Лоу
Дегенерация роговицы Бюклерса
Ретинобластома
Хориоидеремия
Слайд 52
Синдром Лоу
Синдром Лоу – наследственная болезнь, характеризующаяся карликовостью,
поражением глаз (катаракта и глаукома), умственной отсталостью, нарушением выделительной
функции почек, изменениями в скелете. У детей: симптомы, напоминающие поздний рахит. У взрослых: симптомы остеомаляции. Системный остеопороз, множественные зоны патологической перестройки. Искривление ключиц, сколиоз, варусные бедра, вальгусные колени. Могут быть патологические переломы.
Слайд 54
Дегенерация роговицы Бюклерса
Дегенерация роговицы Бюклерса — наследственная болезнь
глаз, проявляющаяся в детском возрасте и характеризующаяся болевыми ощущениями
и гиперемией в области глазного яблока, снижением чувствительности роговицы, дефектами ее переднего эпителия, нарушением целости передней пограничной пластинки (боуменовой оболочки) с появлением в ней полосчатых помутнений; наследуется по аутосомно-доминантному типу.
Слайд 55
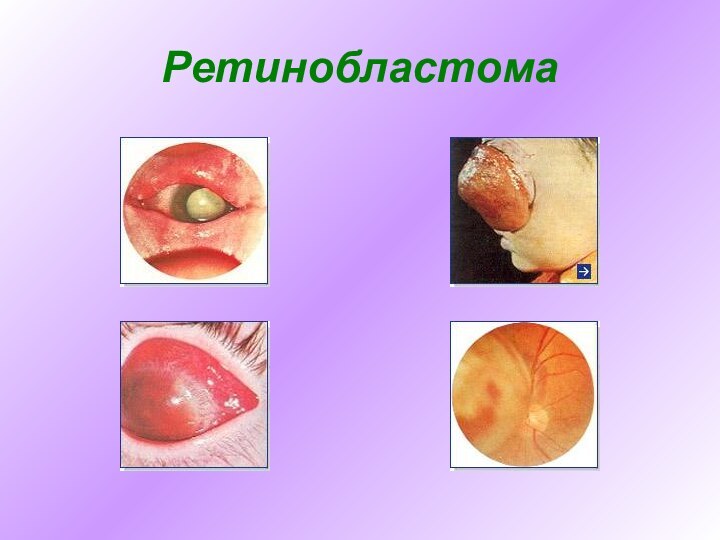
Ретинобластома
Ретинобластома – злокачественная опухоль глаза, развивающаяся преимущественно в

детском возрасте из тканей эмбрионального происхождения. Пик заболевания приходится
на 2 года. Почти все случаи заболевания выявляются до 5-летнего возраста. Распространенность ретинобластомы небольшая – примерно 1 случай на 20 000 новорожденных. На территории Европы заболевание встречается почти в 4 раза реже, чем в Азии.
Ретинобластома может быть: односторонней или двусторонней.
Двусторонняя форма заболевания встречается примерно у каждого четвертого пациента и в большинстве случаев носит наследственный характер.
Односторонние же опухоли, как правило, ненаследственные, но имеется четкая связь заболевания с хромосомными аберрациями.
Как правило, речь идет о делеции участка длинного плеча одной из хромосом 13 пары с повреждением гена RB1. Данное повреждение характерно как для ретинобластомы, так и для остеосаркомы. Считается, что ретинобластома развивается из нейроэктодермы сетчатки. При этом опухолевые клетки имеют разную степень дифференцировки. Для опухолей больших размеров характерны очаги некрозов и кальцификатов. Ретинобластома представлена недифференцированными мелкими клетками с крупным ядром. Типичны множественные очаги роста опухоли на сетчатке. Большинство пациентов погибают от метастазов в ЦНС по зрительному нерву, а также метастазов в кости и костный мозг по крови.
Слайд 57
Хориоидеремия
Хориоидеремия – наследственная болезнь глаз, проявляющаяся понижением
остроты зрения, концентрическим сужением полей зрения, гемералопией и близорукостью,
что сопровождается характерными изменениями глазного дна (почти полное отсутствие сосудистого рисунка, резкие контуры и красновато-коричневый цвет желтого пятна, нечеткость границ диска зрительного нерва). Наследуется по аутосомно-рецессивному и сцепленному с полом рецессивному типу.
Слайд 58
Болезнь Вильсона-Коновалова
Болезнь Жильбера
Болезнь Рандю-Вебера-Ослера
Болезнь Виллебранда
Глютеновая энтеропатия (целиакия) взрослых
Болезни
пищеварительной
системы
Слайд 59
Болезнь Вильсона-Коновалова
Аутосомно-рецессивное наследственное заболевание, связанное с нарушением функции

печени и обмена меди.
Этиология и патогенез. В связи
с нарушенным синтезом церулоплазмина возникают дегенеративные изменения в подкорковых узлах (преимущественно в чечевицеобразных ядрах).
Клиническая картина. Часто задолго до появления неврологических расстройств обнаруживаются заболевания печени в виде гепатита, желтухи, геморрагического диатеза. Прогрессирующее заболевание печени приводит к циррозу. При брюшной форме болезнь протекает по типу подострой дистрофии печени, и больной умирает в состоянии печеночной комы до возникновения неврологических расстройств. В остальных случаях неврологическая симптоматика быстро занимает ведущее место. Появляется дрожание рук, нарастает тонус мускулатуры, возникают выраженная ригидность, амимия; движения становятся замедленными. Ригидность осложняется контрактурами. Возникают клонические и тонические судороги. Затруднения при выполнении движений возрастают, большую часть времени больной проводит в неподвижном состоянии. Ввиду длительных спазмов мускулатуры возникают различные вычурные позы. Появляются насильственные движения: гиперкинезы типа атетоза, насильственный плач, смех. Чувствительность не изменена. Сухожильные рефлексы оживлены. Наблюдаются снижение памяти, эйфория, плаксивость, в дальнейшем — неуклонное снижение интеллекта. Типично появление по периферии роговицы зеленовато-желтого или зеленовато-коричневого пигмента (кольцо Кайзера— Флейшера). У детей наблюдаются несколько форм заболевания.
Слайд 60
Болезнь Жильбера.
Болезнь Жильбера (пигментный гепатоз, ювенильная перемежающаяся желтуха)

относится к наследственным доброкачественным хроническим заболеваниям, передающимся по аутосомно-доминантному
типу. Она встречается в среднем у 5% населения с колебаниями в различных географических регионах от 3 до 7 %, чаще у мужчин во 2-ой и 3-ей декадах жизни.
В патогенезе заболевания основную роль играют нарушения транспортной функции белков, доставляющих неконъюгированный билирубин (красящееся вещество, образующееся при разрушении эритроцитов) к гладкому эндоплазматическому ретикулуму (микросомам) гепатоцитов, а так же неполноценность фермента микросом, при помощи которого осуществляется конъюгация (соединение) билирубина с глюкуроновой и другими кислотами. В 2/3 случаев болезнь Жильбера клинически впервые появляется в связи с острым заболеваниями различного характера (в исходе вирусного гепатита, инфекционного мононуклеоза, токсических поражений печени различной этиологии и др.) и стрессовыми ситуациями (физическое и психическое переутомление, переохлаждение др.). Появление желтушности склер, кожи и гипербилирубинемии после перенесенного вирусного гепатита даже при неизмененных функциональных пробах печени зачастую приводит к ошибочному диагнозу хронического гепатита и назначению соответствующего лечения, которое не дает заметного эффекта.
Первым и ведущим клиническим проявлением болезни Жильбера является хроническая или интермиттирующая желтуха. Ее интенсивность колеблется от субиктеричности склер до достаточно выраженной желтушности кожи и слизистых оболочек. Она усиливается при интеркуррентных заболеваниях, переутомлении, физической нагрузке, употреблении алкоголя. Примерно у 1/3 больных жалобы отсутствуют, а у 2/3 отмечаются астенические явления, тупая боль в верхней половине живота. Печеночные знаки, как правило, отсутствуют. Печень нормальной консистенции, гладкая, безболезненная, у ¼ больных постоянно, но незначительно увеличена - край ее на 1 – 3 см выступает из-под реберной дуги. В периоды обострений такое же увеличение отмечается чаще, у 4/5 больных. Селезенка не увеличена.
Основной признак болезни – умеренная гипербилирубинемия (значительное количество билирубина). Чаще колебания уровня общего билирубина наблюдаются в пределах 25 – 75 мкмоль/л. Изредка встречается повышение уровня билирубина до 120 мкмоль/л. У 20% больных наблюдаются изменения, характерные для хронического холецистита.
Слайд 61
Болезнь Рондю-Вебера-Ослера
Болезнь обусловлена наследственной, передаваемой по аутосомно-доминантному типу
неполноценностью сосудистого эндотелия, что приводит к ранимости сосуда, его
расширению и удлинению.
Клиническая картина. На коже лица, слизистой оболочке носа, губ, пищеварительного тракта образуются телеангиэктазии, которые легко травмируются и дают массивные кровотечения.
Слайд 62
Болезнь Виллебранда
Наследственная комбинированная геморрагическая гемостазиопатия, которая встречается у
мужчин и женщин. Наследуется по аутосомно-доминантному типу.
Клиническая картина. Нарушается
сосудисто-тромбоцитарный и вторичный гемостаз, поэтому у больных отмечается кровоточивость по микроциркуляторному (кровоизлияния в кожу, слизистые оболочки, носовые, десновые, почечные, желудочно-кишечные, меноррагии) и макроциркуляторные (межмышечные и подкожные гематомы и кровоизлияния в суставы) типам.