Слайд 2
Определение
ТАРГЕТНАЯ терапия в онкологии – это терапия
направленного действия, то есть, воздействия на опухолевые «мишени» (белки,
рецепторы, гены), имеющие важнейшее («критическое») значение для развития новообразования.
Благодаря направленному действию целевые препараты поражают в основном опухолевые клетки и практически не повреждают здоровые органы и ткани, на которых мишени отсутствуют или их повреждение не является критичным.
Слайд 3
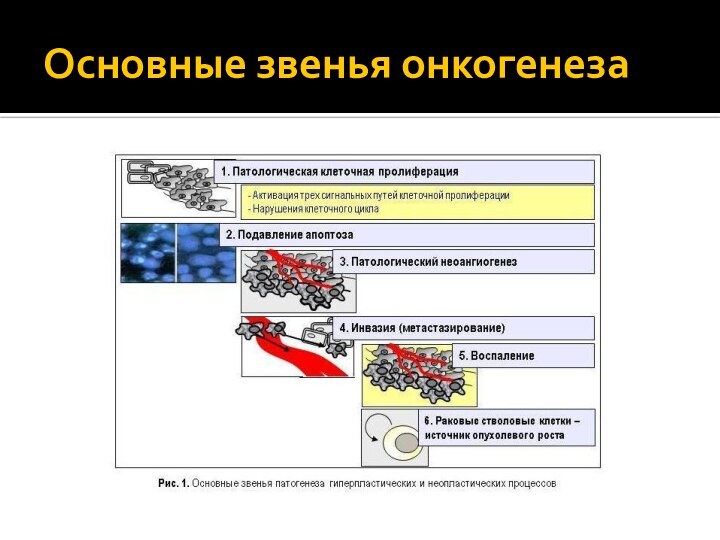
Онкогенез
Онкогенез-многоступенчатый процесс включает в себя:
генетические изменения
трансформация
нормальных
клеток в опухолевые
(нарушение клеточной пролиферации,
ангиогенеза, апоптоза)
При целевой терапии проводят точечное воздействие на указанные выше причины онкогенеза.
Слайд 5
Механизм действия
Предназначенные для таргентной терапии препараты обладают разными
механизмами действия. Некоторые из них являются моноклональными антителами -молекулами,
подобными тем, которые возникают в организме как иммунный ответ на инфекционное вторжение . Другие подавляют функцию ферментов, которые участвуют в передаче сигнала, необходимого для запуска деления клетки. Третьи – блокируют образование новых сосудов в опухоли, необходимых для ее питания и роста. Таким образом, каждый препарат направленно воздействует на какую-то одну мишень, играющую ключевую роль в развитии опухолевой клетки.
Слайд 6
Механизм действия
Строение рецепторов фактора роста:
- экстрацеллюлярный домен,
ответсвенный за соединение с лигандом (фактором роста)
- трансмембранная липофильная часть
- интрацеллюлярный домен, представляющий собой
тирозинсодержащие киназы, с активации которых начинается
каскад последующих реакций по передаче сигнала
на белки‐переносчики
В норме после связывания EGFR c соответствующим лигандом и VEGF с соотвествующим рецептором VEGFR
происходит активация рецепторов, что индуцирует последующую активацию нескольких сигнальных путей (RAS/RAF/MAPK, STAT , PI3K/Akt),
для трансдукции митогенного сигнала от рецептора к ядру клетки (рис 1.)
Слайд 7
Механизм действия
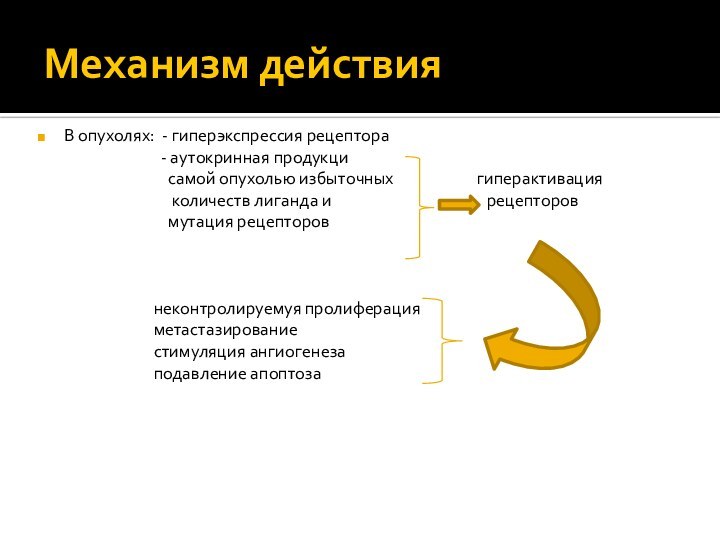
В опухолях: - гиперэкспрессия рецептора
- аутокринная продукци
самой опухолью избыточных гиперактивация
количеств лиганда и рецепторов
мутация рецепторов
неконтролируемуя пролиферация
метастазирование
стимуляция ангиогенеза
подавление апоптоза
Слайд 8
Таргтные препараты
Исходя из этих данных, в качестве противоопухолевых
агентов
предложено использовать моноклональные антитела к:
- EGFR (цетуксимаб, панитумумаб) –
блок сигнальных путей, апоптоз
- VEGF (бевацизумаб) реагирует с участком VEGF, ответственным
за связывание с соответствующим рецептором, что блокирует
образование ангиогенного сигнала и, как следствие подавляет неоангиогенез.
Слайд 9
Таргетные препараты
к семейству рецепторов эпидермального фактора роста ІІ
типа также относят
рецептор Her-2/neu, присутствующий
и в нормальных тканях молочной железы человека — в среднем 20 000–50 000 рецепторов на поверхности клетки, однако их количество возрастает до 1 000 000 и более на поверхности раковых клеток(HER2-позитивный рак груди)
Герцептин – очень эффективный препарат в лечении HER2-позитивного рака груди у женщин на II, III и IV стадиях рака. Герцептин назначается обычно внутривенно один раз в 1 – 3 недели.
Слайд 10
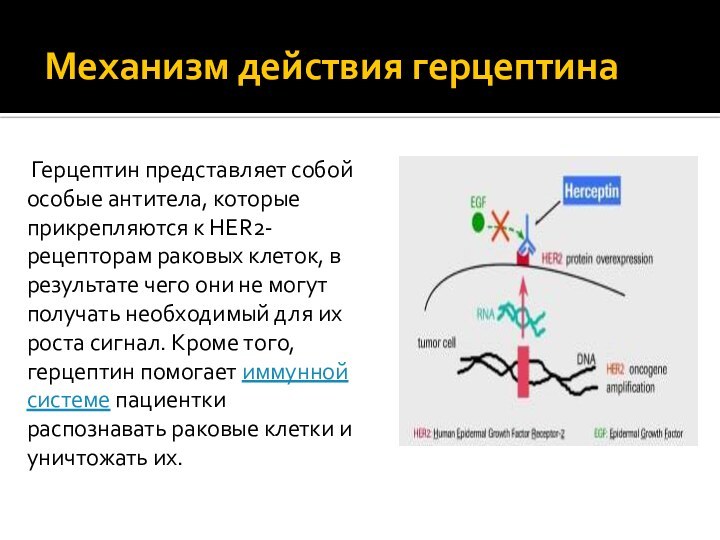
Механизм действия герцептина
Герцептин представляет собой особые антитела,
которые прикрепляются к HER2-рецепторам раковых клеток, в результате чего
они не могут получать необходимый для их роста сигнал. Кроме того, герцептин помогает иммунной системе пациентки распознавать раковые клетки и уничтожать их.
Слайд 11
Просто примите таблетку
Подавляющее число препаратов для таргетной терапии
выпускается в виде таблеток. Это позволяет больным не находиться
в стационаре и зачастую чувствовать себя настолько хорошо, чтобы продолжать работать.
Несомненным преимуществом является также и низкая токсичность, не требующая частого контроля показателей крови, госпитализации при развитии осложнений.
Слайд 12
Благодаря усилиям ученых сегодня в клинической практике уже
используется более 10 препаратов с молекулярно-направленным действием. Несколько десятков
проходят апробацию в клинических исследованиях. Их появление на фармацевтическом рынке ожидается в ближайшие годы.
Параллельно продолжается процесс изучения молекулярно-генетических особенностей опухолевой клетки. Он позволит пролить свет на уязвимые звенья ее развития и создать арсенал препаратов, достаточный не только для подавления роста, но и для полного разрушения злокачественных клеток. А это вселяет надежду на излечение человечества от столь грозного заболевания, как рак.