Слайд 2
Rozdělení
poruchy červené krevní řady (+/-)
poruchy bílé krevní
řady (+/-)
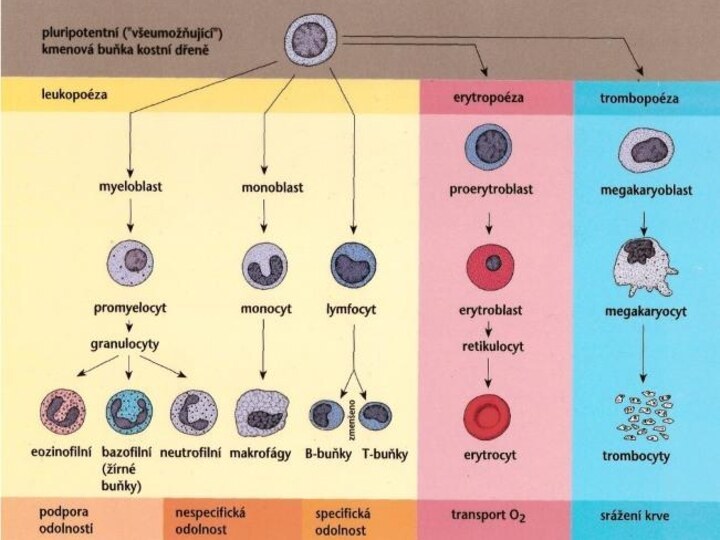
granulocyty – neutrofilní, eozinofilní a bazofilní
agranulocyty –
lymfocyty a monocyty.
krvácivé stavy (poruchy hemostázy)
trombofilní stavy
Слайд 4
Přežívání buněk
neutrofily 10 h
trombocyty 10 dnů
erytrocyty
100 dnů
Слайд 5
Poruchy červené krevní řady
Anémie
Polycytémie
Слайд 6
A.Anémie
= snížené koncentrace hemoglobinu v krvi
dělení dle etiologie
Anémie
ze snížené produkce ery
Anémie ze zvýšených ztrát ery
2.
dělení dle morfologie (velikosti) erytrocytů
makrocytární
normocytární
mikrocytární
Слайд 7
A.Anémie – ze snížené tvorby ery
1) Nedostatek erytropoetinu
Etiologie
Chronické
onemocnění ledvin (syntetozováno ↓množství erytropoetinu)
Proteinová malnutrice (chybí kyseliny pro
syntétu erytropoetinu)
↓ funkce hypofýzy nebo šť. žlázy (u nezralých novorozenců)
=anémie normocytární
Слайд 8
A.Anémie – ze snížené tvorby ery
2) buněčná porucha
krvetvorné tkáně
Etiologie
Ionizující záření (u aplastických A. - vyjma b.
kostní dřeně jsou postiženy i krvetvorné kmenové b.)
Toxické postižení buněk kostní dřeně
Слайд 9
A.Anémie – ze snížené tvorby ery
3) nedostatek Fe
Vyznačuje
se poruchou syntézy hemoglobinu v zárodečních buňkách erytroidní linie,
které je způsobeno nedostatkem železa v organismu.
Červené krvinky obsahují málo hemoglobinu, dochází ke snížení jejich středního objemu a rozvoji hypochromní mikrocytární anémie.
Nedostatek železa v organismu je způsoben nerovnováhou mezi jeho příjmem a ztrátami z organismu
Слайд 10
A.Anémie – ze snížené tvorby ery
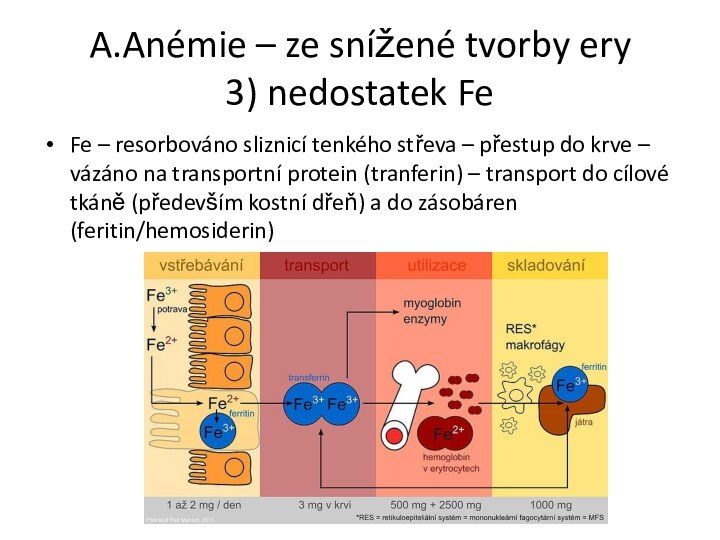
3) nedostatek Fe
Fe
– resorbováno sliznicí tenkého střeva – přestup do krve
– vázáno na transportní protein (tranferin) – transport do cílové tkáně (především kostní dřeň) a do zásobáren (feritin/hemosiderin)
Слайд 12
A.Anémie – ze snížené tvorby ery
3) nedostatek Fe
KO:
Snížení
zásob Fe - pokles hladiny sérového feritinu – dále
↓ hladiny Fe v séru
V kostní dřeni klesá množství sideroblastů
(za normálních okolností asi 50 % erytroblastů obsahuje granula barvitelná na železo, nazývají se sideroblasty. Jejich pokles pod 10 % z celkového počtu erytroblastů charakterizuje snížení dodávky železa erytroidním buňkám)
Слайд 13
A.Anémie – ze snížené tvorby ery
3) nedostatek Fe
Vzhledem
k velikosti erytrocytů a množství hemoglobinu v nich má
anémie charakter mikrocytární a hypochromní.
množství železa v kostní dřeni určuje velikost syntézy hemoglobinu
pokles hemoglobinu v erytrocytech určuje velikost erytrocytů a podmiňuje porušení strukturální integrity buněk, které snadněji podléhají destrukci.
Sideropenie rovněž omezuje dělící schopnost buněk kostní dřeně = kompenzační zvýšení produkce buněk ve dřeni je malé.
Anémie vzniká tedy proto, že nedostatek železa snižuje syntézu hemoglobinu a také snižuje schopnost kostní dřeně odpovídat na anémii zvýšenou produkcí erytroidních buněk.
Слайд 14
A.Anémie – ze snížené tvorby ery
4) nedostatek kyseliny
listové a B12
Kyselina listová
nutná pro syntézu thymidinových nukleotidů,
stavebních kamenů DNA.
k zajištění funkce kyseliny listové je nezbytný vitamin B12 - umožňuje zachování stálé hladiny tetrahydrofolátu.
Vitamin B12
resorbován v tenkém střevě po vytvoření komplexu vit. B12- vnitřní faktor.
Vnitřní faktor je secemován parietálními buňkami žaludeční sliznice a pro resorpci vitaminu B12 je nezbytný.
Слайд 17
A.Anémie – ze snížené tvorby ery
4) nedostatek kyseliny
listové a B12
Klíčovým patogenetickým mechanismem je porucha syntézy DNA
- část buněk červené řady zaniká v kostní dřeni před uvolněním do krevního oběhu (neefektivní erytropoeza).
Porucha buněčného dělení je patrna nejen v krvetvorné tkáni, ale také v ústní dutině (vyhlazení povrchu jazyka) a ve střevní sliznici.
Při nedostatku vitaminu B12 je prodlouženo trvání S-fáze buněčného cyklu, syntéza RNA a proteinů probíhá normálně. To má za následek zvětšení objemu erytroblastů (tyto buňky se nazývají megalo- blasty) a také erytrocytů (makrocyty).
Výskyt megaloblastů a makrocytů řadí tento typ anémie mezi megaloblastové a makrocytární anémie.
Koncentrace hemoglobinu v erytrocytech je normální (0,32-0,34), avšak množství hemoglobinu v makrocytech je zvýšeno (app. 14), proto se také tento typ anémie nazývá hyperchromní.
Слайд 18
A.Anémie – ze zvýšených ztrát ery
1) akutní krevní
ztráta
Akutní krvácení zmenší celkový objem erytromasy.
Zásadní význam má
zmenšení náplně cévního řečiště.
Většina lidí dobře snáší krevní ztrátu 500 až 1000 ml krve (10 až 20 % krevního objemu).
Pokud je ztráta krve větší, mohou se objevit příznaky nedostatečné činnosti kardiovaskulárního systému a při ztrátě kolem 40-50 % krevního objemu se rozvíjí hypovolemický cirkulační šok
Velmi brzy po akutní krevní ztrátě (hodiny) je v plazmě možno zjistit zvýšenou hladinu erytropoetinu, nové erytrocyty se začínají objevovat přibližně za týden po krvácení.
Z morfologického hlediska má anémie charakter normochromní a normocytární.
Слайд 19
A.Anémie – ze zvýšených ztrát ery
2) chronická krevní
ztráta
Chronické krvácení se často objevuje při krvácení do dutiny
zažívacího traktu, vzniká však i z jiných příčin.
V časných fázích se kompenzačně zvyšuje erytropoeza, což se projeví jen mírnou anémií s vysokým počtem retikulocytů.
S erytrocyty ztracenými krvácením se však z organismu ztrácí železo a po vyčerpání zásob železa v organismu se anémie prohlubuje a mění charakter na mikrocytární a hypochromní.
Слайд 20
A.Anémie – ze zvýšených ztrát ery
3) hemolytická anémie
Hemolýza
= rozpad červených krvinek.
Erytrocyty žijí přibližně za 100
až 120 dnů.
Pokud je doba života erytrocytů zkrácena, hovoříme o hemolytickém stavu.
Erytrocyty mohou zanikat
extravaskulárně, zejm. ve slezině, kde jsou pohlceny makrofágy (přirozený mechanismus likvidace starých buněk)
nebo zanikají v cévách – intravaskulárně.
Слайд 21
A.Anémie – ze zvýšených ztrát ery
3) hemolytická anémie
Při
extravaskulárním zániku
v makrofázích odštěpen hem od globinu
globin je
degradován na jednotlivé aminokyseliny
z hemové skupiny nakonec vznikne žlučové barvivo – bilirubin.
Слайд 22
A.Anémie – ze zvýšených ztrát ery
3) hemolytická anémie
Při
intravaskulárním rozpadu
globinová složka ve formě dimerů vázána na
plazmatickou bílkovinu haptoglobin
hemová skupina je vázána na další plazmatický protein - hemopexin.
Hemoglobin, který není navázán na haptoglobin, je filtrován v ledvinných glomerulech a je pak zpětně resorbsnán tubulárními buňkami. V nich dochází k degradaci globinu na aminokyseliny a uvolněné železo je skladováno ve formě hemosiderinu. Tubulární buňky se odlupují a s nimi přechází železo do moči (hemosiderinurie). Část přefiltrovaného hemoglobinu se může dostat do moči přímo, vzniká hemoglobinurie, která může ledviny poškodit.
Слайд 23
A.Anémie – ze zvýšených ztrát ery
3) hemolytická anémie
Pro
většinu hemolytických anémií je charakteristická kompenzační odpověď krvetvorné tkáně
= zvýšenou buněčností kostní dřeně, převažují buněčné prekurzory erytrocytů, v krvi se zvýšená tvorba buněk červené řady projeví zvýšeným počtem retikulocytů (retikulocytózou).
Protože degradačním produktem hemu je bilirubin, bývají hemolytické anémie provázeny žloutenkou - ikterem
Слайд 24
A.Anémie – ze zvýšených ztrát ery
3) hemolytická anémie
Hemolytické
anémie jsou způsobeny:
vnitřním defektem erytrocytů
poškozením erytrocytů zevními
faktory
Слайд 25
A.Anémie – ze zvýšených ztrát ery
4) hemolytická anémie
(vnitřní defekt ery)
=většinou vrozená x dědičná onemocnění
Příčinou zkráceného přežívání
erytrocytů v krvi může být:
porucha membrány erytrocytů (hereditární sférocytóza)
porucha enzymatické výbavy erytrocytů,
výskyt atypických hemoglobinů (hemoglobinopatie)
získaná porucha (paroxysmální noční hemoglobinurie)
Слайд 26
A.Anémie – ze zvýšených ztrát ery
4) hemolytická
anémie (vnitřní defekt ery)
Hereditární sférocytóza
Základním defektem je porucha buněčné
membrány vyvolaná deficitem membránových proteinů (spektrinu a ankyrinu)
Kostní dřeň vytváří normální bikonkávní erytrocyty, které však při průchodu slezinou ztrácejí část své membrány, protože proteinový cytoskelet je menší než lipidová dvojvrstva membrány.
Takto poškozená membrána je zvýšeně propustná pro natrium, které se v krvince hromadí spolu s vodou, a erytrocyt se postupně stává sférickým.
Nejprve vznikají „makrosférocyty“, při opakovaném průchodu erytrocytů slezinou je ztrácena i část cytoplazmatických lipidů a nakonec vznikají mikrosférocyty.
Vzhledem k částečné ztrátě membrány je zmenšena deformovatelnost erytrocytů, ty jsou pak ve slezině snadněji destruovány.
Sférocyty mají výrazně sníženou osmotickou rezistenci.
Слайд 27
A.Anémie – ze zvýšených ztrát ery
4) hemolytická anémie
(poškození ery zevnímy faktory)
Poruchy metabolismu erytrocytů
Enzymatický defekt postihující
anaerobní glykolýzu
Anaerobní glykolýzou je zpracováno 90 % glukózy dodané erytrocytu = hlavní zdroj energie pro červenou krvinku
Nejčastěji se vyskytuje defekt pyruvátkinázy… → hemolylický účinek
Th:
Splenektomie - částečná úprava hemolýzy
substituční léčba transfuzemi erytrocytů
Слайд 28
A.Anémie – ze zvýšených ztrát ery
4) hemolytická anémie
(poškození ery zevnímy faktory)
Hemoglobinopatie
podmíněna změnami molekuly hemoglobinu.
Tyto
změny mohou nastat:
poruchou syntézy globinových řetězců – těžká hemolýza
přítomností abnormálních hemoglobinů – srpkovitá anemie
Слайд 29
A.Anémie – ze zvýšených ztrát ery
4) hemolytická anémie
(poškození ery zevnímy faktory)
Hemoglobinopatie
Hb napomáhá k udržení funkce
a integrity erytrocytů. Při výskytu abnormálního hemoglobinu - srpkovitá anémie.
Onemocnění je způsobeno záměnou aminokyseliny. Takto změněný hemoglobin za podmínek hypoxie a posunu pH krve na kyselou stranu (např. po tělesné námaze) v erytrocytech gelovatí, mění tvar erytrocytů, které mají zkrácenou dobu života a snadno hemolyzují.
Слайд 30
A.Anémie – ze zvýšených ztrát ery
4) hemolytická
anémie (vnitřní defekt ery)
Paroxysmální noční hemoglobinurie
Čtvrtá skupina získaných hemolytických
stavu
Слайд 31
A.Anémie – ze zvýšených ztrát ery
4) hemolytická anémie
(poškození ery zevnímy faktory)
Hemolýza ze zevních příčin může vzniknout:
působením
tepelných a chladových autoprotilátek proti erytrocytům = Autoimunitní hemolytické anémie
Слайд 32
A.Anémie – ze zvýšených ztrát ery
4) hemolytická anémie
(poškození ery zevnímy faktory)
Hemolýza ze zevních příčin může vzniknout:
2. působením
dalších příčin
hemolýza po rozsáhlých popáleninách,
po otravě např. arzenem, fenylhydrazinem,
po aspirací vody,
působením některých hadích toxinů
erytrocyty mohou být poškozeny také mechanicky, např. umělými srdečními chlopněmi
Слайд 33
B.Polycytémie
Koncentrace hemoglobinu a erytrocytů v objemové jednotce krve
může být zvýšena :
relativně - při zmenšeném objemu plazmy
= primární polycytémie
absolutně - při zvýšení počtu erytrocytů v krvi, = sekundární polycytémie
Слайд 34
B.Polycytémie - reaktivní
Vzniká následkem dehydratace organismu
zmenšení objemu
extracelulární tekutiny
nejedná o poruchu krvetvorby ale o poruchu regulace
krevního objemu
Слайд 35
B.Polycytémie - primární
= Vaquezova nemoc
zvýšení počtu erytrocytů v
krvi
zvyšuje se počet granulocytů, monocytů a trombocytů
= klonální onemocnění
- je postižena pluripotentní myeloidní kmenová buňka. Obě unipotentní buňky z ní vzniklé vykazují zvýšenou citlivost vůči erytropoetinu, což se projeví zejména zvýšenou produkcí erytrocytů, při čemž hladina erytropoetinu je snížena oproti jeho hladině u zdravých jedinců.
→ zvyšuje viskozitu krve + trombotizace arterií (příčinou smrti trombóza koronárních + mozkových tepen).
Слайд 36
B.Polycytémie - sekundární
Vznik podmíněn zvýšenou tvorbou erytropoetinu.
Např.
při poruše přísunu kyslíku tkáním
případně (vzácněji) při jeho primárně
zvýšené produkci u některých malignit a ledvinných poruch
K polycytémii může také dojít po, často nekontrolovaném, podání exogenního erytropoetinu (doping u sportovců).
Při polycytémii dochází ke zvětšení hematokritu
Organismus je ohrožen především vzestupem viskosity krve → poruchy mikrocirkulace v životně důležitých systémech (myokard, CNS).
Слайд 37
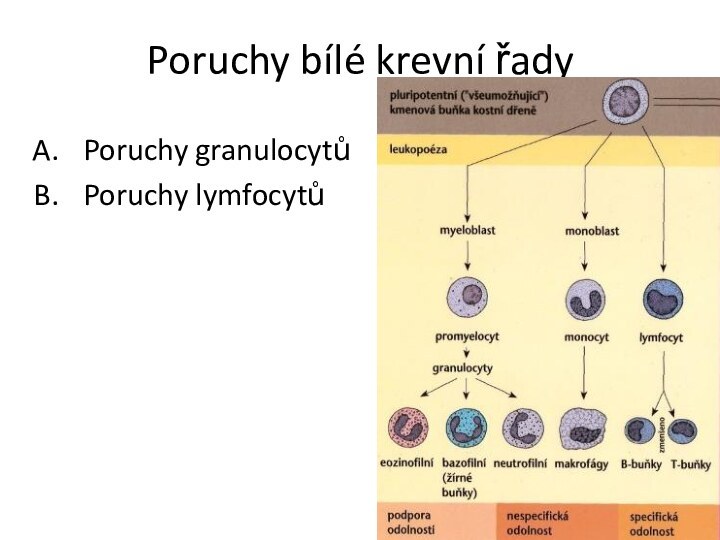
Poruchy bílé krevní řady
Poruchy granulocytů
Poruchy lymfocytů
Слайд 38
Poruchy bílé krevní řady
základních funkcí buněk bílé krevní
řady = specifická a nespecifická imunitní odpověd jedince
Tj.
likvidace korpuskulárních
částic a bakterií,
tvorba protilátek
zprostředkování tkáňové imunity
Proliferace a diferenciace buněk bílé krevní řady je podmíněna účinkem cytokinů (růstový faktor)
Слайд 39
A.Poruchy granulocytů
Účinkem růstových faktorů je pozitivně ovlivněna tvorba
granulocytů a buněk monocyto-makrofá- gového systému
Mezi granulopoezou a erytropoezou
existují významné rozdíly.
Množství granulocytů v krvi, na rozdíl od počtu erytrocytů, neukazuje míru produkce.
1. v kostní dřeni existuje velká zásobní hotovost již vytvořených granulocytů, která se může rychle uvolnit do cirkulace.
2. granulocyty již vyplavené z kostní dřeně se dělí na granulocyty v cirkulaci (intravazální hotovost) a granulocyty adherující k cévní stěně (marginální hotovost), při čemž marginální hotovost představuje přibližně 55 % všech buněk.
Слайд 40
A.Poruchy granulocytů
Účinkem růstových faktorů je pozitivně ovlivněna tvorba
granulocytů a buněk monocyto-makrofá- gového systému
Mezi granulopoezou a erytropoezou
existují významné rozdíly.
Doba života erytrocytů je podstatně delší než doba života granulocytů. Granulocyty žijí přibližně 24-36 hodin, zatímco doba života erytrocytů je podle použité techniky stanovena na 100-120 dnů.
Hlavní rozdíl mezi granulopoezou a erytropoezou spočívá v tom, že hlavním „pracovním místem“ erytrocytů je krev, pro granulocyty (stejně tak pro monocyty) představuje krev možnost transportu z místa vzniku do místa účinku, tj. do tkání.
Слайд 41
A.Poruchy granulocytů
Funkce granulocytů a monocytů (makrofágy)
Základní úlohou neutrofilních
granulocytů je likvidace cizorodého materiálu, což je umožněno jejich
schopností migrace k místu infekce, schopností fagocytózy a schopností ničit fagocytované bakterie.
Hlavním úkolem eozinofilních granulocytů je odstranění látek uvolňujících se při setkání jedince s antigenem, tj. histamínu, 5-hydroxytryptofanu a bradykininu a fagocytóza imunokomplexů.
Funkce bazofiiních granulocytů není úplně vyjasněna.
Monocyty představují cirkulující část mononukleámího fagocytámího systému. Vznikají v kostní dřeni a přestupují do krve a migrují do tkání, kde se mění v tkáňové makrofágy
Слайд 42
A.Poruchy granulocytů - Reaktivní změny bílých krvinek
Reaktivní změny
bílých krvinek
=změny počtu bílých krvinek
Při posuzování změn je hodnocen
absolutní počet bílých krvinek
mikroskopicky z diferenciálního obrazu odchylky jednotlivých typů od normy
např. granulocytóza = ↑ granulocytů, monocytóza = ↑ monocytů
např. granulocytopenie = ↓ granulocytů, monocytopenie = ↓ monocytů )
Слайд 43
A.Poruchy granulocytů - Reaktivní změny bílých krvinek
Neutrofílie
Nejčastější
leukocytóza =zvýšení počtu neutrofilů v periferní krvi
Hlavní příčiny neutrofílie
jsou:
z fyziologických příčin je patrna granulocytóza u novorozenců a malých dětí, v graviditě, při těžké fyzické práci a namáhavých sportovních výkonech;
infekční onemocnění zejména bakteriálního původu nebo přítomnost zánětu;
onemocnění provázená sterilním zánětem nebo nekrózou tkáně (infarkt myokardu, záněty svalů);
endogenní intoxikace (diabetické koma, urémíc- ké koma, dna, otrava olovem, podání některých léků a hormonů);
nádory;
akutní krevní ztráta a hemolýza;
stres.
Слайд 44
A.Poruchy granulocytů - Reaktivní změny bílých krvinek
Neutrofílie
Patogenní
podnět vyvolá zvýšenou potřebu granulocytů ve tkáních. Tam přestupují
buňky z marginální hotovosti a okamžitě jsou do krve vyplaveny již vytvořené granulocyty z kostní dřeně.
V krvi se objeví mladé buňky, které adherují k cévní stěně a postupně se doplní i intravazální hotovost.
V důsledku působení stresu přestupují marginální leukocyty do intravazální hotovosti, tak se zvýší množství cirkulujících granulocytů (granulocytóza po vyplavení adrenalinu, v časných fázích po ozáření apod.).
Účinek ACTH a glukokortikoidů na zvýšení počtu granulocytů je způsoben tím, že je zrychleno vyplavení granulocytů z kostní dřeně a zpomalen přesun buněk do marginální hotovosti.
Слайд 45
A.Poruchy granulocytů - Reaktivní změny bílých krvinek
Eozinofilie
provází zejm.
alergické reakce a parazitární infekce; nedostatečnou funkci kůry nadledvin,
hypo- a hyperfunkci štítné žlázy a neoplazmatické procesy.
Bazofilie
provází některá infekční a hematologická onemocnění (chronickou myeloidní leukémii, Hodgkinovu nemoc, pravou polycytémii a chronické hemolytické anémie).
Слайд 46
A.Poruchy granulocytů - Reaktivní změny bílých krvinek
Monocytóza
zvýšený počet
monocytů v krvi
důležitým diagnostickým znakem (endokarditida, tuberkulóza, infekční hepatitida,
Hodgkinova nemoc…).
Слайд 47
A.Poruchy granulocytů - Reaktivní změny bílých krvinek
Neutropenie
= Nedostatek
neutrofilů
Při snížené produkci nebo jejich zvýšeným odstraňováním z krve.
snížená
produkce
útlum kostní dřeně
zvýšené odstraňování z krve
zvýšený přesunem buněk do marginální hotovosti v počátečních stadiích infekčních onemocnění
zvýšenou aktivitou sleziny (hypersplenismus) při leukémiích, lymfomech a zvětšení sleziny (splenomegalie) různého původu
tvorbou autoprotilátek proti leukocytům.
Слайд 48
A.Poruchy granulocytů - Reaktivní změny bílých krvinek
Eozinopenie
= Nedostatek
eosinofilů
může být vyvoláno dřeňovým útlumem, zvýšenou produkcí ACTH a
glukokortikoidů, eventuelně po terapii glukokortikoidy.
Bazopenie
= Nedostatek basofilů
Vzhledem k malému množství bazofiiních granulocytů v krvi jsou úvahy o příčinách nepřesné.
Слайд 49
A.Poruchy granulocytů – Poruchy funkce granulocytů
Kvalitativní změny leukocytů
= poruchy migrace (chemotaxe) k místu infektu,
= poruchy
fagocytózy a schopnosti ničit fagocytované bakterie.
KO
kožní infekce
tvorba zánětových ložisek a abscesů v různých místech těla
Слайд 50
A.Poruchy granulocytů – Leukémie
leukémie = maligní bujení krvetvorných
buněk
Za normálních okolností ztrácejí leukocyty v průběhu své diferenciace
proliferační schopnost.
U leukémií tomu tak není. Maturace je na určitém vývojovém stupni zastavena a v kostní dřeni a v krvi se objevují nevyzrálé buňky (různé typy blastů u akutních forem) nebo se u chronických forem v organismu hromadí buňky víceméně vyzrálé.
Klasifikace leukémií vychází z morfologie buněk a přítomnosti specifických diferenciačních znaků.
Z klinického hlediska jsou leukémie děleny na akutní a chronické
Слайд 51
A.Poruchy granulocytů – Leukémie
Etiologie
Genetické faktory - vrozené genetické
defekty provázené chromozomálními aberacemi (např. Downův syndrom)
Výskyt leukémií u
dětí rodičů s leukémií je stejný jako v ostatní populaci
Většina defektů zvyšujících možnost vzniku leukémií je získaná.
Uplatňuje se vliv ionizačního záření
Působení chemických látek
Uvažuje se o působení virů
Слайд 52
A.Poruchy granulocytů – Leukémie
KO
akutní leukémie se projevuje
po nahromadění určitého počtu blastů (1 x 109 až
1 x 1012), kdy se projeví infiltrace kostní dřeně nádorovými buňkami a infiltrace orgánů a tkání vedoucí k poruchám funkce.
Слайд 53
A.Poruchy granulocytů – Leukémie
Myelodysplastický syndrom (MDS) = preleukemický
stav
vyvolán onemocněním kmenových buněk myeloidní řady, lymfoidní řada
není postižena
Syndrom je charakterizován vystupňovanou neefektivní krvetvorbou, neodpovídající na léčbu, pancytopenií a dysplazií kostní dřeně.
Kostní dřeň je většinou hypercehilární, méně často je počet buněk normální nebo snížen.
postihuje většinou pacienty starší 50 let
U všech pacientů se leukémie objevit nemusí, tito pacienti umírají většinou na sepsi v důsledku nedostatku granulocytů a monocytů, krvácivé stavy (↓trombocytů)
30-50% - akutní ne-lymfoblastická leukémie (špatná prognóza)
Слайд 54
A.Poruchy granulocytů – Leukémie
Chronická myeloidní leukémie (CML)
v chronické
fázi má relativně benigní průběh
Patologický buněčný klon se po
morfologické a funkční stránce téměř neliší od buněk normální granulocytární řady.
Vznik onemocnění je podmíněn fúzí dvou genů za vzniku onkogenu
Buňky patologického klonu exponenciálně zvyšují svůj počet.
V kostní dřeni i v krvi jsou nalézány všechny vývojové formy granulocytů
leukocytóza v krvi - extrémní hodnoty
V kostní dřeni je patrna hyperplazie granulocytární řady
Postupně se objevuje infiltrace kostní dřeně, jater a sleziny buňkami leukemického klonu → potlačení krvetvorby, hepatosplenomegalie → poruch fce jater, trombocytopenie, anemie
Слайд 55
A.Poruchy granulocytů – Leukémie
Chronická myeloidní leukémie (CML)
80-90% přechází
do akutní formy
KO
Úbytek na váze
↑ TT
Anémie
Krvácivost
Poruch jaterních funkcí
Слайд 56
A.Poruchy granulocytů – Leukémie
Akutní myeloblastová leukémie (AML)
charakterizována rychlým
hromaděním blastů v kostní dřeni a v krvi.
Blasty
nacházející se v krvi mají delší dobu života než granulocyty a jejich funkce neplní.
KO:
rychlý průběh
granulocytopénie, anémie, trombocytopeníe
infekce, horečka, krvácení a anémie
některých forem AML se rozvíjí diseminovaná intravaskulární koagulace
Слайд 57
B.Poruchy lymfocytů
Hlavní funkcí všech typů lymfocytů je uskutečnění
specifických imunitních reakcí
Lymfocyty jsou děleny na dvě základní a
funkčně odlišné kategorie
B-Iymfocyty T-lymfocyty
Слайд 58
B.Poruchy lymfocytů – poruchy produkce
1. Nejčastější změny vznikají
v souvislosti s přítomností cizích antigenů při místních nebo
celkových infekcích (reaktivní změny).
Stavy jsou většinou provázeny lymfadenopatií (zvětšením, případně bolestivostí mízních uzlin), zvýšeným množstvím plazmocytů v krvi a rovněž zvýšením množství lymfocytů v krvi.
2. Druhou příčinou změny produkce Iymfocytů je nádorová (neoplastická) alterace s následkem zvýšené vnímavosti vůči infekcím
V praxi je někdy odlišení reaktivních změn od neoplastické alterace obtížné
Слайд 59
B.Poruchy lymfocytů – poruchy produkce
Lymfocytóza
Zvýšené množství Iymfocytů v
krvi je příznakem některých bakteriálních a zejména virových infekcí.
Výrazným příznakem je u infekční mononukleózy.
Lymfocytóza je také výrazným a důležitým příznakem lymfoproliferativních onemocnění (viz dále).
Слайд 60
B.Poruchy lymfocytů – poruchy produkce
Lymfopenie
Snížené množství Iymfocytů v
krvi je způsobeno jejich sníženou produkcí a zvýšenými ztrátami.
Snížená
produkce
ionizační záření a cytostatická léčba
lymfocyty a lymfatická tkáň citlivě reagují na účinek hormonů kůry nadIedvin, takže lymfopenie vznikne při nadprodukci těchto hormonů a rovněž při léčbě ACTH nebo glukokortikoidy
K lymfopenii dochází rovněž při nádorové infiltraci mízních uzlin, při níž mízní uzliny ztrácejí schopnost uvolňovat lymfocyty do cirkulace.
Zvýšené ztráty
nejčastěji vyvolány rozšířením mízních cév (lymfangiektaziemi) v trávicím systému a také porušením celistvosti hrudního mízovodu (např. nádorem nebo tuberkulózním procesem.
Слайд 61
B.Poruchy lymfocytů – Lymfoproiiferativní onemocnění
Lymfoproliferativní onemocnění - tři
skupiny chorob:
Leukémie odvozené z lymfoidní řady - porucha vzniká
v buňkách kostní dřeně (primární lymfatická tkáň)
Lymfomy - vznikající převážně v mízních uzlinách (sekundární lymfatická tkáň).
Monoklonální gamapatie
Слайд 62
B.Poruchy lymfocytů – Lymfoproiiferativní onemocnění
Akutní lymfoblastová leukémie (ALL)
onemocnění převážně dětského věku.
přibližně ve 20 % případů
je prokázán filadelfský chromozom.
ALL vzniká v kostní dřeni
lymfoblasty nekontrolovatelně proliferují, většina blastů (podobně jako u AML) je však v klidové fázi buněčného cyklu.
Postupně je utlačována normální krvetvorba
U neléčené ALL pacienti umírají během několika měsíců v důsledku infekce, anemie, granulocytopénie a trombocytopenie.
Závažnými komplikacemi jsou neurologické poruchy vznikající v důsledku infiltrace mozkových plen a různých oblastí CNS.
Слайд 63
B.Poruchy lymfocytů – Lymfoproiiferativní onemocnění
Chronická lymfatická leukémie (CLL)
onemocnění převážně staršího věku
tvoří asi 30 % všech
leukémií
charakteristickým obrazem je hromadění morfologicky diferencovaných Iymfocytů v kostní dřeni, mízních uzlinách, histiocytomakrofágovém systému a v krvi.
Leukemické lymfocyty vykazují zásadní funkční poruchy, velice slabě reagují s cizorodými antigeny, na druhé straně jsou zdrojem autoprotilátek reagujících s antigeny vlastních tkání.
Onemocnění probíhá většinou pomalu, deset i dvacet let, někdy však choroba progreduje během několika málo let.
KO:
Lymfocytóza
Lymfatické uzliny jsou zvětšeny, stejně tak játra i slezina
Слайд 64
B.Poruchy lymfocytů – Lymfoproiiferativní onemocnění
Maligní lymfomy
skupina onemocnění
= nekontrolovatelná proliferace mízních uzlin
Proces se šíří mízními cévami
do kostní dřeně a dalších tkání.
Lymfomy jsou děleny :
Hodgkinova nemoc (maligní lymfogranulom). Tvoří asi 30 % všech lymfomů;
ne-hodgkinské lymfomy, které jsou klasifikovány podle morfologických a funkčních kritérií a podle membránových znaků.
Etiologie lymfomů
není zcela vyjasněna
Слайд 65
B.Poruchy lymfocytů – Lymfoproiiferativní onemocnění
Hodgkinova nemoc (maligní lymfogranulom)
onemocnění
postihující jedince mladšího věku (15-34 let) a dále kolem
50 let.
začíná v krčních lymfatických uzlinách, šíří se na další oblasti lymfatických uzlin a v pozdějších stadiích je infiltrována kostní dřeň a nelymfatické orgány (kosti, plíce, játra).
.
Слайд 66
B.Poruchy lymfocytů – Lymfoproiiferativní onemocnění
Hodgkinova nemoc (maligní lymfogranulom)
KO:
Horečka
komplikované
infekce v důsledku defektu specifické imunity
anémie a pancytopenie, lymfopenie
Přítomnost
buněk Reedových-Sternbergových - pravděpodobně transformované lymfocyty mající smíšené znaky T- i B-lymfocytů a vykazující i některé rysy makrofágů.
Слайд 67
B.Poruchy lymfocytů – Lymfoproiiferativní onemocnění
Non-hodgkinské lymfomy
Většina odvozena od
B-lymfocytů.
Část lymfomů je odvozena od T-buněk (lymfoblastický lymfom), z
T-lymfocytů vznikají rovněž kožní lymfomy, které se z kůže šíří do mízních uzlin a do dalších orgánů a tkání. Někdy vznikají primárně v lymfatické tkáni mimo mízní uzliny (např. ve sliznici trávicího ústrojí).
Слайд 69
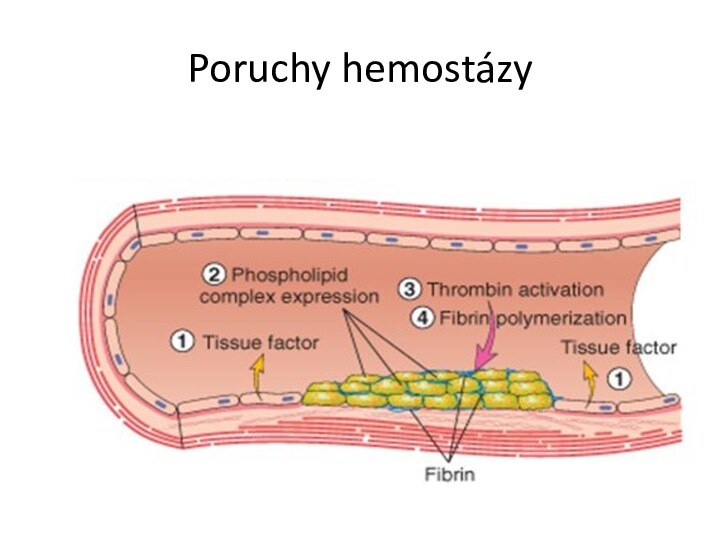
Poruchy hemostázy – hemostatická rovnováha
= vzájemný poměr a
rovnovážná aktivita mechanismů ovlivňujících zástavu krvácení.
Hemostatické mechanismy - pro
přežití jedince nezbytné.
Hemostatická rovnováha je udržována v mezích, které na jedné straně zabraňují vzniku spontánní intravaskulámí trombotizace, na druhé straně účinně staví krvácení (traumatické či spontánní) a omezují tak rozsah krevních ztrát.
Hemostatické mechanismy - koagulační systém vč. jeho inhibitorů a fibrinolytiekého systému, trombocyty a reakce cévní stěny.
Слайд 70
Poruchy hemostázy – krvácivé stavy
Zvýšení krvácivosti je způsobeno:
dysfunkcí
některého hemostatického mechanismu (koagulační kaskáda, počet a funkce trombocytů,
vlastnosti cévní stěny)
hyperstimulací antagonistických mechanismů (zvýšená aktivita inhibitorů koagulace, aktivace fibrinolytického systému).
Etiologie:
vrozené, geneticky podmíněné abnormity (hemofile A, B, C, dysfibrinogénémie);
získané choroby, většinou součásti širšího patologického obrazu (avitaminóza K);
iatrogenní (lékařem záměrně navozené) odchylky (léčba heparinem, antagonisty vitaminu K, fibrinolytiky).
Слайд 71
Poruchy hemostázy – krvácivé stavy
Koagulopatie
nedostatečnost jednoho nebo více
faktorů koagulační kaskády
KO:
při větších poraněních, kdy se tvoří rozsáhlé
hematomy s protrahovaným krvácením
spontánní krvácení do kloubů vede často už v mladém věku ke vzniku artropatií až ankylózy
Слайд 72
Poruchy hemostázy – krvácivé stavy
Koagulopatie
Hemofilíe A. Vrozený nedostatek
faktoru VIII.
Choroba je geneticky vázaná na X chromozom.
Znamená to, že postiženi jsou muži,
zatímco ženy - heterozygotky jsou přenašečkami
změněné alely bez klinických projevů.
Hemofílie B. Vrozený nedostatek faktoru IX.
Choroba je rovněž vázána na chromozom X,
je 10x vzácnější než hemofilíe A.
Hemofílie C. Vrozený deficit faktoru XI.
Je to vzácné onemocnění.
Слайд 73
Poruchy hemostázy – krvácivé stavy
Koagulopatie
Koagulopatie při hypovitaminóze K.
Vitamin K je endogenně syntetizován střevní flórou, nicméně alespoň
malý exogenní přívod potravou je nezbytný.
Je rozpustný v tucích, proto je jeho resorpce závislá na přítomnosti žluči.
Při malabsorpci (nedostatek žluči při obstrukčním ikteru) a při jaterních onemocněních.
Při narušení střevní mikroflóry - ATB
KO:
Zpomalené srážení krve
Krvácení z nosu
Слайд 74
Poruchy hemostázy – krvácivé stavy
Vaskulopatie - PURPURY
Při poruše
cévní stěny nejsou obvykle krvácení závažná. Nejčastějším projevem je
kožní purpura a drobné slizniční krvácení.
Hypovitaminóza C (kurděje, scorbut). Nedostatečnost cévní stěny vede ke krvácení z dásní, bolestivému krvácení do svalů zejména dolních končetin a ke vzniku drobných podkožních hematomů. Hypovitaminóza C je vzácná a setkáváme se s ní především u osaměle žijících starých lidí nebo u alkoholiků.
Слайд 75
Poruchy hemostázy – krvácivé stavy
Trombocytopenie a trombocytopatie
Projevem nedostatku
(trombocytopenie)
nebo funkční méněcennosti trombocytů (trombocytopatie)
KO:
mnohočetné petechie
krvácení ze sliznic
v
nejzávažnějších stavech krvácení do sítnice a do CNS
běžná drobná krvácení se spontánně nezastavují.
Слайд 76
Poruchy hemostázy – krvácivé stavy
Trombocytopenie a trombocytopatie
Trombocytopenie
krvácivé
projevům až při poklesu pod 30000 / mm3.
Příčina:
může být nedostatečná tvorba trombocytů v kostní dřeni při jejím toxickém, infekčním, radiačním nebo nádorovém postižení.
vzácnější jsou vrozené stavy.
Druhou možnou příčinou je zvýšený zánik cirkulujících trombocytů na podkladě autoimunitním, alergickém nebo konzumpčním (spotřebování trombocytů při DIC)
Слайд 77
Poruchy hemostázy – krvácivé stavy
Trombocytopenie a trombocytopatie
Trombocytopatie
většinou
geneticky podmíněná onemocnění postihující některou z funkcí trombocytů:
defekty
adheze (von Willebrandova choroba),
defekty agregace nebo
defekty prokoagulační funkce trombocytů.
Existují i získané trombocytopatie doprovázející urémii, krevní malignity nebo polékové trombocytopatie.
Za iatrogenní trombocytopatii lze považovat léčbu kyselinou acetylsalicylovou (ireverzibilní blokáda syntézy tromboxanu v membráně destiček! nebo dalšími antiagregačními léky v prevenci ischemické choroby srdeční a dalších cévních onemocnění.
Слайд 78
Poruchy hemostázy – Zvýšení krevní srážlivost
Zvýšení krevní srážlivost
hyperkoagulační
stavy (trombofilie) výsledkem narušené rovnováhy hemostatických a antihemostatických mechanismů.
Klinicky může hyperkoagulační stav vyústit v:
postižení makrocirkulace (tromboembolickou příhodu) nebo
generalizované postižení mikrocirkulace (diseminovanon intravaskulámí koagulaci).
Слайд 79
Poruchy hemostázy – DIC
Diseminovaná intravaskulární koagulace (DÍC)
Zvláštní klinickou
situací se uplatní:
zvýšená srážlivost
následně zvýšená krvácivost
=dvoufázový proces
Слайд 80
Poruchy hemostázy – DIC
Diseminovaná intravaskulární koagulace (DÍC)
první fáze
generalizovaná aktivace koagulační kaskády - nejčastějši masivním uvolněním faktoru
ÍH z poškozené tkáně (polytranma, operace, embolie plodové vody).
Dochází k diseminované koagulaci v kapilárním řečišti za vzniku mikrotrombů.
Narušení mikrocirkulace vede k ischemizaci tkání a k obrazu jatemího, renálního nebo nadledvinového selhávání.
Tyto síťovitě utvářené mikrotromby představují překážku prostupu erytrocytů.
Dochází k jejich poškození, fragmentaci a rozvoji hemolytické anémie. Cirkulující koagulační faktory jsou prakticky spotřebovány.
Слайд 81
Poruchy hemostázy – DIC
Diseminovaná intravaskulární koagulace (DÍC)
Druhá fáze
dochází k aktivaci fibrinolytického systému a mizí mikrotromby.
Protože
aktivovaná fibrinolýza není vyvažována koagulační kaskádou, došlo již ke spotřebě (konsumpci) koagulačmch faktorů a destiček a současně je narušena cévní stěna, nastává slizniční a orgánové krvácení, které může být fatální.