- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Злокачественные опухоли гортани и гортаноглотки
Содержание
- 2. ЭПИДЕМИОЛОГИЯ.Рак гортани занимает первое место среди злокачественных
- 4. 20%
- 5. 14,3%
- 6. 12,9%
- 7. 7,7%
- 8. Факультативные предраковые заболевания:-контактная фиброма;-рубцовый процесс после ожогов
- 9. Пахидермия, как правило, представлена наростами с неровными,
- 13. Анатомия гортаноглотки:-Глоточно-пищеводное соединение ( область позади перстневидного
- 14. Анатомические части гортани:1.Надсвязочная часть:-часть надгортанника выше подъязычной
- 15. ГОРТАНОГЛОТКА.
- 16. ГОРТАНЬ.
- 17. ГОРТАНЬ.
- 18. ГОРТАНЬ.
- 21. КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНОГЛОТКИ.Клиническая картина заболевания зависит
- 22. КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНИРазвитие раковой опухоли вестибулярного
- 23. КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНИЧастота поражения раковой опухолью
- 24. КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНИРак подскладочного отдела гортани
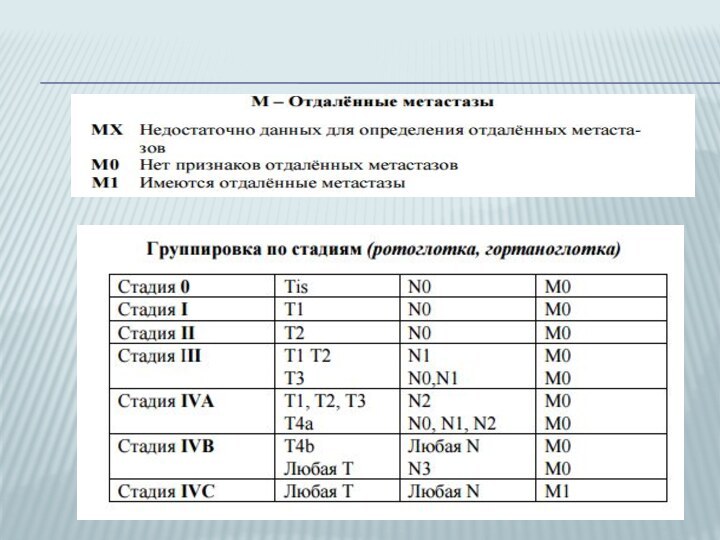
- 25. Отдалённые метастазы выявляют сравнительно редко (1,3–8,4%); локализуются в лёгких, позвоночнике и других органах.
- 26. ДИАГНОСТИЧЕСКИЕ МЕРОПРИЯТИЯ: 1. Осмотр начинается с тщательной
- 27. ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
- 28. СОВРЕМЕННЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯСуществуют три основных метода лечения
- 29. ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ При наличии у больного противопоказаний
- 30. Другой вариант лечения – это химиолучевая
- 31. ВАРИАНТЫ ЛЕЧЕНИЯ ТОЙ ИЛИ ИНОЙ ОБЛАСТИ Рак
- 32. Опухоли надсвязочного отделаПри раке надсвязочного отдела, соответствующем
- 33. Лечение метастазов рака гортани в лимфатических узлах
- 34. При недостаточной регрессии увеличенных лимфатических узлов и
- 35. ХИМИОТЕРАПИЯ1 PFцисплатин 100 мг/м2, в/в, 1 день;фторурацил
- 36. ЛУЧЕВАЯ ТЕРАПИЯ Лучевое лечение больных опухолями гортани
- 37. Ряду ослабленных больных, в том числе с
- 38. ПРОГНОЗПрогноз зависит от стадии опухолевого процесса, однако
- 39. ИНДИКАТОРЫ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯОценка эффективности лечения проводится на
- 40. ЭФФЕКТЫ ОТ ЛЕЧЕНИЯПолный эффект – исчезновение всех
- 41. Скачать презентацию
- 42. Похожие презентации
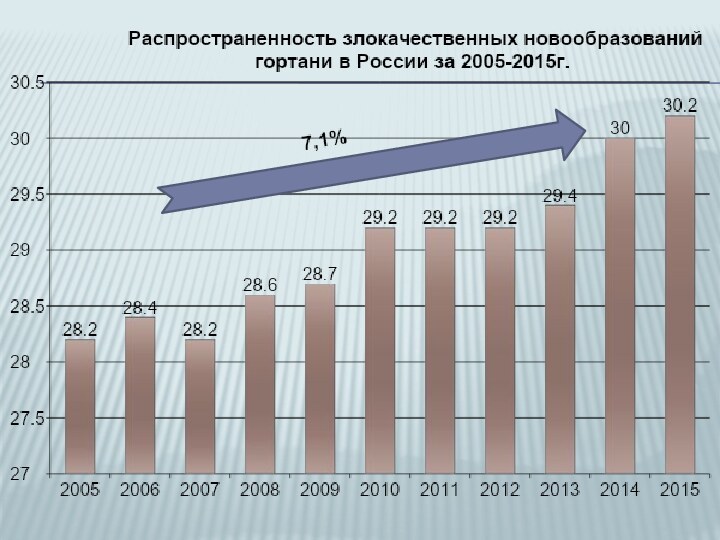
ЭПИДЕМИОЛОГИЯ.Рак гортани занимает первое место среди злокачественных опухолей головы и шеи (50-70%) , составляя 2,6% в общей структуре заболеваемости злокачественными новообразованиями человека. Заболевание чаще встречается у пациентов в возрасте от 40 до 60 лет. Соотношение


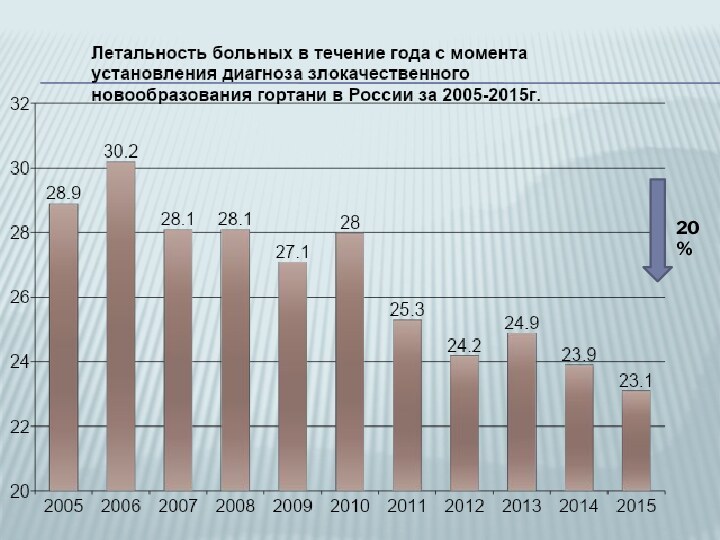
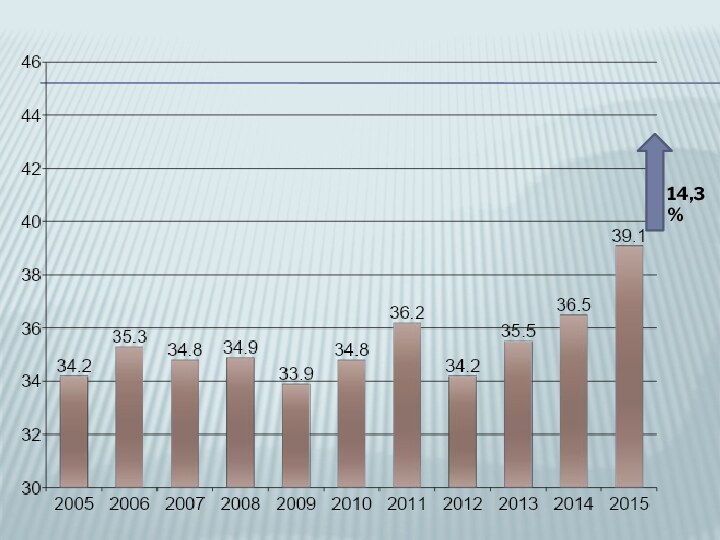
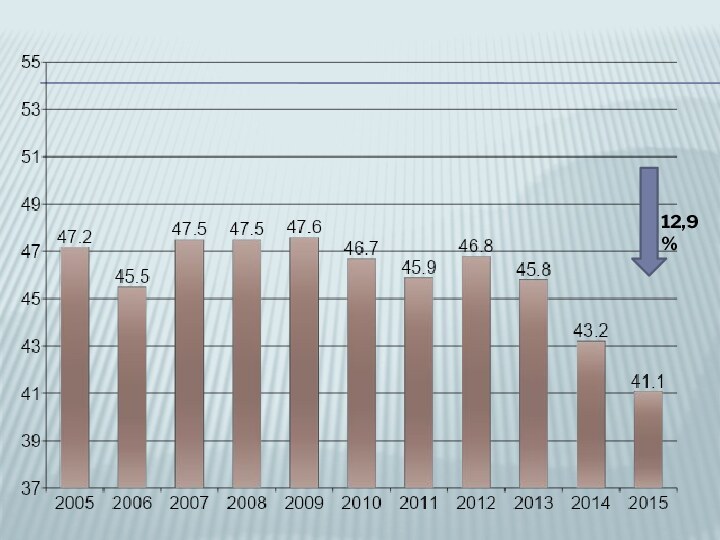
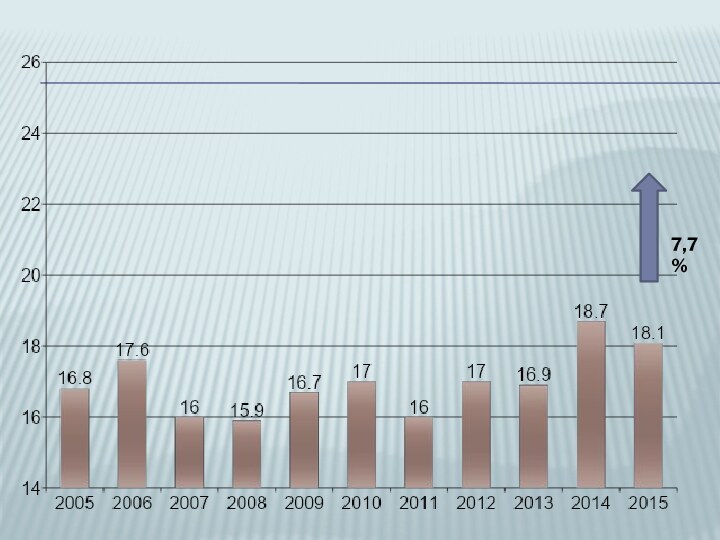


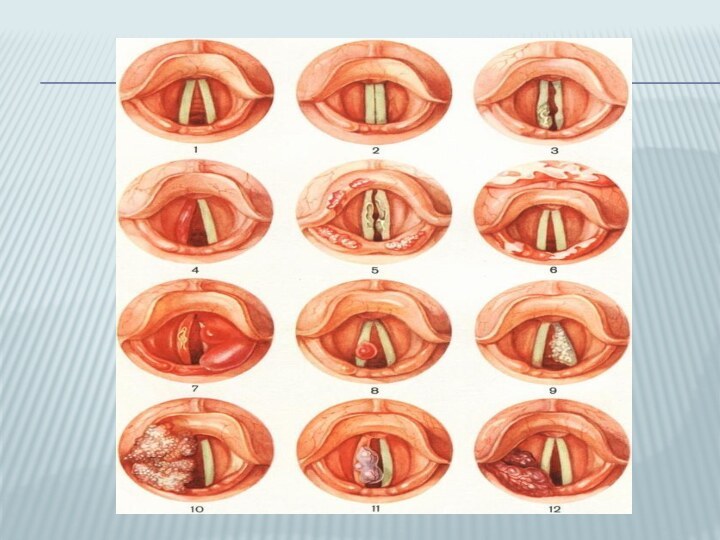
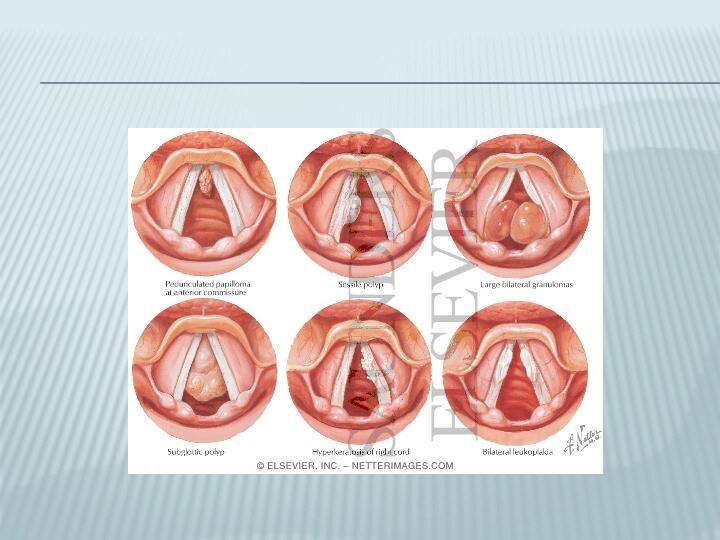
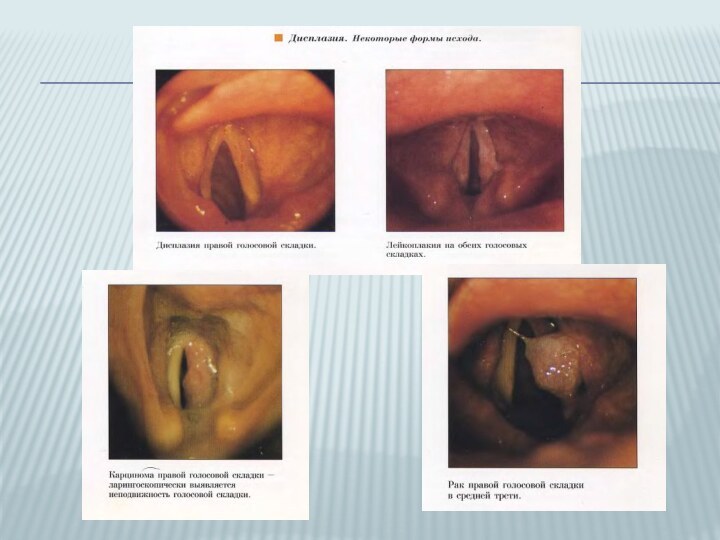


























Слайд 8
Факультативные предраковые заболевания:
-контактная фиброма;
-рубцовый процесс после ожогов и
хронических специфических инфекций, таких как туберкулез, сифилис, склерома.
Облигатные предраковые
заболевания:-гиперпластический ларингит
-папиллома
-лейкоплакия
-лейкокератоз
-пахидермия
Слайд 9 Пахидермия, как правило, представлена наростами с неровными, зазубренными
краями, серого цвета и четко отграничена от окружающей слизистой
оболочки.Лейкоплакия представляет собой ограниченное, продолговатое белое пятно, с неровной поверхностью, без сосудистого рисунка, не возвышающееся над слизистой оболочкой («толстое пятно белой краски»), плотно спаянное с подлежащей тканью.
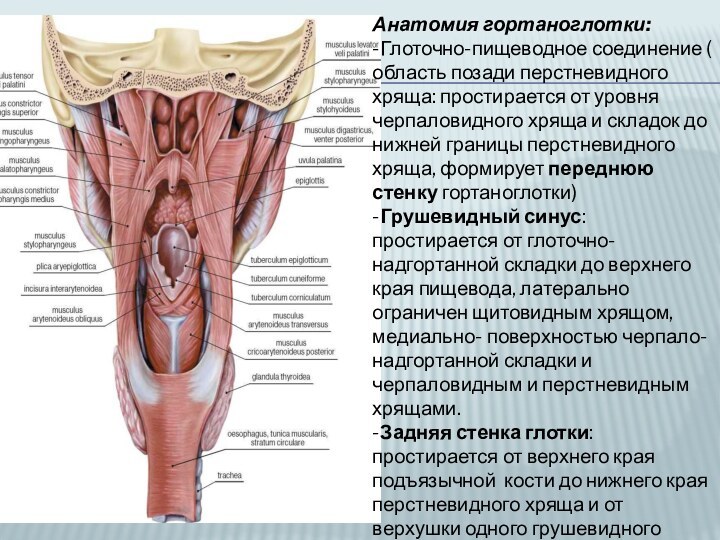
Слайд 13
Анатомия гортаноглотки:
-Глоточно-пищеводное соединение ( область позади перстневидного хряща:
простирается от уровня черпаловидного хряща и складок до нижней
границы перстневидного хряща, формирует переднюю стенку гортаноглотки)-Грушевидный синус: простирается от глоточно-надгортанной складки до верхнего края пищевода, латерально ограничен щитовидным хрящом, медиально- поверхностью черпало-надгортанной складки и черпаловидным и перстневидным хрящами.
-Задняя стенка глотки: простирается от верхнего края подъязычной кости до нижнего края перстневидного хряща и от верхушки одного грушевидного синуса до другого
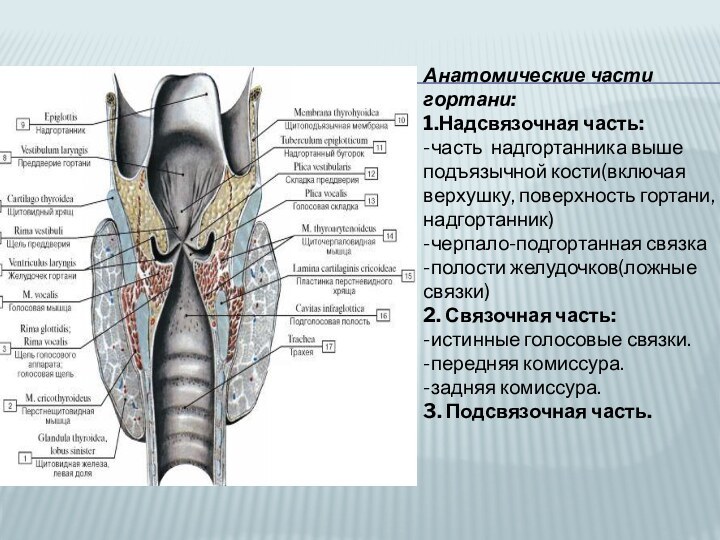
Слайд 14
Анатомические части гортани:
1.Надсвязочная часть:
-часть надгортанника выше подъязычной кости(включая
верхушку, поверхность гортани, надгортанник)
-черпало-подгортанная связка
-полости желудочков(ложные связки)
2. Связочная часть:
-истинные
голосовые связки.-передняя комиссура.
-задняя комиссура.
3. Подсвязочная часть.
Слайд 21
КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНОГЛОТКИ.
Клиническая картина заболевания зависит от
распространенности опухоли, формы роста и особенностей её локализации в
гортаноглотке. Чаще всего опухоли возникают в грушевидном синусе (71,6 %), затем – в заперстневидной области (16,1 %) и на задней стенке глотки (9,2 %).Общими симптомами для рака гортаноглотки различной локализации и распространенности являются локальная болезненность при глотании иногда с иррадиацией в ухо на стороне поражения, функциональные расстройства различной выраженности (попёрхивание пищей, задержка пищи, чувство «инородного тела» или «перекатывания слюны через валик»). По мере прогрессирования опухоли и нарастания явлений дисфагии возникает дефицит массы тела, усиливаются боли, которые становятся постоянными.
Слайд 22
КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНИ
Развитие раковой опухоли вестибулярного отдела
отмечают у 60– 65% больных. Рак этой локализации протекает
особенно агрессивно; раковая опухоль быстро распространяется на окружающие ткани и органы. Частота регионарного метастазирования наиболее высокая (35-45%).Рак надскладочного отдела в начале роста протекает бессимптомно. По мере роста новообразования появляются жалобы на неловкость, поперхивание при глотании, изменение тембра голоса. Прорастание опухоли в голосовую складку вызывает охриплость и только при большом распространении рака появляются боли при глотании, часто с иррадиацией в ухо.
Слайд 23
КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНИ
Частота поражения раковой опухолью складочного
отдела гортани составляет 30–35%. Опухоль поражает преимущественно передние или
средние отделы голосовых складок. Клиническое течение рака этого отдела наиболее благоприятное, метастазирует редко (0,4–5,0%).При раке голосовых складок даже незначительное образование, особенно в передней трети, приводит к нарушению голосообразования, быстрой утомляемости голоса, осиплости, охриплости и афонии. При экзофитном росте опухоли может возникнуть затруднение дыхания.
Слайд 24
КЛИНИЧЕСКАЯ КАРТИНА РАКА ГОРТАНИ
Рак подскладочного отдела гортани диагностируют
у 3–5% больных. Опухоли этой локализации имеют, как правило,
эндофитную форму роста. Частота регионарного метастазирования составляет 15–20%.При раннем раке подскладочного отдела больные жалоб не предъявляют. Иногда первым признаком заболевания является сухой, постепенно усиливающийся приступообразный кашель. При прорастании рака в голосовые складки появляются осиплость, охриплость и афония. При экзофитном росте опухоли возможно затруднение дыхания вплоть до стеноза.
Слайд 25 Отдалённые метастазы выявляют сравнительно редко (1,3–8,4%); локализуются в
лёгких, позвоночнике и других органах.
Слайд 26
ДИАГНОСТИЧЕСКИЕ МЕРОПРИЯТИЯ:
1. Осмотр начинается с тщательной пальпации боковой
поверхности шеи и подчелюстной области.
2. Орофарингоскопия, непрямая ларинго- и
гипофарингоскопия. В случае затруднения при осмотре (отек, наклон надгортанника и др.) необходима местная анестезия, смещение надгортанника.3. Фиброларингоскопия.
4. Биопсия опухоли (всем больным) для гистологического или цитологического исследования.
5. R–томограмма гортани.
6. КТ шеи с толщиной срезов не менее 0,8 см и/или МРТ первичного очага и шеи (по показаниям).
7. УЗИ шеи.
8. Иммуногистохимические исследования по показаниям.
9. Рентгенологическое исследование органов грудной клетки.
10.Лабораторные исследования: общий анализ крови, биохимический анализ крови, общий анализ мочи, определение группы крови и Rh-фактора, анализ крови на RW и ВИЧ
Слайд 28
СОВРЕМЕННЫЕ ПРИНЦИПЫ ЛЕЧЕНИЯ
Существуют три основных метода лечения рака
гортани – хирургический, лучевой и их сочетание. Все методы
могут быть дополнены химиотерапией. При опухолях, соответствующих Т1, эффективность хирургического метода лечения на первом этапе по результатам последних мировых исследований, выше, чем при лучевой терапии достигает 85-95% излеченности, так же снижается риск возникновения рецидива опухоли. При опухолях, соответствующих Т2, также лечение следует начинать с резекции гортани с последующим проведением послеоперационной лучевой терапии.
Слайд 29
ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ
При наличии у больного противопоказаний к
операции лечение начинается с лучевой терапии. При распространенном раке
гортани Т3–4 возможности лучевого лечения ограничены (5–40%), а хирургические вмешательства, если они возможны, носят калечащий характер. Индукционная химиотерапия по схеме TPF(таксотер+цисплатин+фторурацил) с последующей лучевой терапией может быть вариантом органосохранного лечения местно распространенного рака гортани или гортаноглотки у пациентов, ответивших на лечение, в противном случае выполняется ларнгэктомия.Слайд 30 Другой вариант лечения – это химиолучевая терапия.
По данным одного рандомизированного исследования одновременная химиолучевая терапия позволяет
добиться более высокой частоты сохранения гортани в течение первых двух лет после окончания лечения, не влияя при этом на выживаемость по сравнению с индукционной химиотерапией и последующей лучевой терапией (у пациентов, ответивших на лечение) или только лучевой терапии. Выбор органосохранного лечения на основе индукционной химиотерапии или одновременной химиолучевой терапии зависит от различных факторов (анатомическая локализация, предполагаемая комплементность пациента/переносимость лечения, соматический статус и др.) Кроме того, не каждому пациенту может быть проведено органосохранное лечение. Пациентам с массивной опухолью, распространяющейся на хрящи гортани, такое лечение не показано. Оба варианта лечения (на основе индукционной химиотерапии или одновременной химиолучевой терапии) не оказывают негативного влияния на безрецидивную и общую выживаемость, поскольку в случае неэффективности возможно проведение хирургического вмешательства по жизненным показаниям. Несмотря на это, у пациентов, подвергнутых комбинированным методам лечения, отмечено снижение частоты отдаленного метастазирования. При наличии у больного признаков перихондрита хрящей гортани, опухолевого стеноза лечение следует начинать с хирургического этапа.
Слайд 31
ВАРИАНТЫ ЛЕЧЕНИЯ ТОЙ ИЛИ ИНОЙ ОБЛАСТИ
Рак среднего отдела
гортани
Начинать лечение больных раком среднего отдела гортани Т1-2 следует
с хирургического удаления опухоли (различные виды резекции гортани в зависимости от локализации опухоли в том числе видеоэндоскопические) или лучевой терапии. При второй стадии местнораспространенного процесса проводится послеоперационный курс дистанционной гамм-терапии до 40 гр. При Т3 на первом этапе проводится хирургическое лечение или химиолучевая терапия. В случае недостаточной регрессии опухоли после 40 гр. больному необходимо предложить хирургическое вмешательство. В случае применения хирургического метода на первом этапе проводится послеоперационный курс лучевой терапии до СОД – 40-50 гр. При наличии положительных краев резекции должна проводится химиолучевая терапия. Рецидивы опухоли среднего отдела лечатся хирургически.
Слайд 32
Опухоли надсвязочного отдела
При раке надсвязочного отдела, соответствующем Т1–2,
лечение следует начинать с лучевого или хирургического лечения (эндоларингеальные
или супракрикоидные резекции). В случае уменьшения опухоли после 40 гр. более чем наполовину облучение продолжается до полной дозы. При недостаточной регрессии опухоли предлагается резекция или полное удаление гортани.Лечение рака гортани Т3–4 следует начинать с химиолучевой терапии или хирургического лечения. В случае уменьшения опухоли после 40 гр. более чем наполовину облучение продолжается до полной дозы. При недостаточной регрессии опухоли предлагается полное удаление гортани. При отказе от операции продолжается облучение до полной дозы.
Рак подскладочного отдела
При раке подскладочного отдела гортани или прорастании в подскладочное пространство опухолей других отделов больному необходимо хирургическое вмешательство с пред- или послеоперационным облучением.
Слайд 33
Лечение метастазов рака гортани в лимфатических узлах шеи
Наличие
регионарных метастазов у больных раком гортани не препятствует консервативному
лечению, т.к. метастазы этой локализации (N1–2) часто хорошоподдаются лучевому и химиолучевому лечению. Поэтому лимфатические узлы шеи с обеих сторон следует включать в зону облучения гортани. При необходимости облучения лимфатических узлов нижних отделов шеи больным показано использование прямого поля с блоком. Нижний край прямого поля
проходит на 1 см ниже нижнего края ключиц. При поражении надключичных лимфатических узлов должны облучаться лимфатические узлы верхнего средостения.
При наличии ограниченно смещаемых или не смещаемых метастазов лечение целесообразно начинать с неоадъювантной полихимиотерапии и последующего лучевого лечения в дозе 40 гр. Дальнейшая тактика зависит от эффективности проведенной терапии. В случае значительной или полной регрессии метастазов или их неоперабельности после указанной дозы облучение следует довести до СОД 60–70 гр.
Слайд 34 При недостаточной регрессии увеличенных лимфатических узлов и их
операбельности после 40 гр. необходимо производить фасциально-футлярное иссечение шейной
клетчатки (ФФиШК) или операцию Крайля по показаниям.Показаниями к выполнению фасциально-футлярной лимфодиссекции является наличие Н0, N1, N2а подвижных лимфоузлов без вовлечения в процесс внутренней яремной вены и кивательной мышцы.
Показаниями к проведению операции Крайля является наличие N1, N2а, б, с неподвижных, вколоченных лимфоузлов с вовлечением в опухолевый процесс
внутренней яремной вены и кивательной мышцы.
В случае спаянности регионарного метастаза на шее с сосудами шеи больному необходимо дополнительное обследование (КТ шеи и ангиография), т.к. возможно проведение операции Крайля с резекцией артерии и ее пластическим замещением.
При обнаружении у больного раком гортани единичных метастазов в легких и печени необходимо обследование для решения вопроса о возможности удаления этих образований.
Слайд 35
ХИМИОТЕРАПИЯ
1 PF
цисплатин 100 мг/м2, в/в, 1 день;
фторурацил 1000
мг/м2, в/в, с 1-го по 4-й дни.
Повторный курс через
3 недели.2. СрF
карбоплатин 300 мг/м2, 1 день;
фторурацил 1000 мг/м2, с 1-го по 4-й дни.
Повторный курс через 3 недели.
3. ТР
доцетаксел 75 мг/м2, 1 день;
цисплатин 75 мг/м2, 1 день.
Повторный курс через 3 недели.
4. TF
доцетаксел 75 мг/м2, 1 день;
фторурацил 750 мг/м2, с 1-го по 5-й дни.
Повторный курс через 3 недели.
5. МРF
метотрексат 20 мг/м2, 2 и 8 день;
фторурацил 375 мг/м2, 2 и 3 день;
цисплатин 100 мг/м2, 4 день.
Повторный курс через 3 недели.
6. СрР
карбоплатин 300 мг/м2, в/в, 1 день;
цисплатин 100 мг/м2, 3 день.
Повторный курс через 3 недели.
7. САР (а)
цисплатин 100 мг/м2, в/в, 1 день;
циклофосфан 400-500 мг/м2, в/в, 1 день;
доксорубицин 40-50 мг/м2, в/в, 1 день.
Повторный курс через 3 недели.
8. TPF
доцетаксел 75 мг/м2, 1 день;
цисплатин 100 мг/м2, 1 день;
фторурацил 1000 мг/м2, 1,2,3,4 день.
9. PBF
фторурацил 1000 мг/м2, 1,2,3,4 дни;
блеомицин 15 мг, 1-3 дни;
цисплатин 120 мг, 4 день.
Повторный курс через 3 недели.
Слайд 36
ЛУЧЕВАЯ ТЕРАПИЯ
Лучевое лечение больных опухолями гортани проводится, как
правило, с двух боковых противолежащих полей, обязательно включающих всю
гортань и зоны регионарного метастазирования. Размеры боковых полей определяются анатомическими размерами шеи, пределами распространенности первичной опухоли, наличием, величиной и локализацией метастазов и обычно равны 5–8х5–14 см. Границы указанных полей проходят: верхняя – по краю нижней челюсти до сосцевидного отростка, нижняя – на уровне ключицы, передняя – на 0,5 см дорсальнее передней поверхности шеи, задняя – по краю трапециевидной мышцы. В случае наличия метастазов в нижней трети шеи нижнюю границу поля необходимо опустить на 1 см ниже ключицы. Угол наклонацентральной оси пучка излучения к сагиттальной плоскости находится в пределах 90-100. Облучение осуществляется фотонным пучком на гамма-терапевтических аппаратах 60Со (1,25МэВ) или на линейном ускорителе (4–8МэВ), а также электронным пучком (6–12МэВ). Облучение проводится ежедневно с каждого поля. Разовая доза на очаг 2,0 гр. У больных с опухолями голосовой складки Т1 при отсутствии регионарных метастазов облучение осуществляется с небольшого поля (4–6 см) только на область гортани.
На первом этапе очаговая доза составляет 40 гр; в случае уменьшения объема опухоли на 50% и более облучение продолжается до СОД 70 гр. При регрессии опухоли менее 50% делается перерыв на две недели для реализации эффекта лечения и стихания лучевых реакций. После перерыва больной опять осматривается. В случае уменьшения новообразования более чем на 50% облучение продолжается до СОД 70–74 гр. Если же новообразование уменьшилось меньше чем наполовину, больному предлагается хирургическое вмешательство.
.
Слайд 37 Ряду ослабленных больных, в том числе с тяжелыми
сопутствующими заболеваниями, облучение проводится по расщепленному курсу: после дозы
38–40 гр. делается 7–14-дневный перерыв для стихания лучевых реакций и восстановления сил больного. После перерыва лучевая терапия продолжается до СОД 70–74 гр.В случае недостаточного эффекта лучевой терапии после 40 гр. и категорического отказа больного от хирургического вмешательства телегамматерапию следует продолжить до лечебной дозы. Укрупненное фракционирование при данной локализации опухолей рекомендуется только при предоперационном облучении у больных распространенными новообразованиями, подлежащими комбинированному лечению (прорастанием опухоли в мягкие ткани шеи, щитовидный хрящ или подскладочный отдел гортани).
При распространении опухолей гортани на переднюю комиссуру, боковую стенку глотки, преднадгортанниковое пространство лучевое лечение в качестве единственного метода недостаточно эффективно и его целесообразно дополнять локальной СВЧ-гипертермией, химиотерапией и/или выполнять хирургическое вмешательство.
Наличие у больного трахеостомы не препятствует проведению лучевого лечения. При распространенных новообразованиях трахеостома включается в поле облучения.
Слайд 38
ПРОГНОЗ
Прогноз зависит от стадии опухолевого процесса, однако в
целом его нельзя назвать благоприятным. В значительной степени это
обусловлено большой долей пациентов с распространенными формами заболевания. Так, согласно данным литературы и клинических наблюдений, распространенные, запущенные формы рака гортаноглотки составляют более 85 % среди всех впервые выявленных случаев заболевания. При использовании современных схем комплексного лечения в целом удается достичь 5-летней выживаемости у 56 % больных. Прогноз ухудшается при возникновении метастазов: 3-летняя выживаемость в группах больных раком гортаноглотки Т3–4N0–1М0 составляет до 80 %, а при Т3–4N2–3М0 – не превышает 40 %. При достижении полной регрессии новообразования в результате химиолучевого лечения показано регулярное наблюдение и обследование пациентов с це- лью своевременного выполнения хирургического вмешательства в случае возникновения рецидива
Слайд 39
ИНДИКАТОРЫ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ
Оценка эффективности лечения проводится на основании
следующих методов исследования:
1. Фиброларингоскопия.
2. R–томограмма гортани.
3. КТ шеи с
толщиной срезов не менее 0,8см и/или МРТ первичного очага и шеи (по показаниям).4. УЗИ шеи.
Слайд 40
ЭФФЕКТЫ ОТ ЛЕЧЕНИЯ
Полный эффект – исчезновение всех очагов
поражения на срок не менее 4х недель.
Частичный эффект –
большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов. Стабилизация - (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование - увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения.