- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему ДВС - синдром
Содержание
- 2. Синдром диссеминированного внутрисосудистого свертывания крови (двс)
- 3. Этот синдром обусловлен формированием множественных микросгустков, агрегатов
- 4. Этиология Этиологические факторы, запускающие каскад свёртывающей
- 5. ДВС в акушерстве проявляется в основном :При
- 6. Основные механизмы патогенеза ДВС-синдрома:- Повреждение тканей. Поступление
- 7. - Поражение тромбоцитов и макрофагов. Непосредственная стимуляция
- 8. Действия тромбина и их результат: •
- 9. Действия плазмина и их результат: •
- 10. Образование тромбина на ранних стадиях ДВС способствует
- 11. Классификация ДВС - синдромаМолниеносныеОстрые ПодострыеХроническиеРецидивирующиеГенерализованныеЛокальныеПо патогенезу:ДВС с
- 12. КЛИНИЧЕСКАЯ КАРТИНАОсновные клинические проявления ДВС-синдрома — тромбозы,
- 13. Стадии (фазы) ДВС-синдрома: • I стадия
- 14. Стадия гиперкоагуляцииВ стадию гиперкоагуляции происходит активация сосудисто-тромбоцитарного
- 15. Стадия коагулопатии потребленияСтадия коагулопатии потребления — «немая»
- 16. Стадия гипокоагуляцииСтадия гипокоагуляции характеризуется потерей одной из
- 17. Стадия исходаПолное несвертывание крови,Развитие полиорганной недостаточности,Шок и формирование шоковых органов,Выздоровление.
- 18. Главные клинические проявления ДВС-синдрома: • тромботические
- 19. ДИАГНОСТИКАДиагностика ДВС-синдрома возможна на основании клинических (тромбогеморрагический
- 20. ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯСтадия гиперкоагуляции: • время свёртывания
- 21. Стадия коагулопатии потребления: • тромбоциты↓; • фибриноген
- 22. Стадия гипокоагуляции: • время кровотечения↑, время
- 23. ЛечениеЛечение ДВС-синдрома заключается в проведении одновременно трёх
- 24. При гестозах беременным с хронической формой ДВС-синдрома
- 25. При острых формах ДВС, наряду с мероприятиями
- 26. Торможение фибринолитической активности достигают введением её ингибиторов
- 27. Интенсивную терапию продолжают и после устранения ДВС-синдрома.
- 28. Скачать презентацию
- 29. Похожие презентации
Синдром диссеминированного внутрисосудистого свертывания крови (двс) – неспецифический общепатологический процесс, обусловленный поступлением в кровоток активаторов свертывания крови, агрегацией тромбоцитов, увеличением тромбина, активацией и последующим истощением плазменных ферментных систем (калий-кинин-креиновой, фибринолитической, свертывающей системы комплемента, и























Слайд 3 Этот синдром обусловлен формированием множественных микросгустков, агрегатов клеток,
агрегатов МЦР, что приводит к гипоксии, ацидозу, дистрофии, развитию
геморрагических осложнений и глубокой дисфункции жизненноважных органов.
Слайд 4
Этиология
Этиологические факторы, запускающие каскад свёртывающей системы:
•повреждения клеток крови, в результате чего высвобождается
фосфолипиды, активирующие внутрисосудистое свертывание•повреждения тканей и в результате поступление в кровоток тканевого тромбопластина
•поражение эндотелия сосудистой стенки,когда происходит активация ХII фактора.
•гемодинамические нарушения, сопровождающие шок, макро- и микроциркуляторные нарушения в тканях с развитием гипоксии
•исходная гиперкоагуляция.
Эти состояния приводят к гипоксии тканей и метаболическому ацидозу, что, в свою очередь, вызывает активацию кровяного и тканевого тромбопластина.
Слайд 5
ДВС в акушерстве проявляется в основном :
При тяжелых
формах гестоза,
Преждевременной отслойке нормально расположенной или предлежащей плаценте,
Эмболии
околоплодными водами,Мертвом плоде,
Септическом и
геморрагическом шоке
Разрыве матки и д.р.
Слайд 6
Основные механизмы патогенеза ДВС-синдрома:
- Повреждение тканей. Поступление прокоагулянтов
(тканевой фактор) в системный кровоток запускают каскад реакций системы
свёртывания крови, прежде всего благодаря активации VII фактора. Происходит образование активного тромбопластина (самая продолжительная фаза гемостаза) при участии плазменных (XII, XI, IX, VIII, X, IV, V) и тромбоцитарных факторов.- Повреждение эндотелия. Приводит к обнажению коллагена и субэндотелиальной зоны, активации факторов свёртывания контактной фазы и тромбоцитов. Это ведёт к избыточному переходу протромбина в тромбин при действии активного тромбопластина и участии ионов кальция (фактор IV).
Слайд 7 - Поражение тромбоцитов и макрофагов. Непосредственная стимуляция тромбоцитов
приводит к образованию внутрисосудистых тромбоцитарных микроагрегатов и фибрин-полимера. Тромбин
при участии ионов кальция (фактор IV) и фактора тромбоцитов переводит фибриноген в фибрин-мономер. В свою очередь, фибрин-мономер при действии VIII фактора плазмы и тромбоцитарного фактора II превращается в нерастворимые нити фибрина-полимера.Активация системы свёртывания крови любого происхождения приводит к чрезмерному образованию тромбина и плазмина, действие которых обусловливает проявления ДВС-синдрома.
Слайд 8
Действия тромбина и их результат:
• образование
фибрина — снижение активности факторов I, II; • агрегация тромбоцитов
— снижение количества тромбоцитов; • активация факторов V, VIII — снижение концентрации факторов V, VIII; • активация фактора ХIII — снижение концентрации фактора XIII; • активация системы протеина С/протеина S — снижение их концентрации; • активация фибринолитической системы
Слайд 9
Действия плазмина и их результат:
• деградация
фибрина — значительное повышении продуктов деградации фибрина; • деградация фибриногена
— снижение концентрации фактора I; • протеолиз фактов V и VIII — снижение их содержания; • протеолиз фактора Виллебрандта, XIII, XI — снижение их содержания; • протеолиз фактора XIII — снижение его концентрации; • изменения в гликопротеидах тромбоцитарной мембраны.Слайд 10 Образование тромбина на ранних стадиях ДВС способствует появлению
больших растворимых комплексов фибрин- фибриноген и образованию фибриновых микротромбов,
вызывающих обструкцию микроциркуляторного русла и ПОН.
Слайд 11
Классификация ДВС - синдрома
Молниеносные
Острые
Подострые
Хронические
Рецидивирующие
Генерализованные
Локальные
По патогенезу:
ДВС с преобладанием
прокоагулянтного звена гемостаза
ДВС с преобладанием сосудисто-тромбоцитарного звена гемостаза
ДВС с
одинаковой активностью прокоагулянтного и сосудисто-тромбоцитарного звеньев.
Слайд 12
КЛИНИЧЕСКАЯ КАРТИНА
Основные клинические проявления ДВС-синдрома — тромбозы, приводящие
к нарушению микроциркуляции и возникновению ПОН и геморрагического синдрома.
ДВС-синдром характеризуется стадийностью развития.
Слайд 13
Стадии (фазы) ДВС-синдрома:
• I стадия —
гиперкоагуляция, • II стадия — коагулопатия потребления, • III
стадия — гипокоагуляция,• IV стадия — стадия исхода.
Слайд 14
Стадия гиперкоагуляции
В стадию гиперкоагуляции происходит активация сосудисто-тромбоцитарного звена
гемостаза, усиление коагуляционного потенциала крови и гиперагрегация тромбоцитов. Кроме
того, повышается концентрация тромбина, содержание фибриногена, вязкость крови и Ht.Клинически стадия гиперкоагуляции характеризуется ухудшением самочувствия. Пациенты предъявляют жалобы неспецифического характера на повышенную утомляемость, тревожное настроение, снижение диуреза и сердцебиение. При объективном осмотре выявляют повышение АД.
Слайд 15
Стадия коагулопатии потребления
Стадия коагулопатии потребления — «немая» и
коварная. Внешнее благополучие не соответствует тяжести развивающейся патологии. Периодически
на фоне нормального или даже несколько пониженного АД возникает АГ, тахикардия или брадикардия.В эту стадию происходит потребление факторов свёртывания крови (фибриногена, тромбина, VII, V, IX, X факторов, тромбоцитов) на образование множества тромбов, которые лизируются благодаря интенсивной продукции плазминогена и антитромбина III. Усиливается ферментативный и неферментативный фибринолиз, одновременно происходит распад и деградация многих белков (усиленный протеолиз), снижается образование антитромбина III.
Слайд 16
Стадия гипокоагуляции
Стадия гипокоагуляции характеризуется потерей одной из главных
жизненных функций — способности крови свёртываться. Это происходит вследствие
отсутствия главного фактора коагуляционного звена — фибриногена (фактор I), при этом фибринолиз может достигать 100%.Клиническая картина стадии гипокоагуляции характеризуется массивными кровотечениями. Как из-за острой кровопотери, так и вследствие токсического влияния продуктов протеолиза и фибринолиза быстро развивается тяжёлое состояние пациентки. В паренхиматозных органах (печени, почках, поджелудочной железе) одновременно отмечаются и тромбозы, и кровоизлияния.
Слайд 17
Стадия исхода
Полное несвертывание крови,
Развитие полиорганной недостаточности,
Шок и формирование
шоковых органов,
Выздоровление.
Слайд 18
Главные клинические проявления ДВС-синдрома:
• тромботические явления;
•
геморрагический синдром; • микроциркуляторные нарушения; • ПОН; • анемия; • нестабильная гемодинамика; • шок
и формирование шоковых органов.
Слайд 19
ДИАГНОСТИКА
Диагностика ДВС-синдрома возможна на основании клинических (тромбогеморрагический синдром,
микроциркуляторные нарушения) и лабораторных (тромбоцитопения, фрагментация эритроцитов, снижение концентрации
АТ III иплазминогена) данных.
Слайд 20
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
Стадия гиперкоагуляции:
• время свёртывания
крови ↓; • АЧТВ ↓; • Ht ↑ (40 и
≥); • фибриноген ↑; • время рекальцификации плазмы ↑ (более 45”); • тромбиновое время ↑ (более 10”); • АЧТВ ↓ (менее 45”); • ±продукты деградации фибрина (более 10 мг%); • ±растворимые комплексы мономеров фибрина; • ± тесты: этаноловый, протаминсульфатный.
Слайд 21
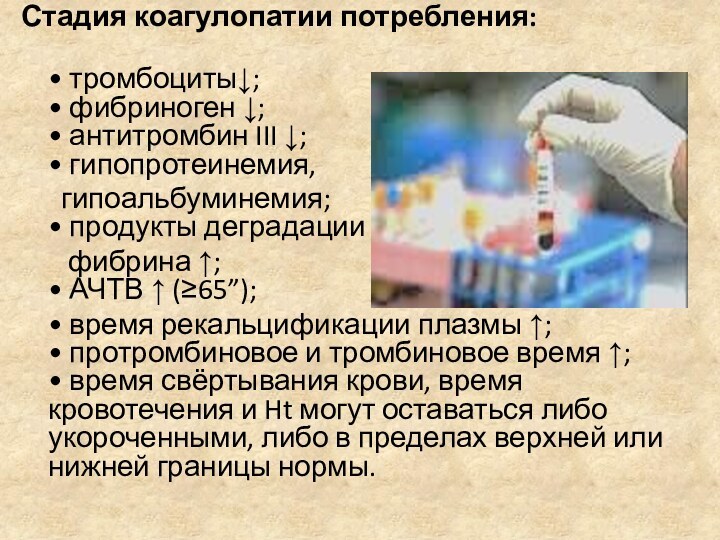
Стадия коагулопатии потребления:
• тромбоциты↓;
• фибриноген ↓;
• антитромбин III
↓;
• гипопротеинемия,
гипоальбуминемия;
• продукты деградации
фибрина ↑;
• АЧТВ ↑ (≥65”);• время рекальцификации плазмы ↑; • протромбиновое и тромбиновое время ↑; • время свёртывания крови, время кровотечения и Ht могут оставаться либо укороченными, либо в пределах верхней или нижней границы нормы.
Слайд 22 Стадия гипокоагуляции: • время кровотечения↑, время свертывания крови
↑; • ↑фибринолитической активности и протеолиза; • фибриноген ↓; • Hb ↓,
Ht ↓; • эритроциты ↓; • плазменные факторыIV, VIII, I, II, V, XIII ↓; • активность антитромбина III ↓; • плазминоген ↓; • повышенная кровоточивость, отсутствие сгустков или быстрое их растворение.
Слайд 23
Лечение
Лечение ДВС-синдрома заключается в проведении одновременно трёх основных
мероприятий:
• ликвидации основной причины, вызвавшей ДВС;
• нормализации
гемодинамики;
• нормализации свёртывания крови.Для лечения ДВС-синдрома при акушерских кровотечениях следует учитывать фазу синдрома, в которую начато лечение, а также характер акушерской патологии. Лечение
проводят под контролем лабораторной
диагностики.
Слайд 24 При гестозах беременным с хронической формой ДВС-синдрома показано
применение низкомолекулярных кровезаменителей (декстран, гемодез в сочетании со спазмолитиками,
которые улучшают реологические свойства крови, препятствуют микротромбозу и способствуют усилению тканевой перфузии.Гепарин натрия — антикоагулянт прямого действия, при введении подкожно по 5000–10 000 ЕД каждые 12 ч он нормализует уровень тромбоцитов и фибриногена. Гепарин уменьшает активность тромбоцитов, обладает антитромбопластиновой и антитромбиновой активностью,
тем самым нормализует
кровообращение в
паренхиматозных органах и
маточно-плацентарном комплексе.
Слайд 25 При острых формах ДВС, наряду с мероприятиями по
нормализации центральной и периферической гемодинамики, проводят мероприятия по восстановлению
коагуляционных свойств крови. Для этого необходимо остановить внутрисосудистое свёртывание и снизить фибринолитическую активность крови. Лекарственную терапию осуществляют под контролем коагулограммы. Для восстановления коагуляционных свойств крови проводят замещающую терапию: переливание свежезамороженной плазмы, свежезамороженных эритроцитов, «тёплой донорской крови», свежецитратной крови, антигемофильной плазмы.Слайд 26 Торможение фибринолитической активности достигают введением её ингибиторов животного
происхождения, например апротинина. Разовая доза контрикала — 2000 ЕД
(суточная — 6000 ЕД), трасилола — 2500 ЕД (суточная — 10 000 ЕД), гордокса — 100 000 ЕД (суточная — 500 000 ЕД). Ингибиторыфибринолиза применяют
строго под контролем
коагулограммы.
Слайд 27 Интенсивную терапию продолжают и после устранения ДВС-синдрома. Пациенту
проводят лечение почечной, печёночной и лёгочной недостаточности, восстановление белкового
и электролитного баланса, профилактику инфекционных осложнений.Решается вопрос
о родоразрешении.