- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
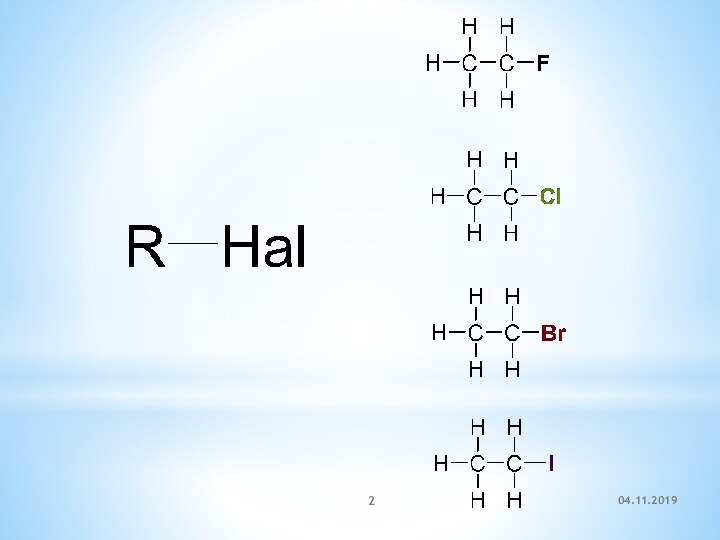
Презентация на тему ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
Содержание
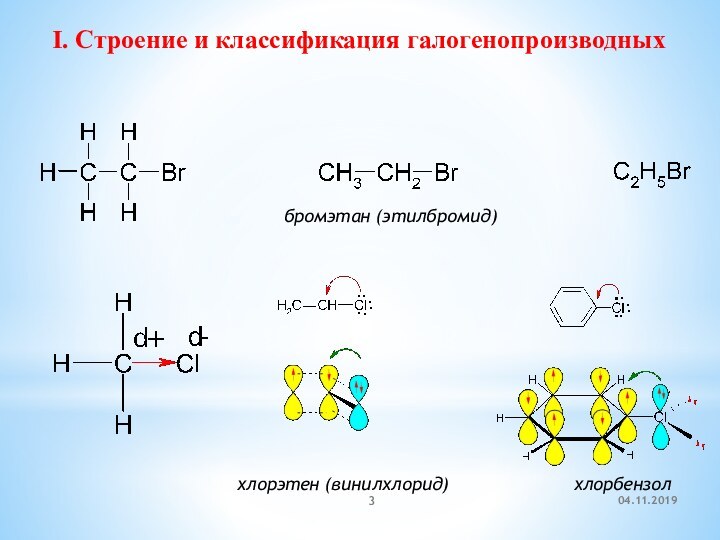
- 3. I. Строение и классификация галогенопроизводныхбромэтан (этилбромид)хлорэтен (винилхлорид)
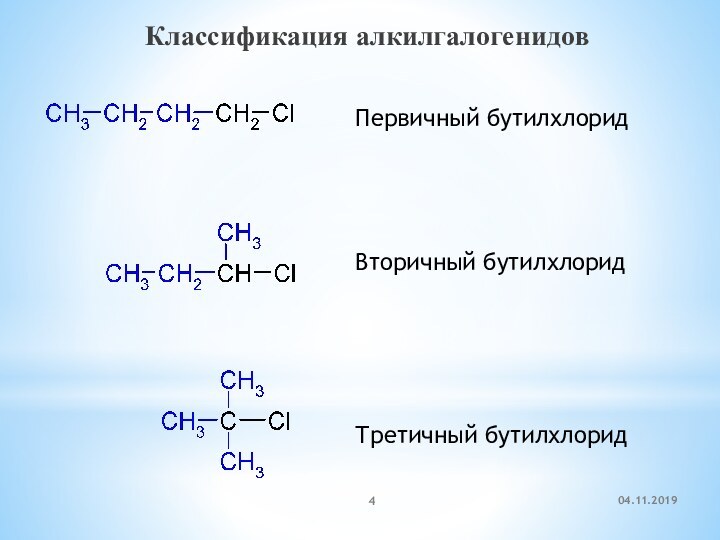
- 4. Классификация алкилгалогенидовПервичный бутилхлоридВторичный бутилхлоридТретичный бутилхлорид
- 5. II. Номенклатура 3-метил-1-хлоробутан
- 6. хлороформ
- 7. III. Изомерия1. Cтруктурная изомерия
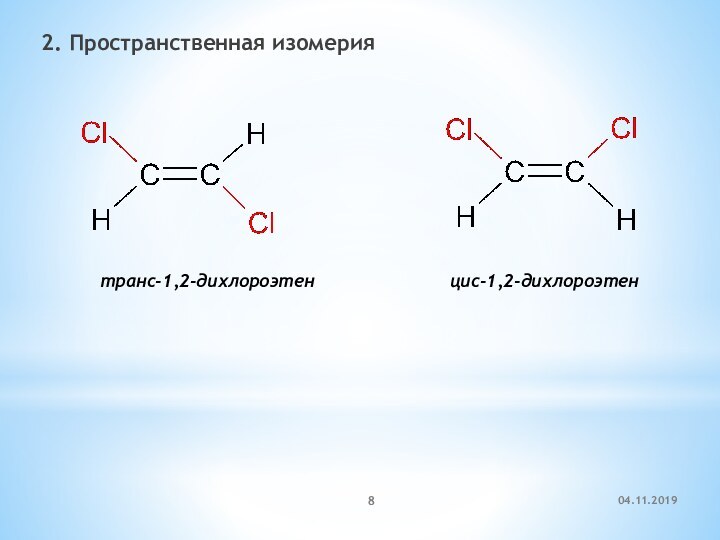
- 8. 2. Пространственная изомерия транс-1,2-дихлороэтен
- 9. IV. Физические и биологические свойстваРис. 1. Зависимость
- 10. t кип. oC
- 11. фторотан (используется для наркоза) 1,1,1-трифтор-2-бром-2-хлорэтан
- 12. V. Способы получения галогенопроизводных углеводородов 1. Галогенирование алканов 2.
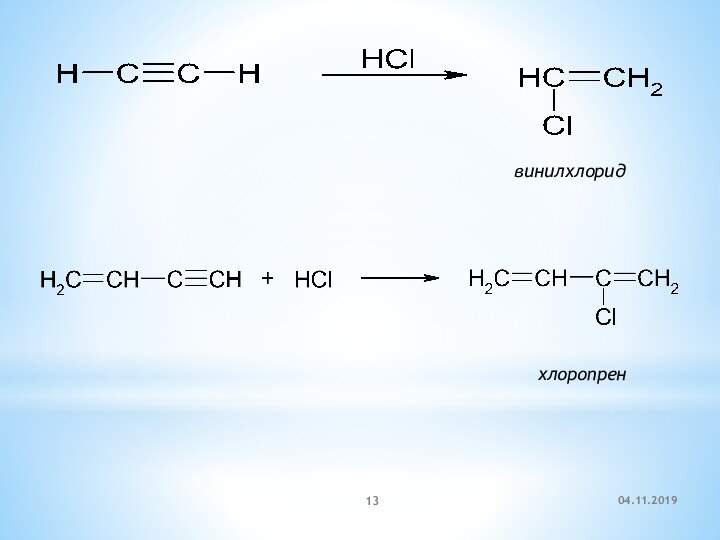
- 13. винилхлорид хлоропрен
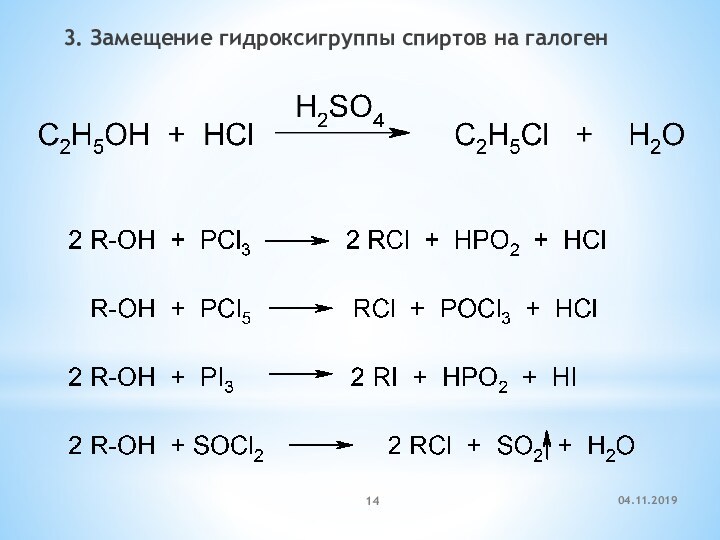
- 14. 3. Замещение гидроксигруппы спиртов на галоген
- 15. 4. Реакция Бородина-ХунсдиккераАлександр Бородин (31.10.1833 – 15.02.1887)русский учёный-химик (химик-органик) и композитор
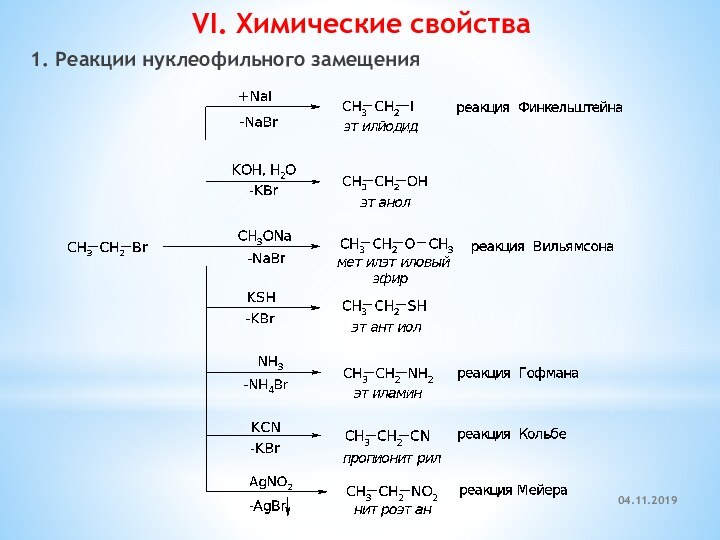
- 16. VI. Химические свойства1. Реакции нуклеофильного замещения
- 17. Органические галогенидыАлкилгалогенидыАрилгалогенидыТипичные реакции c участием галогена:SNEМеханизмы:SN1, SN2E1,
- 18. Типовые реакции алифатического нуклеофильного замещения с участием алкилгалогенидов
- 19. Механизм реакций нуклеофильного замещенияВ случае вторичных и
- 20. В случае третичных алкилгалогенидов нуклеофильное замещение идёт
- 22. 2. Реакции элиминирования (отщепления)
- 23. Реакции дегидрогалогенирования идут в соответствии с правилом
- 24. Дата рождения: 2 июля 1841Место рождения: г.
- 25. Механизмы реакций элиминирования Механизм E1субстрат
- 26. Механизм Е1(мономолекулярное элиминирование)Лимитирующая стадия – образование карбокатионаВозможны перегруппировки карбокатионаСкорость реакции = k × [RX]
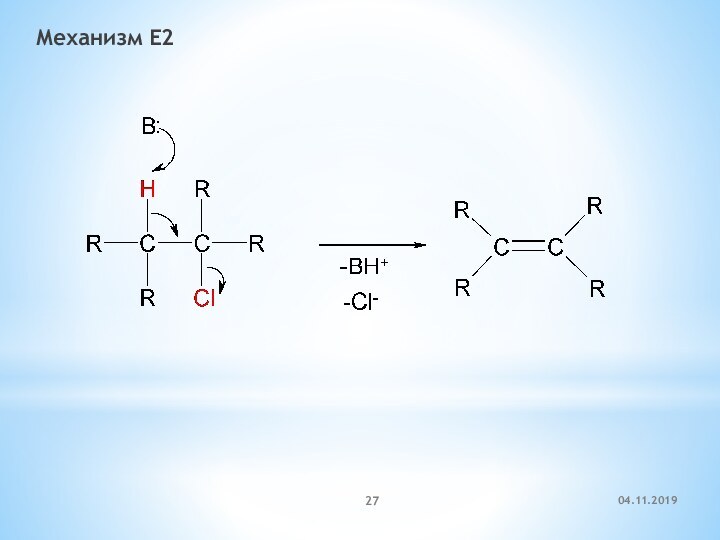
- 27. Механизм E2
- 28. Механизм Е2(бимолекулярное элиминирование)Скорость реакции = k × [RX] × [В]
- 30. 3. Взаимодействие с металлами 1). При взаимодействии алкилгалогенидов
- 31. этилбромид
- 32. Гриньяр (Grignard) Франсуа Огюст Виктор (06.05.1871, Шербур,
- 34. Метод предложен русским учёным-химиком Фёдором Фёдоровичем Бейльштейном
- 35. CuO + 2RHal +
- 36. Нижник Я.П. http://norgchem.professorjournal.ru
- 37. Скачать презентацию
- 38. Похожие презентации







![ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ Механизм Е1(мономолекулярное элиминирование)Лимитирующая стадия – образование карбокатионаВозможны перегруппировки карбокатионаСкорость реакции = k × [RX]](/img/tmb/14/1395535/340d3312d4b0235db0deaa29ae8e5411-720x.jpg)
![ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ Механизм Е2(бимолекулярное элиминирование)Скорость реакции = k × [RX] × [В]](/img/tmb/14/1395535/8e7f9ce0d086f768e5138aebbb8f5f60-720x.jpg)






Слайд 4
Классификация алкилгалогенидов
Первичный бутилхлорид
Вторичный бутилхлорид
Третичный бутилхлорид
Слайд 5
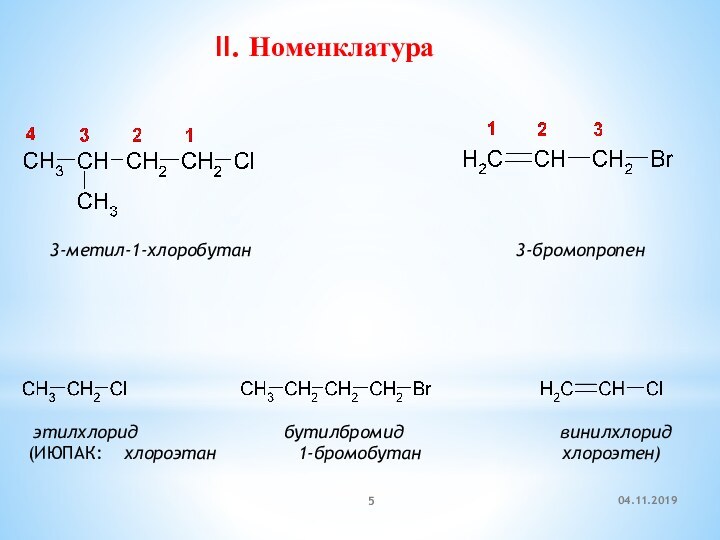
II. Номенклатура
3-метил-1-хлоробутан
3-бромопропен
этилхлорид бутилбромид винилхлорид
(ИЮПАК: хлороэтан 1-бромобутан хлороэтен)
Слайд 7
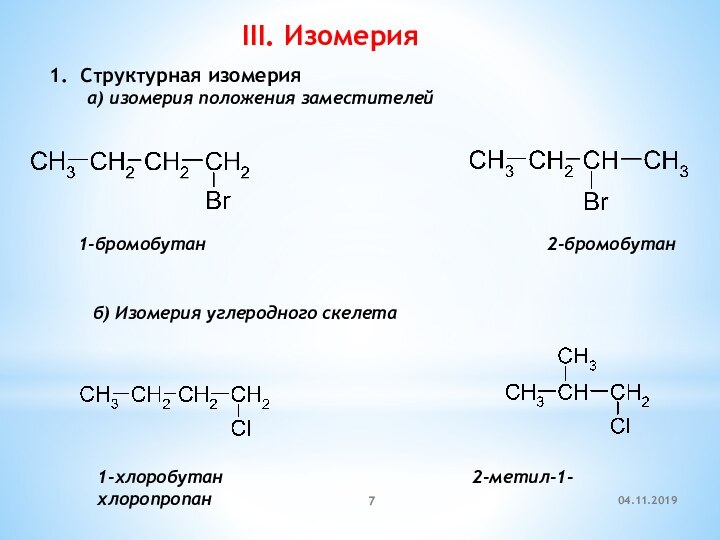
III. Изомерия
1. Cтруктурная изомерия
а)
изомерия положения заместителей
1-бромобутан
2-бромобутан б) Изомерия углеродного скелета
1-хлоробутан 2-метил-1-хлоропропан
Слайд 9
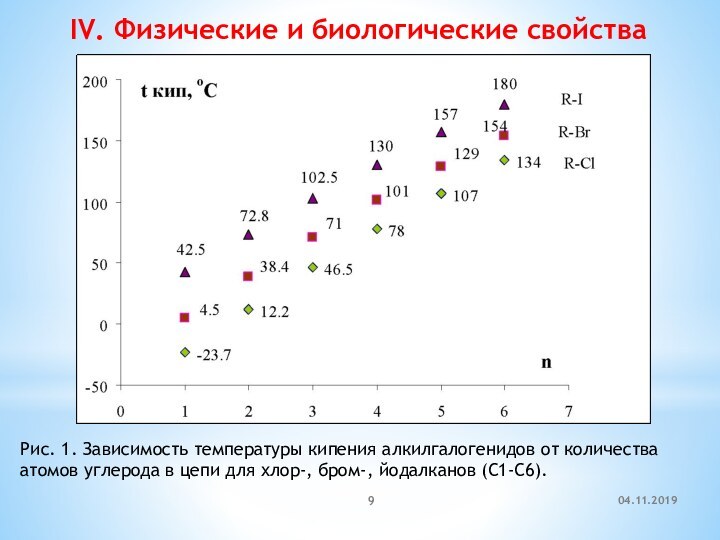
IV. Физические и биологические свойства
Рис. 1. Зависимость температуры
кипения алкилгалогенидов от количества атомов углерода в цепи для
хлор-, бром-, йодалканов (С1-С6).Слайд 10 t кип. oC -23,7
40 61,2 76,8
Галогенопроизводные являются гидрофобными веществами: они плохо растворяются в воде и хорошо растворяются в неполярных гидрофобных растворителях.
Многие галогенопроизводные используются как хорошие растворители: хлороформ, хлористый метилен, четырёххлористый углерод используются для растворения масел, жиров и эфирных масел.
Слайд 11
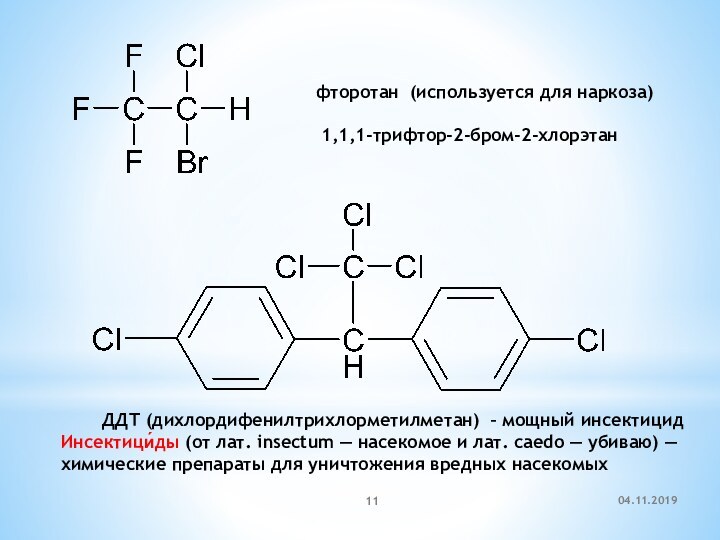
фторотан (используется для наркоза)
1,1,1-трифтор-2-бром-2-хлорэтан
ДДТ (дихлордифенилтрихлорметилметан) – мощный инсектицид
Инсектици́ды (от лат. insectum
— насекомое и лат. caedo — убиваю) — химические препараты для уничтожения вредных насекомых
Слайд 12
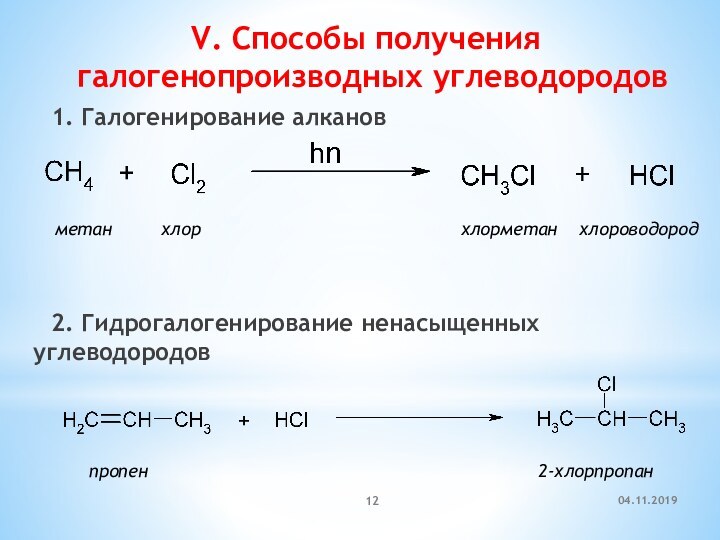
V. Способы получения галогенопроизводных углеводородов
1. Галогенирование алканов
2. Гидрогалогенирование
ненасыщенных углеводородов
метан хлор
хлорметан хлороводород пропен 2-хлорпропан
Слайд 15
4. Реакция Бородина-Хунсдиккера
Александр Бородин (31.10.1833 – 15.02.1887)
русский учёный-химик
(химик-органик) и композитор
Слайд 17
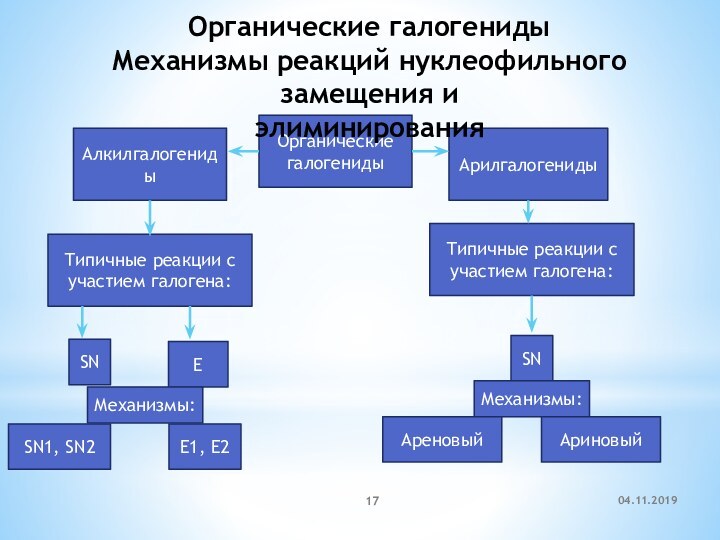
Органические галогениды
Алкилгалогениды
Арилгалогениды
Типичные реакции c участием галогена:
SN
E
Механизмы:
SN1, SN2
E1, E2
Типичные
реакции c участием галогена:
SN
Механизмы:
Ареновый
Ариновый
Органические галогениды
Механизмы реакций нуклеофильного замещения и
элиминирования
Слайд 19
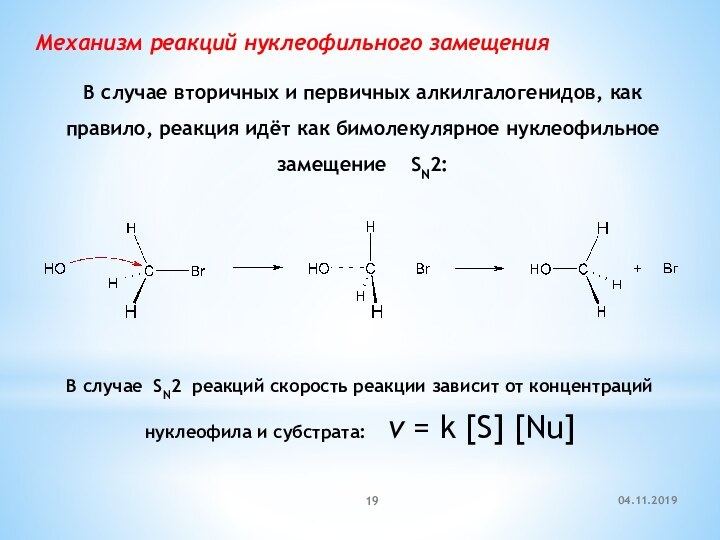
Механизм реакций нуклеофильного замещения
В случае вторичных и первичных
алкилгалогенидов, как правило, реакция идёт как бимолекулярное нуклеофильное замещение
SN2:В случае SN2 реакций скорость реакции зависит от концентраций нуклеофила и субстрата: v = k [S] [Nu]
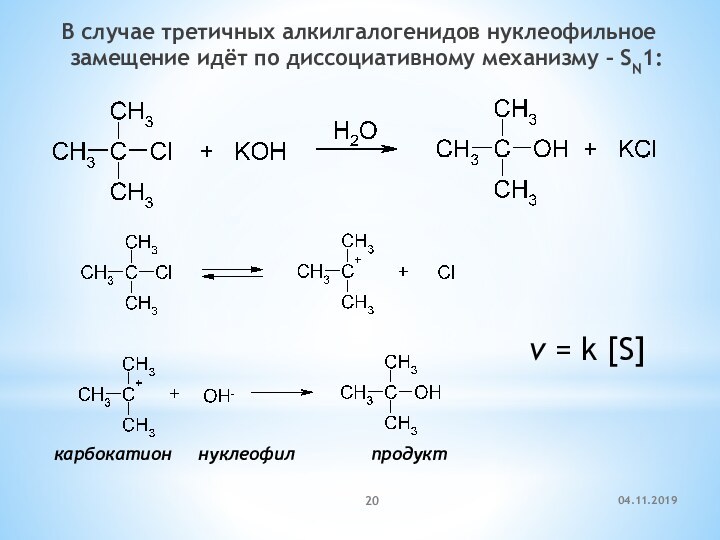
Слайд 20 В случае третичных алкилгалогенидов нуклеофильное замещение идёт по
диссоциативному механизму – SN1:
карбокатион
нуклеофил продукт v = k [S]
Слайд 22
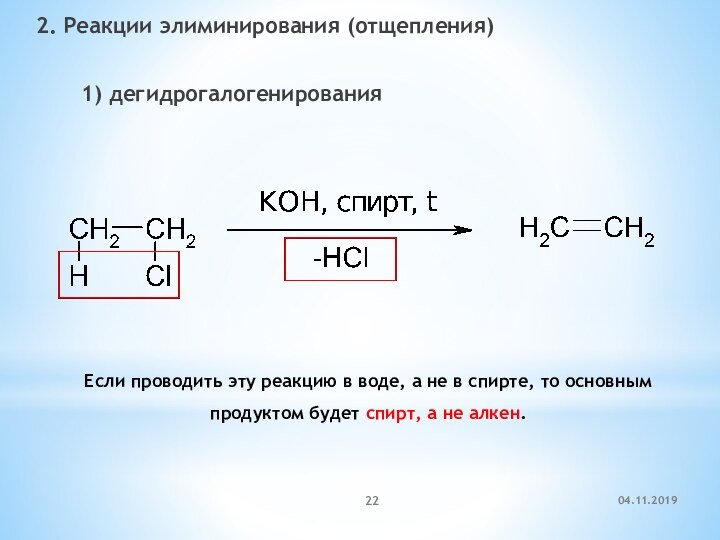
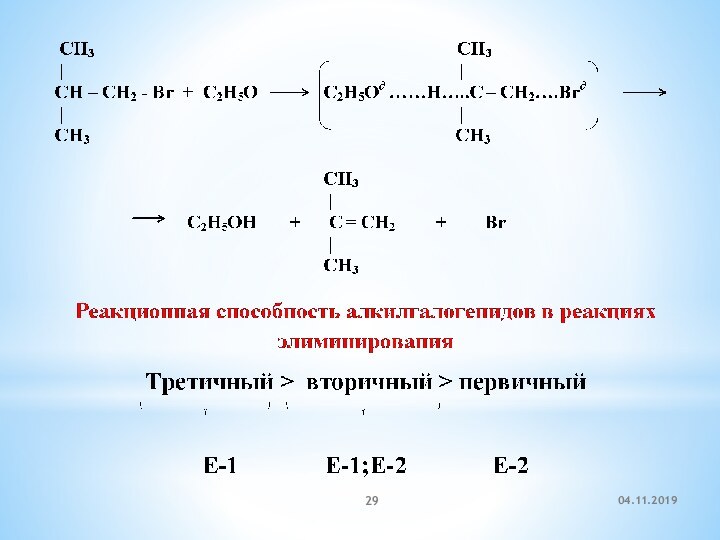
2. Реакции элиминирования (отщепления)
1)
дегидрогалогенирования
Если проводить эту реакцию в воде, а не в
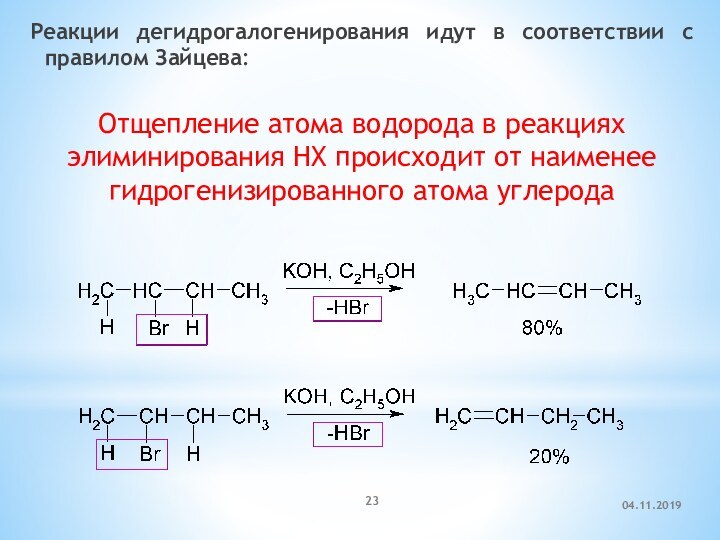
спирте, то основным продуктом будет спирт, а не алкен.Слайд 23 Реакции дегидрогалогенирования идут в соответствии с правилом Зайцева:
Отщепление атома водорода в реакциях элиминирования HX происходит от
наименее гидрогенизированного атома углерода
Слайд 24
Дата рождения: 2 июля 1841
Место рождения: г. Казань
Дата
смерти: 1 сентября 1910 (69 лет)
Место смерти: г. Казань
Страна: Российская империя
Научная
сфера: химияМесто работы: Казанский университет
Научный руководитель: А. М. Бутлеров
Зайцев воспитал большую школу химиков (Е. Е. Вагнер, А. Е. Арбузов, С. Н. Реформатский, А. Н. Реформатский, И. И. Канонников и др.).
Александр Михайлович Зайцев
Слайд 26
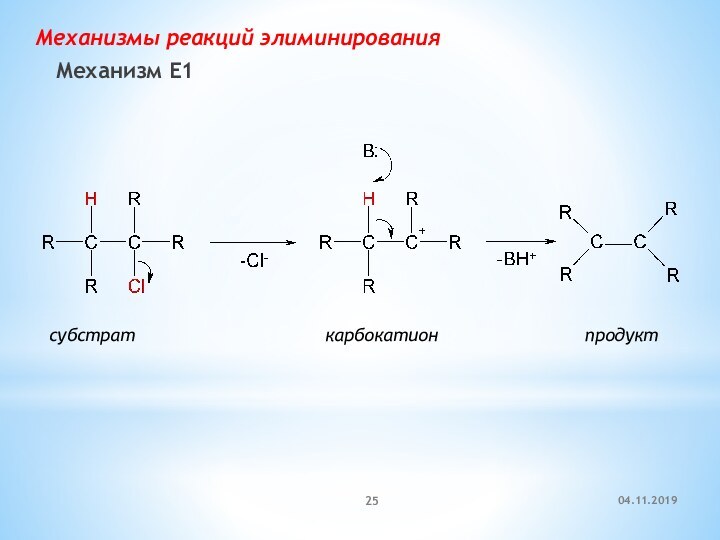
Механизм Е1
(мономолекулярное элиминирование)
Лимитирующая стадия –
образование карбокатиона
Возможны перегруппировки
карбокатиона
Скорость реакции = k × [RX]
Слайд 30
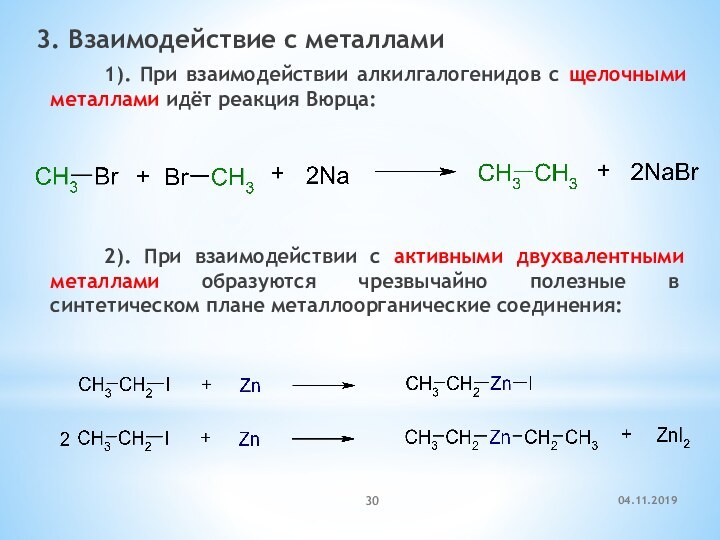
3. Взаимодействие с металлами
1). При взаимодействии алкилгалогенидов с
щелочными металлами идёт реакция Вюрца:
2). При взаимодействии с активными
двухвалентными металлами образуются чрезвычайно полезные в синтетическом плане металлоорганические соединения:Слайд 31 этилбромид
этилмагнийбромид
Mg-органические соединения – реактивы Гриньяра (Гриньяр, Нобелевская премия, 1912)
Слайд 32 Гриньяр (Grignard) Франсуа Огюст Виктор (06.05.1871, Шербур, —
13.12.1935, Лион), французский химик-органик, член Парижской АН (1926). Преподаватель,
а затем профессор университета в Нанси (с 1909). В 1900 совместно со своим учителем Ф. Барбье получил раствор эфиратов смешанных магний-галогенорганических соединений и применил эти соединения для синтеза многих классов органических соединений. Вскоре новый метод широко вошёл в химическую практику (см. Гриньяра реакция). Много внимания Г. уделил разработке номенклатуры органических соединений. Нобелевская премия (1912, совместно с П. Сабатье).
Слайд 34
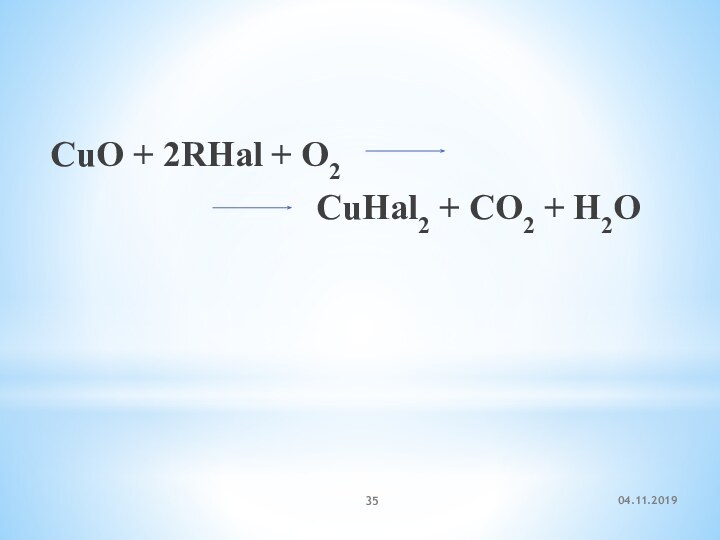
Метод предложен русским учёным-химиком Фёдором Фёдоровичем Бейльштейном в
1872 г
Качественная реакция на галогенопроизводные называется пробой Бейльштейна:
При нагревании
галогенопроизводного с медью, атомы галогена отщепляются с образованием летучих хлоридов меди, окрашивающий пламя в красивый зелёный или сине-зелёный цвет.Фёдор Фёдорович (Фридрих Конрад) Бейльштейн