Слайд 2
ГЕМОПОЭЗ
Кроветворением или гемопоэзом, называют развитие крови.
Различают эмбриональный
гемопоэз, который происходит в эмбриональный период и приводит к
развитию крови как ткани.
Постэмбриональный гемопоэз, который представляет собой процесс физиологической регенерации крови.
Слайд 3
ГЕМОПОЭЗ
Развитие эритроцитов называют эритропоэзом.
Развитие гранулоцитов — гранулоцитопоэзом.
Тромбоцитов —
тромбоцитопоэзом
Моноцитов — моноцитопоэзом.
Развитие лимфоцитов и иммуноцитов — лимфоцито-
и иммуноцитопоэзом.
Слайд 4
Эмбриональный гемопоэз
В развитии крови как ткани в эмбриональный
период можно выделить 3 основных этапа, последовательно сменяющих друг
друга – мезобластический, гепатолиенальный и медуллярный.
Первый, мезобластический этап – это появление клеток крови во внезародышевых органах, а именно в мезенхиме стенки желточного мешка, мезенхиме хориона и стебля. При этом появляется первая генерация стволовых клеток крови (СКК). Мезобластический этап протекает с 3-й по 9-ю неделю развития зародыша человека.
Слайд 5
Эмбриональный гемопоэз
Второй, гепатолиенальный этап начинается с 5—6-й недели
развития плода, когда печень становится основным органом гемопоэза, в
ней образуется вторая генерация стволовых клеток крови.
Кроветворение в печени достигает максимума через 5 мес. и завершается перед рождением.
СКК печени заселяют тимус, селезенку и лимфатические узлы.
Слайд 6
Эмбриональный гемопоэз
Третий, медуллярный (костномозговой) этап — это появление
третьей генерации стволовых клеток крови в красном костном мозге,
где гемопоэз начинается с 10-й недели и постепенно нарастает к рождению.
После рождения костный мозг становится центральным органом гемопоэза.
Слайд 7
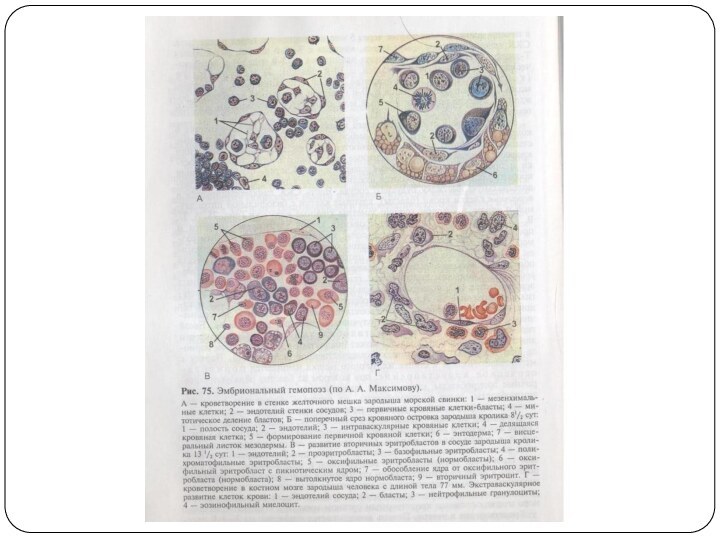
Кроветворение в стенке желточного мешка
В мезенхиме стенки желточного
мешка обособляются зачатки сосудистой крови, или кровяные островки.
В
них мезенхимные клетки округляются, теряют отростки и преобразуются в стволовые клетки крови.
Клетки, ограничивающие кровяные островки, уплощаются, соединяются между собой и образуют эндотелиальную выстилку будущего сосуда.
Часть стволовых клеток дифференцируется в первичные клетки крови (бласты).
Слайд 8
Кроветворение в стенке желточного мешка
Большинство первичных кровяных клеток
митотически делится и превращается в первичные эритробласты, характеризующиеся крупным
размером – мегалобласты.
Это превращение совершается в связи с накоплением эмбрионального гемоглобина (HbF) в цитоплазме бластов.
В некоторых первичных эритробластах ядро подвергается кариорексису и удаляется из клеток, в других ядро сохраняется.
В результате образуются безъядерные и ядросодержащие первичные эритроциты, отличающиеся большим размером по сравнению с нормоцитами и поэтому получившие название мегалоцитов.
Слайд 9
Кроветворение в стенке желточного мешка
Такой тип кроветворения называется
мегалобластическим.
Он характерен для эмбрионального периода, но может появляться
в постнатальном периоде при некоторых заболеваниях.
Слайд 10
Кроветворение в стенке желточного мешка
Наряду с мегалобластическим в
стенке желточного мешка начинается нормобластическое кроветворение, при котором из
бластов образуются вторичные эритробласты, из которых образуются вторичные эритроциты (нормоциты).
Слайд 11
Кроветворение в стенке желточного мешка
Развитие эритроцитов в стенке
желточного мешка происходит внутри первичных кровеносных сосудов, т.е. интраваскулярно.
Одновременно экстраваскулярно из бластов, расположенных вокруг сосудистых стенок, дифференцируется небольшое количество гранулоцитов — нейтрофилов и эозинофилов.
Слайд 12
Кроветворение в стенке желточного мешка
Часть СКК остается в
недифференцированном состоянии и разносится током крови по различным органам
зародыша, где происходит их дальнейшая дифференцировка в клетки крови или соединительной ткани.
После редукции желточного мешка основным кроветворным органом временно становится печень.
Слайд 13
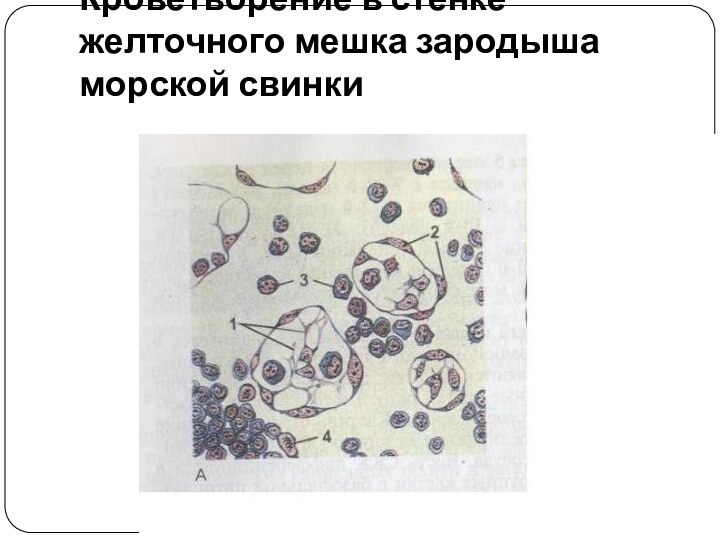
Кроветворение в стенке желточного мешка зародыша морской свинки
Слайд 14
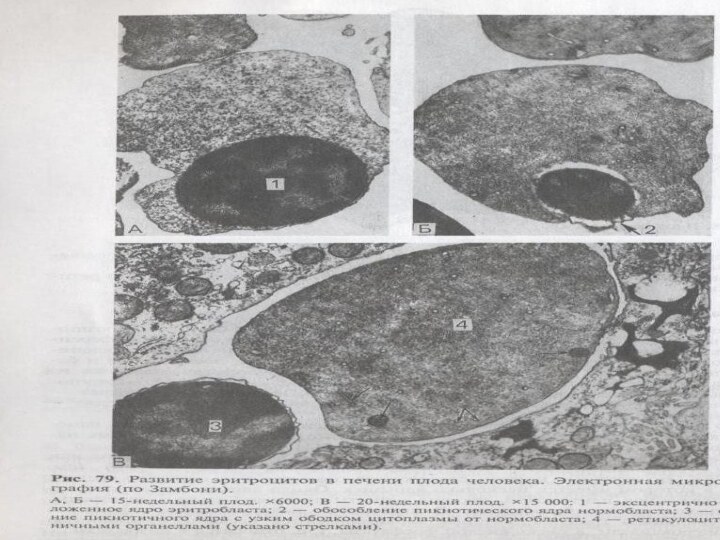
Кроветворение в печени
Печень закладывается примерно на 3—4-й неделе
эмбриональной жизни, а с 5-й недели она становится центром
кроветворения.
Кроветворение в печени происходит экстраваскулярно, - по ходу капилляров, врастающих вместе с мезенхимой внутрь печеночных долек.
Источником кроветворения в печени являются стволовые клетки крови, из которых образуются бласты, дифференцирующиеся во вторичные эритроциты.
Слайд 15
Кроветворение в печени
Одновременно с развитием эритроцитов в печени
образуются зернистые лейкоциты, главным образом нейтрофильные и эозинофильные.
Слайд 16
Кроветворение в печени
Кроме гранулоцитов, в печени формируются гигантские
клетки — мегакариоциты, - предшественники тромбоцитов.
К концу внутриутробного
периода кроветворение в печени прекращается.
Слайд 17
Кроветворение в тимусе
Тимус закладывается в конце 1-го месяца
внутриутробного развития, и на 7—8-й неделе его эпителий начинает
заселяться стволовыми клетками крови, которые дифференцируются в лимфоциты тимуса.
Увеличивающееся число лимфоцитов тимуса дает начало T-лимфоцитам, заселяющим T-зоны периферических органов иммунопоэза.
Слайд 18
Кроветворение в селезенке
Закладка селезенки также происходит в конце
1-го месяца эмбриогенеза.
Из вселяющихся сюда стволовых клеток происходит
экстраваскулярное образование всех видов форменных элементов крови, т.е. селезенка в эмбриональном периоде представляет собой универсальный кроветворный орган.
Образование эритроцитов и гранулоцитов в селезенке достигает максимума на 5-м месяце эмбриогенеза.
После этого в ней начинает преобладать лимфоцитопоэз.
Слайд 19
Кроветворение в лимфатических узлах
Первые закладки лимфатических узлов человека
появляются на 7—8-й неделе эмбрионального развития. Большинство лимфатических узлов
развивается на 9—10-й неделе.
В этот же период начинается проникновение в лимфатические узлы стволовых клеток крови, из которых на ранних стадиях дифференцируются эритроциты, гранулоциты и мегакариоциты.
Однако формирование этих элементов быстро подавляется образованием лимфоцитов, составляющих основную часть лимфатических узлов.
Слайд 20
Кроветворение в лимфатических узлах
Появление единичных лимфоцитов происходит уже
в течение 8—15-й недели развития, однако массовое «заселение» лимфатических
узлов предшественниками T- и B-лимфоцитов начинается с 16-й недели, когда формируются посткапиллярные венулы, через стенку которых осуществляется процесс миграции клеток.
Из клеток-предшественников дифференцируются сначала лимфобласты (или большие лимфоциты), а далее средние и малые лимфоциты.
Дифференцировка T- и B-лимфоцитов происходит, соответственно, в T- и B-зависимых зонах лимфатических узлов.
Слайд 21
Кроветворение в костном мозге
Закладка костного мозга осуществляется на
2-м месяце эмбрионального развития. Первые гемопоэтические элементы появляются на
12-й неделе развития; в это время основную массу их составляют эритробласты и предшественники гранулоцитов.
Из СКК в костном мозге формируются все форменные элементы крови, развитие которых происходит экстраваскулярно. Часть СКК сохраняется в костном мозге в недифференцированном состоянии. Они могут расселяться по другим органам и тканям и являться источником развития клеток крови и соединительной ткани.
Слайд 22
Кроветворение в костном мозге
Таким образом, костный мозг становится
центральным органом, осуществляющим универсальный гемопоэз, и остается им в
течение постнатальной жизни.
Он обеспечивает стволовыми кроветворными клетками тимус и другие гемопоэтические органы.
Слайд 24
Постэмбриональный гемопоэз
Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации
крови, который компенсирует физиологическое разрушение дифференцированных клеток.
Он подразделяется
на миелопоэз и лимфопоэз.
Слайд 25
Постэмбриональный гемопоэз
Миелопоэз происходит в миелоидной ткани, расположенной в
эпифизах трубчатых и полостях многих губчатых костей.
Здесь развиваются
эритроциты, гранулоциты, моноциты, тромбоциты, а также предшественники лимфоцитов.
В миелоидной ткани находятся стволовые клетки крови и соединительной ткани.
Предшественники лимфоцитов постепенно мигрируют и заселяют тимус, селезенку, лимфоузлы и некоторые другие органы.
Слайд 26
Постэмбриональный гемопоэз
Лимфопоэз происходит в лимфоидной ткани, которая имеет
несколько разновидностей, представленных в тимусе, селезенке, лимфоузлах.
Она выполняет
функции образования T- и B-лимфоцитов и иммуноцитов (например, плазмоцитов).
Слайд 27
Постэмбриональный гемопоэз
Миелоидная и лимфоидная ткани являются разновидностями соединительной
ткани, т.е. относятся к тканям внутренней среды.
В них
представлены две основные клеточные линии — клетки ретикулярной ткани и гемопоэтические клетки.
Слайд 28
Постэмбриональный гемопоэз
Ретикулярные, а также жировые, тучные и остеогенные
клетки вместе с межклеточным веществом формируют микроокружение для гемопоэтических
элементов.
Структуры микроокружения и гемопоэтические клетки функционируют в неразрывной связи друг с другом.
Микроокружение оказывает воздействие на дифференцировку клеток крови (при контакте с их рецепторами или путем выделения специфических факторов).
Слайд 29
Постэмбриональный гемопоэз
Таким образом, для миелоидной и всех разновидностей
лимфоидной ткани характерно наличие стромальных и гемопоэтических элементов, образующих
единое функциональное целое.
Слайд 30
Постэмбриональный гемопоэз
СКК относятся к самоподдерживающейся популяции клеток.
Они
редко делятся.
Выявление СКК стало возможным при применении метода
образования клеточных колоний – потомков одной стволовой клетки.
Слайд 31
Постэмбриональный гемопоэз
Пролиферативную активность СКК регулируют колониестимулирующие факторы (КСФ),
различные виды интерлейкинов (ИЛ-3 и др.).
Каждая СКК в эксперименте
или лабораторном исследовании образует одну колонию и называется колониеобразующей единицей (сокращенно КОЕ).
Слайд 32
Постэмбриональный гемопоэз
Исследование клеточного состава колоний позволило выявить две
линии их дифференцировки.
Одна линия дает начало мультипотентной клетке
— родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного рядов гемопоэза (сокращенно КОЕ-ГЭММ).
Вторая линия дает начало мультипотентной клетке — родоначальнице лимфопоэза (КОЕ-Л).
Слайд 33
Постэмбриональный гемопоэз
Из мультипотентных клеток дифференцируются олигопотентные (КОЕ-ГМ) и
унипотентные родоначальные клетки.
Методом колониеобразования определены родоначальные унипотентные клетки
для моноцитов (КОЕ-М), нейтрофильных гранулоцитов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Б), эритроцитов (БОЕ-Э и КОЕ-Э), мегакариоцитов (КОЕ-МГЦ), из которых образуются клетки-предшественники.
В лимфопоэтическом ряду выделяют унипотентные клетки — предшественницы для B-лимфоцитов и для T-лимфоцитов.
Полипотентные (плюрипотентные и мультипотентные), олигопотентные и унипотентные клетки морфологически не различаются.
Слайд 34
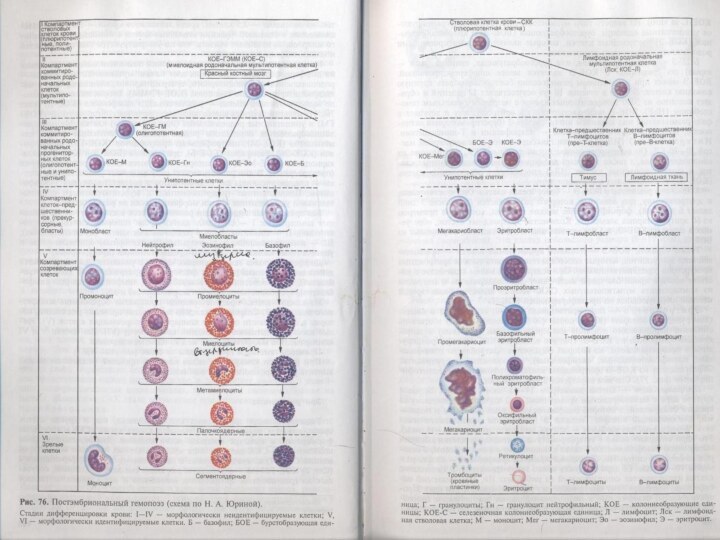
Все приведенные выше стадии развития клеток составляют четыре
основных класса, или компартмента, гемопоэза:
I класс — СКК -
стволовые клетки крови (плюрипотентные, полипотентные);
II класс — КОЕ-ГЭММ и КОЕ-Л - коммитированные мультипотентные клетки (миелопоэза или лимфопоэза);
III класс — КОЕ-М, КОЕ-Б и т.д. - коммитированные олигопотентные и унипотентные клетки;
IV класс — клетки-предшественники (бласты, напр.: эритробласт, мегакариобласт и т.д.).
Слайд 35
Сразу отметим, что оставшиеся два класса гемопоэза составляют
созревающие клетки (V класс) и зрелые клетки крови (VI
класс).
Слайд 36
Постэмбриональный гемопоэз
Эритропоэз у млекопитающих и человека протекает в
костном мозге в особых морфофункциональных ассоциациях, получивших название эритробластических
островков.
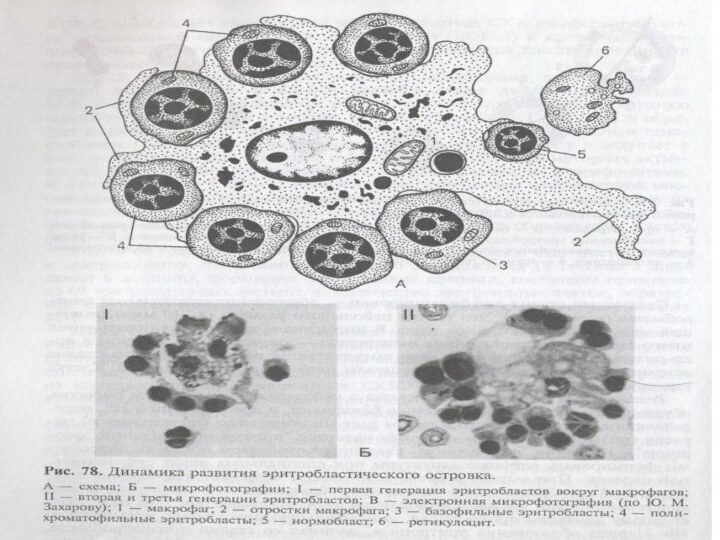
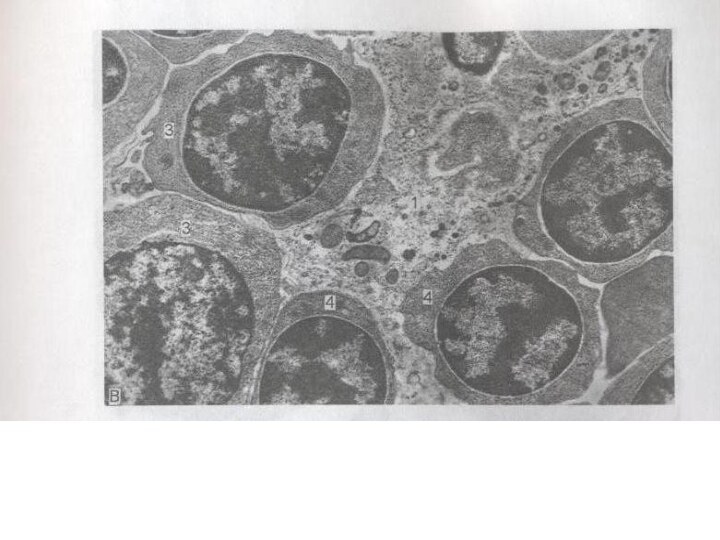
Эритробластический островок состоит из макрофага, окруженного одним или несколькими кольцами эритроидных клеток, развивающихся из унипотентной КОЕ-Э, вступившей в контакт с макрофагом.
КОЕ-Э и образующиеся из нее клетки (от проэритробласта до ретикулоцита) удерживаются в контакте с макрофагом его рецепторами.
Слайд 37
Постэмбриональный гемопоэз
У взрослого организма потребность в эритроцитах обычно
обеспечивается за счет усиленного размножения эритробластов.
Но всякий раз,
когда потребность организма в эритроцитах возрастает (например, при потере крови), эритробласты начинают развиваться из предшественников, а последние — из стволовых клеток.
В норме из костного мозга в кровь поступают только эритроциты и ретикулоциты.
Слайд 38
Эритроцитопоэз
Эритроцитопоэз начинается со стволовой кроветворной клетки.
Через стадию
колониеобразующей мультипотентной клетки (КОЕТЭММ) формируются бурстобразующая (БОЭ-Э) и далее
колониеобразующая единица эритроцитов (КОЕ-Э).
Клетки этих колоний чувствительны к факторам регуляции пролиферации и дифференцировки.
Слайд 40
Эритроцитопоэз
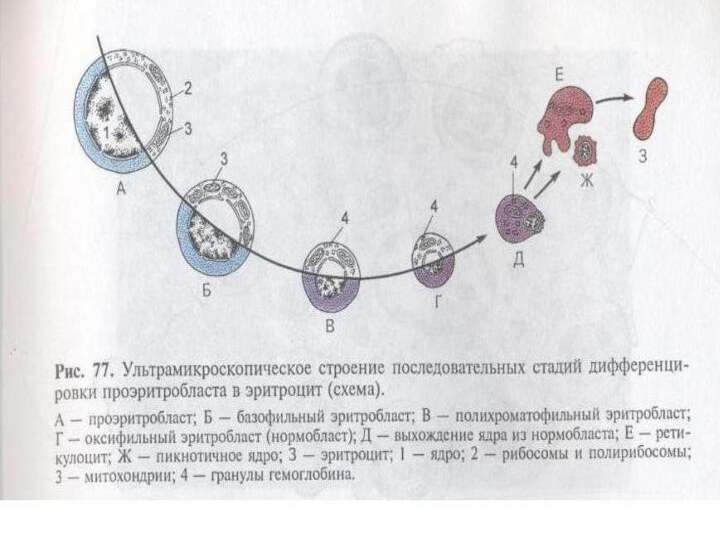
В IV-й класс включаются базофильный, полихроматофильный и оксифильный
эритробласты.
Проэритроциты, потом ретикулоциты составляют V-й класс и, наконец,
формируются эритроциты (VI-й класс).
В эритропоэзе на стадии оксифильного эритробласта происходит выталкивание ядра.
В целом цикл развития эритроцита до выхода ретикулоцита в кровь продолжается до 12 суток.
Слайд 41
Эритроцитопоэз
Общее направление эритропоэза характеризуется следующими основными структурно-функциональными изменениями:
1)постепенным
уменьшением размеров клетки
2)накоплением в цитоплазме гемоглобина
3)редукцией органелл
4)снижением базофилии и
повышением оксифилии цитоплазмы
5)уплотнением ядра с последующим его выделением из состава клетки.
В эритробластических островках эритробласты поглощают путем микропиноцитоза железо, поставляемое макрофагами, для синтеза гемоглобина.
Слайд 42
Эритроцитопоэз
Развитие эритроцитов происходит в миелоидной ткани красного костного
мозга.
В периферическую кровь поступают только зрелые эритроциты и
немного ретикулоцитов.
Слайд 43
Эритроцитопоэз
В норме потребность в эритроцитах обеспечивается за счет
размножения клеток IV-V классов. Этот процесс называется гомопластическим гемопоэзом.
При резком дефиците эритроцитов, вызванном кровопотерей или другими факторами, гомопластического гемопоэза оказывается недостаточно.
Эритроциты начинают развиваться путем деления клеток I-III-го классов.
Такой процесс называется гетеропластическим гемопоэзом.
Слайд 44
Эритроцитопоэз
Эритропоэтин – гликопротеиновый гормон, вызывающий повышение продукции эритроцитов.
У взрослого человека он образуется преимущественно в почках, а
в эмбриональном периоде практически полностью - в печени плода. Уменьшение содержания доступного кислорода в крови, достигающей почек, повышает выработку эритропоэтина, что, в свою очередь, вызывает увеличение скорости образования и дифференцировки клеток эритроидного ряда в костном мозге.
Эритропоэтин, таким образом, участвует в физиологическом ответе организма на анемию и гипоксию.
Слайд 45
Эритроцитопоэз
Проэритробласт - крупная клетка круглой формы.
Это самая
молодая клетка эритроидного ряда, имеющая круглое ядро, которое занимает
в клетке большее место, чем цитоплазма.
Ядро расположено в центре клетки, и содержит 1-3 ядрышка.
Структура хроматина ядра мелкосетчатая, образующая в пересечениях небольшие утолщения (зернистость).
При окраске по Романовскому ядро окрашивается в темно-красно-фиолетовый цвет, цитоплазма интенсивно базофильная.
Слайд 46
Эритроцитопоэз
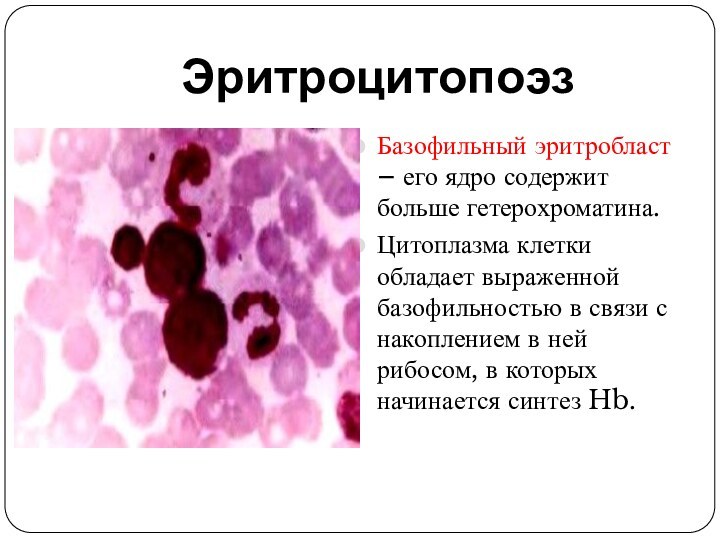
Базофильный эритробласт – его ядро содержит больше гетерохроматина.
Цитоплазма клетки обладает выраженной базофильностью в связи с накоплением
в ней рибосом, в которых начинается синтез Hb.
Слайд 47
Эритроцитопоэз
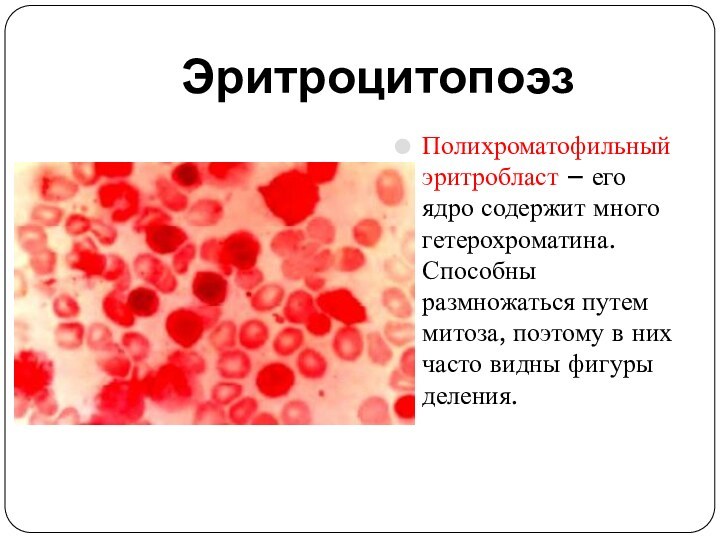
Полихроматофильный эритробласт – его ядро содержит много гетерохроматина.
Способны размножаться путем митоза, поэтому в них часто видны
фигуры деления.
Слайд 48
Эритроцитопоэз
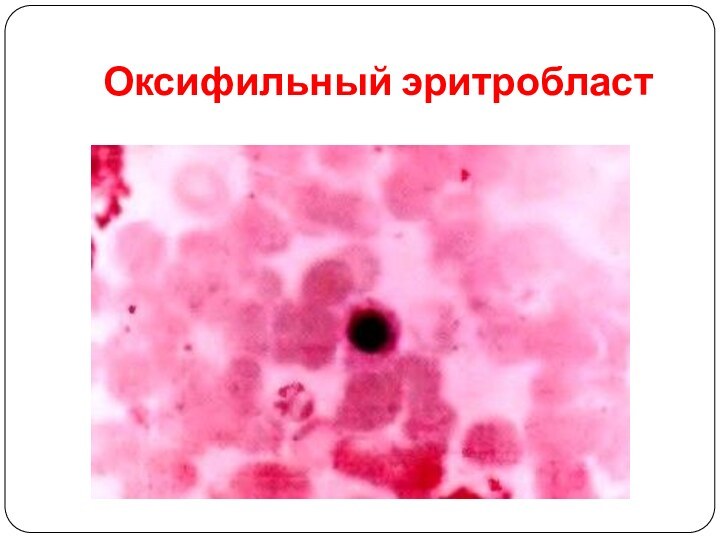
Оксифильный эритробласт - клетка округлой формы с бесструктурным
ядром темно-фиолетового цвета, по размеру еще меньше, чем у
предыдущих клеток. Ядро иногда расположено немного эксцентрично. Цитоплазма не содержит базофилию, она насыщена гемоглобином и по цвету сходна с эритроцитами. Клетка утрачивает способность к делению.
Слайд 50
Эритроцитопоэз
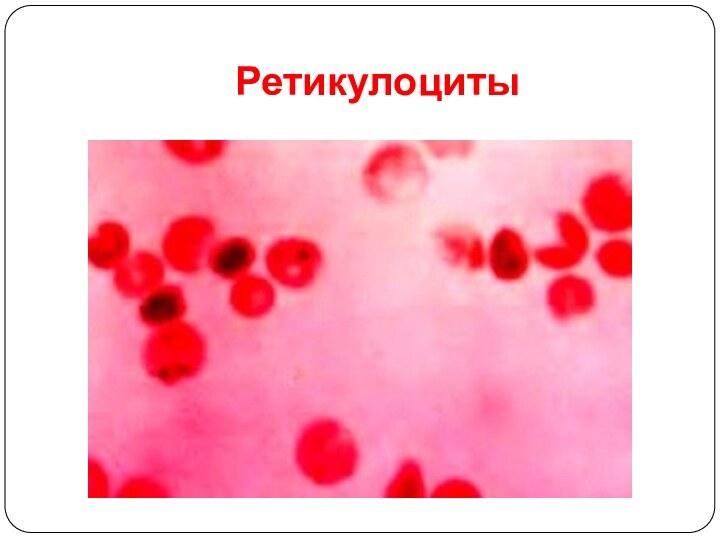
Ретикулоциты - это молодые эритроциты в которых выявляются
остатки РНК и митохондрий. Время созревания ретикулоцитов составляет 4-5
дней, из которых 3 дня они созревают в периферической крови. Находясь в костном мозге, ретикулоциты способны синтезировать гемоглобин.
Слайд 52
Эритроцитопоэз
Эритроциты (красные кровяные тельца) - безъядерные форменные элементы
крови, содержащие гемоглобин.
Основная функция эритроцитов - транспортировка кислорода
и углекислого газа.
Эритроциты составляют основную массу форменных элементов крови. Двояковогнутый диск эритроцита обеспечивает максимальное соотношение площади поверхности к объему.
Слайд 53
Эритроцитопоэз
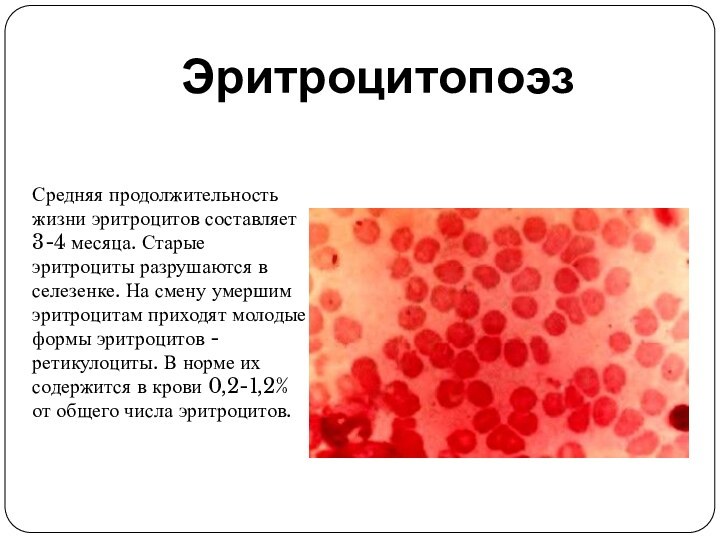
Средняя продолжительность жизни эритроцитов составляет 3-4 месяца. Старые
эритроциты разрушаются в селезенке. На смену умершим эритроцитам приходят
молодые формы эритроцитов - ретикулоциты. В норме их содержится в крови 0,2-1,2% от общего числа эритроцитов.
Слайд 55
Эритроцитопоэз
Эритропоэз у млекопитающих и человека протекает в костном
мозге в особых морфофункциональных ассоциациях, получивших название эритробластическим островком.
Слайд 56
Эритроцитопоэз
Эритробластический островок состоит из макрофага, окруженного одним или
несколькими кольцами эритроидных клеток, развивающихся из унипотентной КОЕ-Э, вступившей
в контакт с макрофагом.
Слайд 59
Гранулоцитопоэз
Гранулоцитопоэз - дифференцировка и созревание клеток гранулоцитопоэза происходит
в костном мозге. И образует гранулоциты трех видов:
1) Нейтрофилы
2)
Эозинофилы
3) Базофилы
Слайд 60
Гранулоцитопоэз
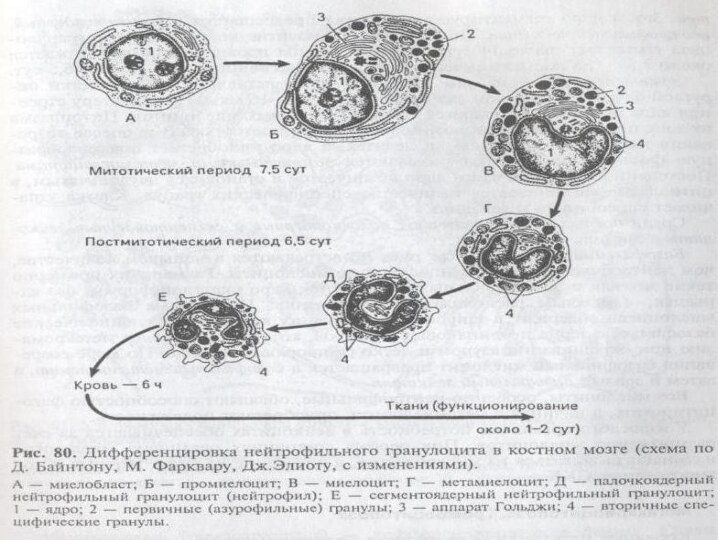
Основные ряды для каждой из групп гранулоцитов слагаются
из следующих клеточных форм:
СКК
КОЕ-ГЭММ КОЕ-ГЭМ унипотентные предшественники(КОЕ-Б, КОЕ-Эо, КОЕ-Гн) миелобласт промиелоцит
миелоцит метамиелоцит палочкоядерный гранулоцит сегментоядерный гранулоцит.
Слайд 61
Гранулоцитопоэз
Миелобласты -это крупные клетки, содержащие овальное или округлое
светлое ядро, в котором имеется несколько ядрышек.
Около ядра располагается
ясно выраженная центросома, хорошо развиты аппарат Гольджи, лизосомы.
Миелобласты являются родоначальниками нейтрофилов, эозинофилов и базофилов.
В обычном костном мозге эозинофильные и базофильные миелобласты неразличимы.
Базофильные миелобласты определяются в случае хронического миелолейкоза, когда в крови содержится большое количество зрелых базофилов.
Слайд 62
Гранулоцитопоэз
Промиелоциты делятся миотически. Специфическая зернистость отсутствует.
Нейтрофильные, или гетерофильные,
миелоциты клетки размножаются митозом.
В миелоцитах обнаруживаются все органеллы.
Количество митохондрий невелико.
ЭПС состоит из пузырьков.
Рибосомы располагаются на поверхности мембранных пузырьков, а также диффузно в цитоплазме.
Слайд 65
Гранулоцитопоэз
По мере размножения нейтрофильных миелоцитов округлое или овальное
ядро становится бобовидным.
Начинает окрашиваться темнее.
Хроматиновые глыбки становятся грубыми.
Ядрышки исчезают.
Такие
клетки уже не делятся. Это метамиелоциты.
Слайд 66
Гранулоцитопоэз
Полный период развития нейтрофильного гранулоцита составляет около 14
суток, при этом период пролиферации продолжается около 7,5 суток,
а постмиотический период дифференцировки- около 6,5 суток.
Слайд 67
Гранулоцитопоэз
Эозинофильные миелоциты - это большие круглые клетки, с
крупным круглым, овальным или почковидным ядром и сравнительно небольшим
количеством протоплазмы.
Ядро обладает особой структурой, зависящей от чередования более темных и светлых участков хроматина; это создает впечатления складчатости.
Оно окрашивается в красновато-фиолетовый цвет, менее интенсивно у более юных миелоцитов и более интенсивно у более зрелых. Протоплазма содержит обильную зернистость - нейтрофильную, эозинофильную или базофильную, в зависимости от которой клетка относится к типу нейтрофильных, эозинофильных или базофильных лейкоцитов.
Слайд 68
Гранулоцитопоэз
Базофильные миелоциты – ядро округлой формы, без ядрышек,
с рыхлым расположением хроматина.
По мере созревания базофильный миелоцит
превращается в базофильный метамиелоцит, а затем в зрелый базофильный лейкоцит.
Слайд 69
Гранулоцитопоэз
Все миелоциты обладают способностью фагоцитировать, а начиная с
метамиелоцита, приобретает подвижность.
Слайд 70
Мегакариоцитопоэз.Тромбоцитопоэз
Кровяные пластинки образуются из гигантских клеток красного костного
мозга — мегакариоцитов. Последовательность стадии дифференцировки можно представить след.рядом
клеток:
СКК КОЕ-ГЭММ КОЕ-МГЦ мегакариобласт промегакариоцит тромбоциты(кровяные пластинки).
Слайд 71
Мегакариоцитопоэз.Тромбоцитопоэз
Мегакариобласт — предшественник клетки промегакариоцита, которая в свою
очередь, становится мегакариоцитом во время гемопоэза. Она начинает серию
тромбоцитов.
Мегакариобласт — самый большой из известных бласт костного мозга.
Ядро округлой формы с 2-4 ядрышками.
Структура хроматина крупно-сетчатая, некоторые нити высокой плотности.
Базофилия цитоплазмы очень сильная, гранулы отсутствуют.
Слайд 72
Мегакариоцитопоэз.Тромбоцитопоэз
Промегакариоцит – содержит полиплоидные ядра – тетраплоидные, октаплоидные
(4n, 8n), несколько пар центриолей.
Клетка также способна к эндомитозу
и дальнейшему увеличению плоидности ядер.
Слайд 74
Мегакариоцитопоэз.Тромбоцитопоэз
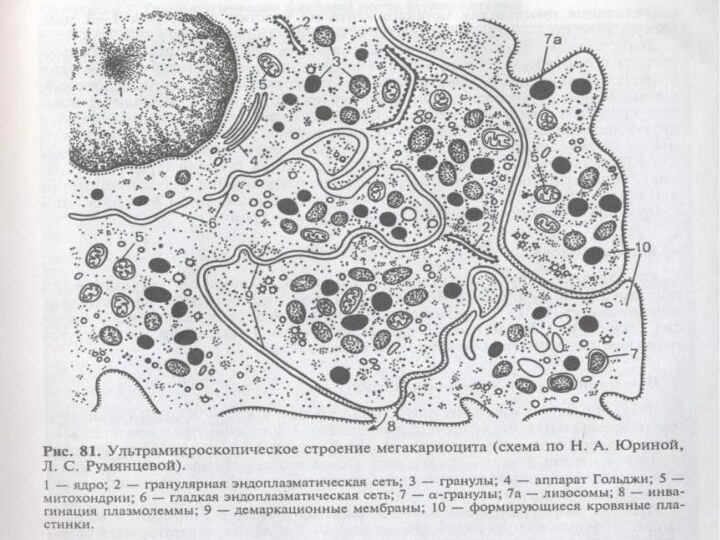
Мегакариоциты — это гигантские клетки костного мозга. Они
имеют крупное ядро. От них отшнуровываются тромбоциты, представляющие собой
фрагменты цитоплазмы мегакариоцитов, окруженные мембраной.
Отшнуровывание тромбоцитов от мегакариоцитов усиливается тромбопоэтином, глюкокортикоидами.
Слайд 75
Мегакариоцитопоэз.Тромбоцитопоэз
Мегакариоциты высокочувствительны к воздействию цитостатических препаратов, поэтому при
химиотерапии злокачественных опухолей часто развивается тромбоцитопения.
Однако мегакариоциты менее чувствительны
к цитостатическим воздействиям, чем гранулоцитарный росток костного мозга, поэтому обычно при химиотерапии опухолей более серьёзную проблему представляет выраженная лейкопения, в особенности нейтропения.
Слайд 76
Моноцитопоэз
Образование моноцитов происходит из стволовых клеток костного мозга
по схеме:
СКК КОЕ-ГЭММ
унипотентный предшественник моноцита(КОЕ-М) монобласт промоноцит моноцит.
Моноциты из крови поступают в ткани, где являются источником развития различных видов макрофагов.
Слайд 77
Лимфоцитопоэз и иммуноцитопоэз
Лимфоидная ткань у человека имеется
в составе лимфатических узлов, селезенки, миндалин, аппендикса и в
других лимфоидных образованиях по ходу пищеварительного тракта. В лимфоидной ткани происходит лимфопоэз.
Исходными клетками лимфопоэза являются стволовые клетки красного костного мозга.
Через стадию мультипотентных клеток (КОЕ-Л) они дифференцируются в родоначальные про-Т- и про-В-лимфобласты и далее в Т- и В-лимфобласты, Т- и В-пролимфоциты и Т- и В-лимфоциты.
Слайд 78
Лимфоцитопоэз и иммуноцитопоэз
Процесс дифференцировки Т-лимфоцитов в тимусе
приводит к образованию из унипотентных предшественников Т-бластов, из которых
формируется эффекторные лимфоциты- киллеры, хелперы, супрессоры.
Слайд 79
Лимфоцитопоэз и иммуноцитопоэз
В лимфоцитопоэзе в тимусе возникают
субпопуляции Т-клеток с различными рецепторами (так называемая антигеннезависимая пролиферация
и дифференцировка).
Т-лимфоциты участвуют в формировании клеточного иммунитета.
Другой ряд дифференцировки в лимфопоэзе приводит к образованию из В-лимфоцитов через стадии плазмобласта и проплазмоцита — плазматических клеток (плазмоцитов).
Эти клетки вырабатывают антитела, обеспечивая гуморальный иммунитет.
Слайд 80
Регуляция гемопоэза
Кроветворение регулируется:
Факторами роста, обеспечивающими пролиферацию и дифференцировку
СКК и последующих стадий их развития,
Факторами транскрипции, влияющими на
экспрессию генов, определяющих направление дифференцировки гемопоэтических клеток,
Витаминами, гормонами.
Слайд 81
Регуляция гемопоэза
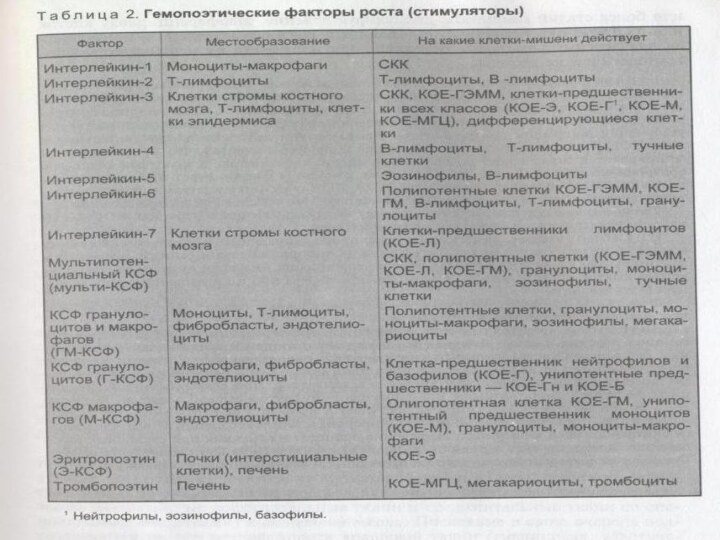
Факторы роста включают колониестимулирующие факторы (КСФ), интерлейкины
и ингибирующие факторы. Они являются гликопротеинами, действующими и как
циркулирующие гормоны, и как местные медиаторы, регулирующие гемопоэз и дифференцировку специфических типов клеток. Почти все факторы роста действуют на СКК, КОЕ, коммитированные и зрелые клетки. Однако отмечаются индивидуальные особенности действия этих факторов на клетки-мишени.
Слайд 82
Регуляция гемопоэза
КСФ действуют на специфические клетки или группы
клеток на различных стадиях дифференцировки. Например, фактор роста стволовых
клеток влияет на пролиферацию и миграцию СКК в эмбриогенезе. В постнатальном периоде на гемопоэз оказывают влияние несколько КСФ, среди которых наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ), а также интерлейкины.
Слайд 83
Регуляция гемопоэза
Большинство указанных факторов выделено и применяется для
лечения различных болезней. Для получения их используются биотехнологические методы.
Дифференцировка
полипотентных клеток в унипотентные определяется действием ряда специфических факторов, поэтинов — эритропоэтинов (для эритробластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лимфобластов), тромбопоэтинов (для мегакариобластов).
Слайд 84
Регуляция гемопоэза
Большая часть эритропоэтина образуется в почках. Его
образование регулируется содержанием в крови кислорода, которое зависит от
количества циркулирующих в крови эритроцитов. Снижение числа эритроцитов и соответственно парциального давления кислорода, является сигналом для увеличения продукции эритропоэтина.
Тромбопоэтин синтезируется в печени, стимулирует пролиферацию КОЕ-МГЦ, их дифференцировку и образование тромбоцитов.
Слайд 85
Регуляция гемопоэза
Ингибирующие факторы дают противоположный эффект, т.е. тормозят
гемопоэз; их недостаток может быть одной из причин лейкемии,
характеризующейся значительным увеличением числа лейкоцитов в крови. Выделен ингибирующий лейкемию фактор (ЛИФ), который тормозит пролиферацию и дифференцировку моноцитов-макрофагов.
Слайд 86
Регуляция гемопоэза
Витамины необходимы для стимуляции пролиферации и дифференцировки
гемопоэтических клеток. Витамин В12 поступает с пищей и соединяется
с внутренним фактором (Касла), который синтезируется париетальными клетками желудка. Образуемый при этом комплекс, в присутствии ионов Са2+, соединяется с рецепторами эпителиоцитов подвздошной кишки и всасывается.
Слайд 87
Регуляция гемопоэза
При всасывании в эпителиоциты поступает лишь витамин
В12, а внутренний фактор освобождается. Витамин В12 поступает с
кровью в костный мозг, где влияет на гемопоэз, и в печень, где может депонироваться. Нарушение процесса всасывания при различных заболеваниях желудочно-кишечного тракта может служить причиной дефицита витамина В12 и нарушений в гемопоэзе.