Слайд 2
Главную роль в противоинфекционной защите играет не иммунитет,
а разнообразные механизмы механического удаления микроорганизмов (клиренса)
В органах дыхания
– это продукция сурфактанта и мокроты, перемещение слизи за счет движений ресничек цилиарного эпителия, кашля и чихания.
В кишечнике – это перистальтика и выработка соков и слизей (диарея при инфекции и т.п.)
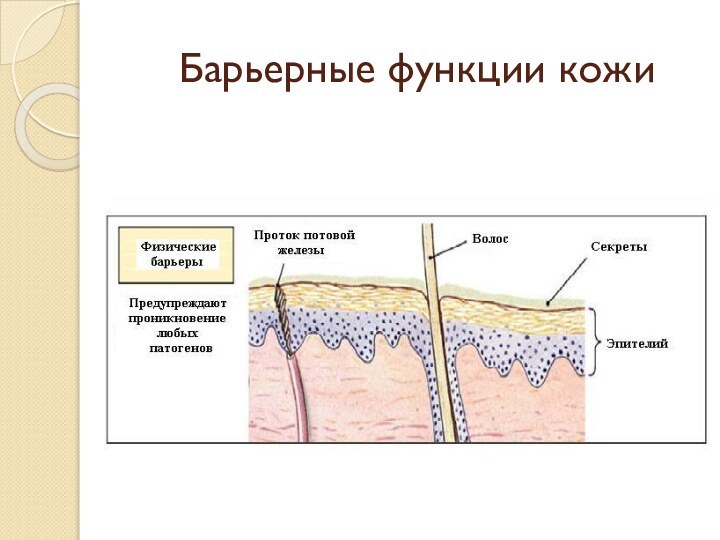
На коже это постоянное слущивание и обновление эпителия.
Система иммунитета включается тогда, когда механизмы клиренса не справляются.
Слайд 6
Таким образом, чтобы выжить в организме хозяина микроб
должен «закрепиться» на эпителиальной поверхности (иммунологи и микробиологи называют
это адгезией, то есть, приклеиванием)
Организм должен препятствовать адгезии, используя механизмы клиренса.
Если адгезия произошла, то микроб может попытаться проникнуть вглубь ткани или в кровоток, где механизмы клиренса не работают.
В этих целях микробы вырабатывают ферменты, разрушающие ткани хозяина
Все патогенные микроорганизмы отличаются от непатогенных способностью вырабатывать такие ферменты
Слайд 7
Если тот или иной
механизм клиренса
не справляется
с инфекцией, то в борьбу включается система иммунитета.
Слайд 8
Специфическая
и
неспецифическая иммунная защита
Под специфической защитой понимаются
специализированные лимфоциты, которые могут бороться только с одним антигеном.
Неспецифические
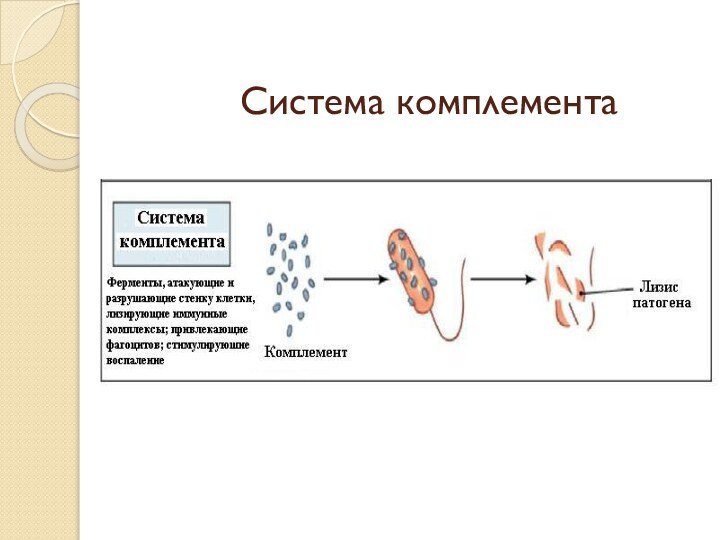
факторы иммунитета, такие как фагоциты, естественные киллерные клетки и комплемент (особые ферменты) могут бороться с инфекцией как самостоятельно, так и в кооперации со специфической защитой.
Слайд 11
Система иммунитета состоит из:
иммунных клеток,
ряда
гуморальных факторов,
органов иммунитета (вилочковой железы, селезенки, лимфоузлов), а
также скоплений лимфоидной ткани (наиболее массивно представленных
в органах дыхания и пищеварения).
Слайд 12
Органы иммунитета сообщаются между собой и с тканями
организма через лимфатические сосуды и систему кровообращения.
Слайд 13
Различают четыре основных типа патологических состояний иммунной системы:
1.
реакции гиперчувствительности, проявляющиеся в виде иммунного повреждения тканей;
2. аутоиммунные
болезни, развивающиеся в результате иммунных реакций против собственного организма;
3. синдромы иммунного дефицита, возникающие вследствие врождённого или приобретённого дефекта иммунного ответа;
4. амилоидоз.
Слайд 14
РЕАКЦИИ ГИПЕРЧУВСТВИТЕЛЬНОСТИ
Контакт организма с антигеном не только обеспечивает
развитие защитного иммунного ответа, но и может привести к
реакциям, повреждающим ткани. Такие реакции гиперчувствительности (иммунного повреждения тканей) могут быть инициированы взаимодействием антигена с антителом или клеточными иммунными механизмами. Эти реакции могут быть связаны не только с экзогенными, но и с эндогенными антигенами.
Слайд 15
Болезни гиперчувствительности классифицируют на основе иммунологических механизмов, их
вызывающих.
Классификация
Выделено четыре типа реакций гиперчувствительности:
Тип I — иммунный ответ
сопровождается высвобождением вазо- активных и спазмогенных веществ.
Тип II — антитела участвуют в повреждении клеток, делая их восприимчивыми к фагоцитозу или лизису.
Тип III — взаимодействие антител с антигенами приводит к образованию иммунных комплексов, активирующих комплемент. Фракции комплемента привлекают нейтрофилы, повреждающие ткани;
Тип IV — развивается клеточный иммунный ответ с участием сенсибилизированных лимфоцитов.
Слайд 16
Реакции гиперчувствительности I типа
(немедленный тип, аллергический тип)
могут быть местными или системными.
Системная реакция развивается в ответ
на внутривенное введение антигена, к которому организм хозяина предварительно сенсибилизирован, и может носить характер анафилактического шока.
Местные реакции зависят от места проникновения антигена и имеют характер ограниченного отёка кожи (кожная аллергия, крапивница), выделений из носа и конъюнктив (аллергический ринит, конъюнктивит), сенной лихорадки, бронхиальной астмы или аллергического гастроэнтерита (пищевая аллергия).
Слайд 18
Реакции гиперчувствительности I типа проходят в своём развитии
две фазы — инициального ответа и позднюю:
- Фаза инициального
ответа развивается через 5—30 мин после контакта с аллергеном и характеризуется расширением сосудов, повышением их проницаемости, а также спазмом гладкой мускулатуры или секрецией желёз.
- Поздняя фаза наблюдается через 2—8 ч без дополнительных контактов с антигеном, продолжается несколько дней и характеризуется интенсивной инфильтрацией тканей эозинофилами, нейтрофилами, базофилами и моноцитами, а также повреждением эпителиальных клеток слизистых оболочек. Развитие гиперчувствительности I типа обеспечивают IgE-антитела, образующиеся в ответ на аллерген при участии
Т2-хелперов.
Слайд 19
Реакция гиперчувствительности
I типа лежит в основе развития
анафилактического шока.
Системная анафилаксия возникает после введения гетерологичных белков
— антисывороток, гормонов, ферментов, полисахаридов, некоторых лекарств (например пенициллина).
Слайд 20
Реакции гиперчувствительности II типа (реакция немедленной повышенной чувствительности)
обусловлена IgG-антителами к экзогенным антигенам, адсорбированным на клетках или
внеклеточном матриксе. При таких реакциях в организме появляются антитела, направленные против клеток собственных тканей. Антигенные детерминанты могут образовываться в клетках в результате нарушений на генном уровне, приводящих к синтезу атипичных белков или же представляют собой экзогенный антиген, адсорбированный на поверхности клетки или внеклеточном матриксе. В любом случае реакция гиперчувствительности возникает как следствие связывания антител с нормальными или повреждёнными структурами клетки или внеклеточного матрикса.
Слайд 21
Реакции гиперчувствительности III типа (реакция немедленной повышенной чувствительности,
обусловленная взаимодействием IgG-антител и растворимым экзогенным антигеном)
Развитие таких реакций
обусловлено наличием комплексов «антиген—антитело», образующихся в результате связывания антигена с антителом в кровеносном русле (циркулирующие иммунные комплексы) или вне сосудов на поверхности или внутри клеточных (или внеклеточных) структур (иммунные комплексы in situ).
Слайд 22
Циркулирующие иммунные комплексы (ЦИК) вызывают повреждение при попадании
в стенку кровеносных сосудов или в фильтрующие структуры (кпубочковый
фильтр в почках).
Известны два типа иммунокомплексных повреждений, которые формируются при поступлении в организм экзогенного антигена (чужеродный белок, бактерия, вирус) и при образовании антител против собственных антигенов.
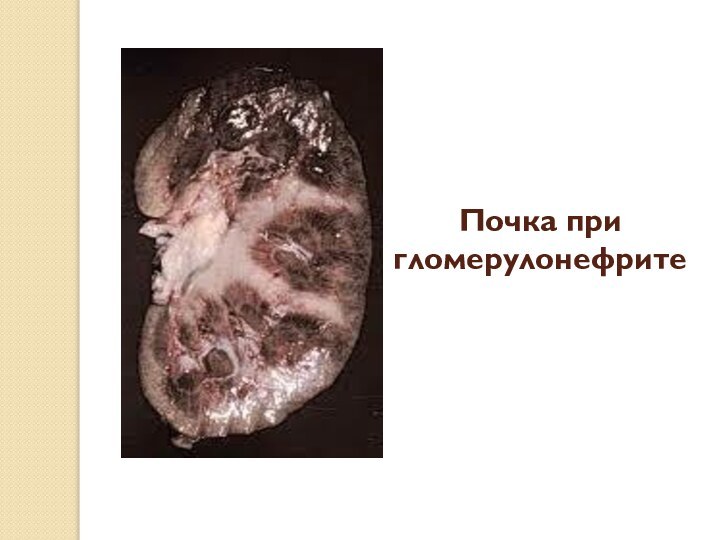
Заболевания, обусловленные наличием иммунных комплексов, могут быть генерализованными, если эти комплексы образуются в крови и оседают во многих органах, или связанными с отдельными органами, такими, как почки (гломерулонефрит), суставы (артрит) или мелкие кровеносные сосуды кожи.
Слайд 24
Системная иммунокомплексная болезнь
Одной из её разновидностей является острая
сывороточная болезнь, возникающая в результате пассивной иммунизации, возникающей в
результате многократного введения больших доз чужеродной сыворотки.
Слайд 25
Хроническая сывороточная болезнь
развивается при продолжительном контакте с антигеном.
Постоянная антигенемия необходима для развития хронической иммунокомплексной болезни, так
как иммунные комплексы чаще всего оседают в сосудистом русле.
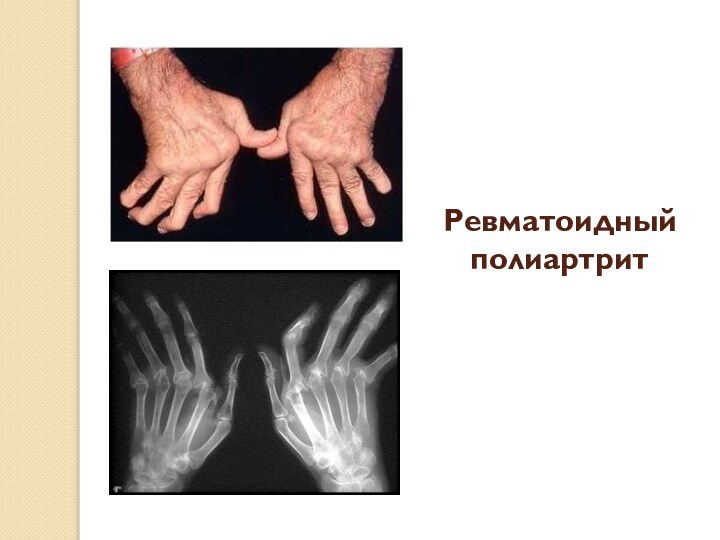
Например, системная красная волчанка связана с долгим сохранением (персистенцией) аутоантигенов. Часто, несмотря на наличие характерных морфологических изменений и других признаков, свидетельствующих о развитии иммунокомплексной болезни, антиген остаётся неизвестным. Такие явления характерны для ревматоидного артрита, узелкового периартериита, мембранозной нефропатии и некоторых васкулитов.
Слайд 29
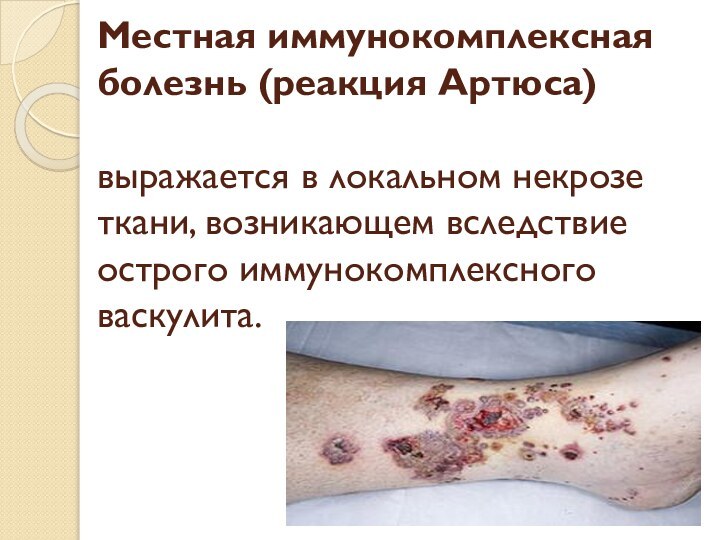
Местная иммунокомплексная болезнь (реакция Артюса)
выражается в локальном некрозе
ткани, возникающем вследствие острого иммунокомплексного васкулита.
Слайд 30
Реакции гиперчувствительности IV типа (замедленного типа)
развиваются с
участием специфически сенсибилизированных Т-лимфоцитов. Это основной тип иммунного ответа
на различные внутриклеточные микробиологические агенты, особенно микобактерии туберкулёза, а также на многие вирусы, грибы, простейшие и паразиты. Другим ярким примером является реакция отторжения — трансплантат против хозяина.
Слайд 31
Гиперчувствительность замедленного типа (ГЗТ) складывается из нескольких этапов:
1
— первичный контакт с антигеном обеспечивает накопление специфических Т,-хелперов;
2
— при повторном введении того же антигена происходит его захват региональными макрофагами, которые выступают в роли антиген-представляющих клеток, выводя фрагменты антигена на свою поверхность;
3 — антигенспецифические Т-хелперы взаимодействуют с антигеном на поверхности макрофагов и секретируют ряд цитокинов;
4 — секретируемые цитокины обеспечивают формирование воспалительной реакции, сопровождающейся накоплением моноцитов/макрофагов, продукты которых разрушают близлежащие клетки хозяина.
Слайд 32
При персистенции антигена макрофаги трансформируются в эпителиоидные клетки,
окружённые валом из лимфоцитов, — формируется гранулёма.
Такое воспаление
характерно для гиперчувствительности IV типа и называется гранулематозным.
Слайд 33
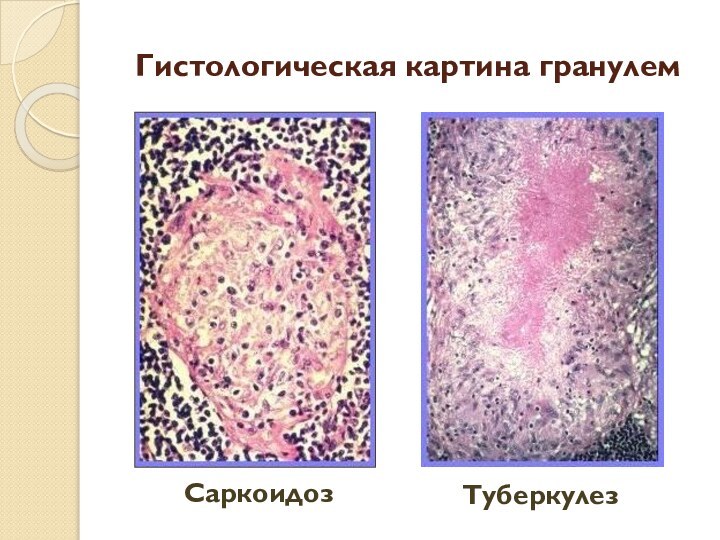
Гистологическая картина гранулем
Саркоидоз
Туберкулез
Слайд 34
АУТОИММУННЫЕ БОЛЕЗНИ
Нарушения иммунологической толерантности приводят к своеобразной иммунологической
реакции на собственные антигены организма — аутоиммунной агрессии и
формированию состояния аутоиммунитета.
В норме аутоантитела могут быть найдены в сыворотке крови или тканях у многих здоровых людей, особенно в старшей возрастной группе. Эти антитела образуются после повреждения ткани и играют физиологическую роль в удалении её остатков.
Слайд 35
Различают три основных признака аутоиммунных заболеваний:
- наличие аутоиммунной
реакции;
- наличие клинических и экспериментальных данных о том, что
такая реакция не вторична к повреждению ткани, а имеет первичное патогенетическое значение;
- отсутствие иных определённых причин болезни.
Слайд 36
В то же время встречаются состояния, при которых
действие аутоантител направлено против собственного органа или ткани, в
результате развивается местное повреждение ткани.
Например, при тиреоидите Хашимото (зоб Хашимото) антитела абсолютно специфичны для щитовидной железы. При системной красной волчанке разнообразные аутоантитела реагируют с составными частями ядер различных клеток, а при синдроме Гудпасчера антитела против базальной мембраны лёгких и почек вызывают повреждения только в этих органах. Очевидно, что аутоиммунитет подразумевает потерю аутотолерантности.
Иммунологическая толерантность — состояние, при котором иммунный ответ на специфический антиген не развивается.
Слайд 37
СИНДРОМЫ ИММУННОГО ДЕФИЦИТА
Иммунологическая недостаточность (иммунодефицит) — патологическое состояние,
обусловленное дефицитом компонентов, факторов или звеньев иммунной системы с
неизбежными нарушениями иммунного надзора и/или иммунного ответа на чужеродный антиген.
Слайд 38
Все иммунодефициты подразделяют на первичные (почти всегда детерминированы
генетически,) и вторичные (связаны с осложнениями инфекционных заболеваний, нарушениями
метаболизма, побочными эффектами иммуносупрессии, облучением, химиотерапией при онкологических заболеваниях).
Первичные иммунодефициты — гетерогенная группа врождённых, генетически детерминированных заболеваний, обусловленных нарушениями
дифференцировки и созревания Т- и В - лимфоцитов.
Слайд 39
По данным ВОЗ, существует более 70 первичных иммунодефицитов.
Несмотря на то, что большинство иммунодефицитов встречается довольно редко,
некоторые из них
(например дефицит IgA) достаточно распространены, особенно у детей.
Слайд 40
Приобретённые (вторичные) иммунодефициты
Если иммунодефицит становится основной причиной развития
персистирующего или часто рецидивирующего инфекционного или опухолевого процесса, можно
говорить о синдроме вторичной иммунной недостаточности (вторичном иммунодефиците).
Слайд 41
Синдром приобретённого иммунодефицита (СПИД)
К началу XXI в. СПИД
зарегистрирован в более чем 165 странах мира, а наибольшее
количество инфицированных вирусом иммунодефицита человека (ВИЧ) находится в Африке и Азии.
Среди взрослых людей идентифицировано 5 групп риска:
- гомосексуальные и бисексуальные мужчины составляют наиболее крупную группу (до 60% больных);
- лица, которые вводят внутривенно наркотики (до 23%);
- больные гемофилией (1%);
- реципиенты крови и её компонентов (2%);
- гетеросексуальные контакты членов других групп повышенного риска, преимущественно наркоманов — (6%).
Приблизительно в 6% случаев факторы риска не определяются. Около 2% больных СПИДом — дети.
Слайд 42
Этиология
Возбудитель СПИДа — вирус иммунодефицита человека — ретровирус
семейства лентивирусов. Различают две генетически разные формы вируса: вирусы
иммунодефицита человека 1 и 2 (HIV-1 и HIV-2, или ВИЧ-1 и ВИЧ-2).
ВИЧ-1 наиболее распространённый тип, встречается в США, Европе, Центральной Африке, а ВИЧ-2 — главным образом в Западной Африке.
Слайд 43
Патогенез
Существуют две основные мишени для ВИЧ: иммунная система
и центральная нервная система.
Иммунопатогенез СПИДа характеризуется развитием глубокой
иммунодепрессии, что главным образом связано с выраженным уменьшением количества CD4 Т- клеток. Имеется множество оказательств того, что молекула CD4 фактически является высокоаффинным рецептором для ВИЧ.
Это объясняет селективный тропизм вируса к CD4 Т-клеткам.
Слайд 44
Течение СПИДа складывается из трёх фаз, отражающих динамику
взаимодействия вируса с хозяином:
- ранней острой фазы,
-
средней хронической,
- и финальной кризисной фаз.
Слайд 45
Острая фаза. Развивается первоначальный ответ иммунокомпе- тентного индивидуума
на вирус. Эта фаза характеризуется высоким уровнем образования вируса,
виремией и распространённым обсеменением лимфоидной ткани, но инфекция ещё контролируется с помощью антивирусного иммунного ответа.
Хроническая фаза — период относительного сдерживания вируса, когда иммунная система интактна, но наблюдается слабая репликация вируса, преимущественно в лимфоидной ткани. Эта фаза может продолжаться несколько лет.
Финальная фаза характеризуется нарушением защитных механизмов хозяина и безудержной репликацией вируса. Снижается содержание CD4 Т-клеток. После неустойчивого периода появляются серьёзные оппортунистические инфекции, опухоли, поражается нервная система.
Слайд 46
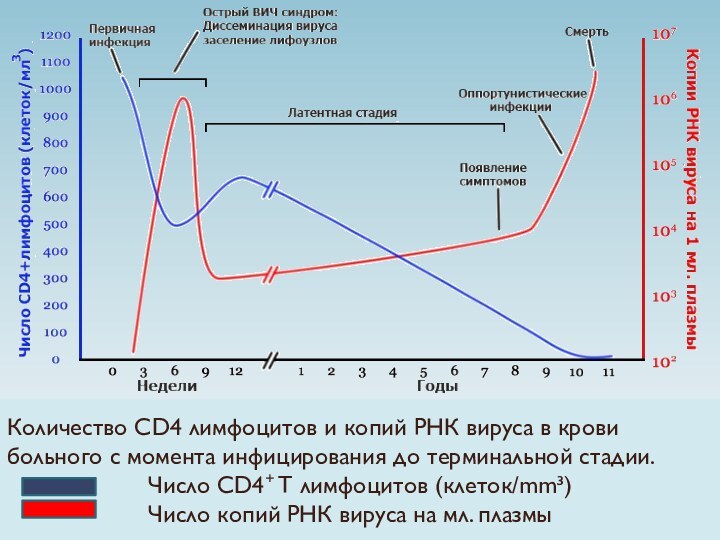
Количество CD4 лимфоцитов и копий РНК вируса в
крови больного с момента инфицирования до терминальной стадии.
Число CD4+ T лимфоцитов (клеток/mm³)
Число копий РНК вируса на мл. плазмы