- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Соли.
Содержание
- 2. ВеществаПростыеСложныеМеталлыНеметаллыОксидыОснования?Кислоты
- 3. NOHNONaOHHNO23К какому классу соединений относятся вещества, дать им названия
- 4. Задание1На какие группы и по каким признакам
- 5. ВеществаПростыеСложныеМеталлы Аl, Ca, Na НеметаллыS,
- 6. Задание 2Вставьте пропущенный фрагмент.S------ SО2 ----- H2SO3
- 7. проверкаS------ SО2 ----- H2SO3 Na----Na2O ----- NaОН
- 9. СОЛИ ,как производные кислот и оснований.Их состав и номенклатура (название).
- 10. СОЛИNaOHHClNaCl+-+_
- 11. Соли - это сложные вещества, которые состоят из ионов металла и кислотного остатка.
- 12. Задание.Определить : почему у солей разное
- 13. 3адание.Na+1
- 14. задание 4.Определить : почему у солей
- 15. Так как кислотные остатки имеют свою степень
- 16. Выведем общую формулу солей? Ме+n m(К. О.-m)n
- 17. Алгоритм названия солей++=
- 18. Алгоритм названия солейFe+2(NO3-1)2 – нитрат железа (II)Fe
- 19. задание 5. НАЗОВИТЕ СОЛИNaCl Fe +2SO4
- 20. задание
- 21. Контрольное задание1 Установите соответствие между формулой вещества и его названием
- 22. 2. Составление формул солей по их названиям.
- 23. 1. Запиши рядом знаки химических элементов, которые
- 24. 2. Над знаками химических элементов поставь их степень окисления.Пример:FeSO4+3-2Второй пункт выполнили переходим к третьему
- 25. 3. Определи Н.О.К. чисел выражающих степень окисления
- 26. 4. Раздели Н.О.К. на степень окисления каждого
- 27. Составить формулу сульфата алюминия: (второй способ)Составить формулы:
- 28. Составьте формулу хлорида кальцияСаCl2Составьте формулу нитрата натрияNaNO3Zn(SO4)2Cu
- 29. 3. Отдельные Представители стр.77 в таблицу хлорид натрия
- 30. NaCl
- 31. "Среди всех природных минеральных солей, самая главная
- 32. За
- 33. Соль в геральдике российских городовГерб Соликамска Герб Солигалича Герб Сольвычегодска Герб Соль-ИлецкаГерб Усолья-СибирскогоГерб Дрогобыча
- 34. Добыча солииз соляных шахтиз соленых озер
- 35. На озере Баскунчак ежегодно добывается около 5 млн. тонн соли
- 36. Применение NaCl
- 38. Моллюски, раки, радиолярии, кораллы – все имеют известковый скелет
- 39. Большой Барьерный риф
- 40. Меловые горы
- 41. Минералы карбоната кальция находятся в горных породах:Известняк МелМрамор Мрамор Мрамор МраморТравертин
- 42. Мрамор – строительный материалЕдинственное в России здание,
- 43. Д/З: Фосфат кальция
- 48. Контрольное задание - итоговоеЧасть А (задания
- 49. Контрольное задание - итоговоеЧасть В Выбери
- 50. Контрольное задание - итоговоеЧасть А ГАЧасть В
- 51. Скачать презентацию
- 52. Похожие презентации
ВеществаПростыеСложныеМеталлыНеметаллыОксидыОснования?Кислоты

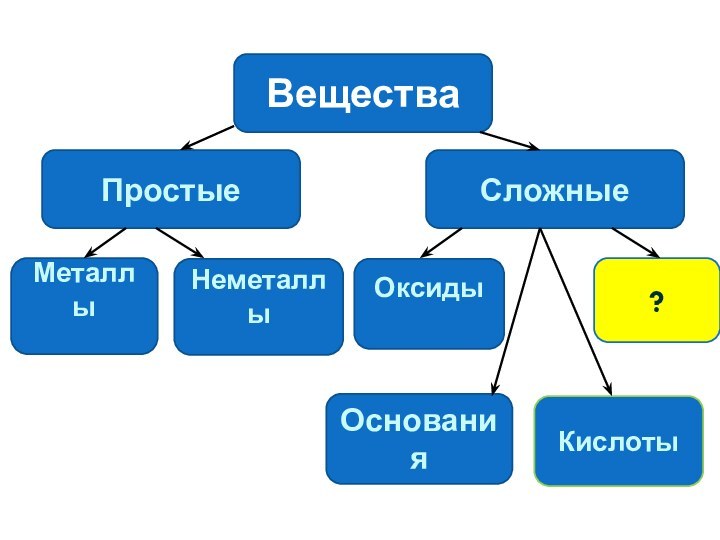














































Слайд 4
Задание1
На какие группы и по каким признакам можно
разделить вещества , формулы которых приведены ниже?
Na2O ;
H2CO3; ; H2SiO3 Ca(NO3)2 CaCO3 NaCl Cr2S3
NaOH ; О2; Al2O3 ; Ca (OH)2 ; С
СаO ; Аl; N2 ; Al(OH)3 ; S ; СО2 ;
H2SO3 ; SO2 ; Ca; Na
формулы запишите в схему:
Слайд 5
Вещества
Простые
Сложные
Металлы
Аl, Ca, Na
Неметаллы
S, С
,
N2, , О2
Оксиды
Na2O, Al2O3,
СаO, СО2, SO2
Основания
Ca
(OH)2 , NaOH, Al(OH)3Ca(NO3)2 CaCO3 NaCl Cr2S3 ?
Кислоты
H2CO3;, H2SiO3 , H2SO3
Слайд 6
Задание 2
Вставьте пропущенный фрагмент.
S------ SО2 ----- H2SO3
Na----Х-----
NaОН
С------- Х ---- H2CO3
Ca----- CaO
----- Ca (OH)2 Х
ХХ
CaCO3
Слайд 7
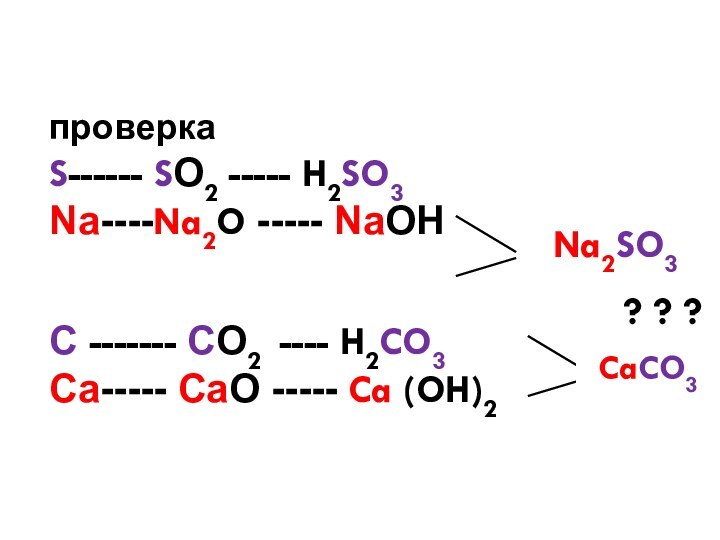
проверка
S------ SО2 ----- H2SO3
Na----Na2O ----- NaОН
? ? ?
С ------- СО2 ---- H2CO3
Ca----- CaO ----- Ca (OH)2
Na2SO3
CaCO3
Слайд 12
Задание.
Определить : почему у солей разное количество
кислотных остатков Дайте обоснованный ответ.
NaNO3
Ca (NO3 )2 Al (NO3 )3
Слайд 14
задание 4.
Определить : почему у солей разное
количество ионов металла? Дайте обоснованный ответ.
NaNO3
Na 2СО3 Na 3 РО4
Слайд 15
Так как кислотные остатки имеют свою степень окисления:
(см.
таблицу растворимости)
NO2-1- нитрит
NO3-1 - нитрат
SO3-2- сульфит
SO4-2 - сульфат
СO3-2-карбонат
Р-O4-3 - фосфат
Cl-1 - хлорид
SiO3-2 -силикат
Слайд 18
Алгоритм названия солей
Fe+2(NO3-1)2 – нитрат железа (II)
Fe +3(NO3-1)3
– нитрат железа (III)
=
+
+
Назовите соль:
ZnSO4-2
AlCl 3
Cu (NO3-1)2
Слайд 20
задание 5. НАЗОВИТЕ СОЛИ
NaCl - хлорид натрия
Fe
+2SO4 - сульфат железа (II)
Al3(PO4)3 – фосфат алюминия
Ca(NO3)2 -
нитрат кальция Cu+2CO3 – карбонат меди (II)
Cr2+3S3 – сульфид хрома (III)
Na2SO4 – сульфат натрия
Ba(NO3 )2 - нитрат бария
Слайд 23 1. Запиши рядом знаки химических элементов, которые входят
в состав вещества.
Алгоритм составления формул солей: Составить химическую формулу
сульфата железа (III ) (первый способ)
Fe
SO4
Соли - это сложные вещества, которые состоят из ионов металла и кислотного остатка
Первый пункт выполнили переходим ко второму
Слайд 24 2. Над знаками химических элементов поставь их степень
окисления.
Пример:
Fe
SO4
+3
-2
Второй пункт выполнили переходим к третьему
Слайд 25 3. Определи Н.О.К. чисел выражающих степень окисления этих
элементов.
Запиши Н.О.К. в квадратике над формулой.
Пример: Составить химическую
формулу сульфата железа (III).Fe
SO4
+3
-2
6
Третий пункт выполнили переходим ко четвертому
Н.О.К. (наименьшее общее кратное) – это число, которое делится на исходные числа без остатка.
Слайд 26 4. Раздели Н.О.К. на степень окисления каждого элемента. Запиши
полученный индекс.
Пример: Составить химическую формулу сульфата железа (III )..
Fe
(SO4)
+3
-2
2
3
6
2
3
Формула
составлена6
6
3
2
:
:
=
=
Слайд 27
Составить формулу сульфата алюминия:
(второй способ)
Составить формулы: нитрат железа
(III), сульфат натрия, карбонат меди (II), фосфат бария, силикат
калия.Al
2
+
SO
4
3
( )
3
2
Слайд 28
Составьте формулу
хлорида кальция
СаCl2
Составьте формулу
нитрата натрия
NaNO3
Zn(SO4)2
Cu NO3
Составьте
формулу
сульфата цинка
Составьте формулу
хлорида свинца (II)
Составьте формулу
нитрата меди
(I) PbCl2
Контрольное задание 2
Слайд 31 "Среди всех природных минеральных солей, самая главная та,
которую мы называем просто “соль”
А.Е.Ферсман
Слайд 33
Соль в геральдике российских городов
Герб Соликамска
Герб Солигалича
Герб Сольвычегодска
Герб Соль-Илецка
Герб Усолья-Сибирского
Герб Дрогобыча
Слайд 41
Минералы карбоната кальция находятся в горных породах:
Известняк
Мел
Мрамор
Мрамор Мрамор
Мрамор
Травертин
Слайд 42
Мрамор – строительный материал
Единственное в России здание, полностью
построенное из
нешлифованного мрамора — железнодорожный вокзал в городе Слюдянка
Иркутской области
Слайд 48
Контрольное задание - итоговое
Часть А (задания с
выбором ответа)
1. Соли – это сложные вещества:
А) состоящие из
ионов металлов и связанных с ними одного или нескольких гидроксид- ионов.Б) состоящие из ионов металлов и кислотных остатков;
В) состоящие из двух химических элементов, один из которых – кислород со степенью окисления -2;
Г) молекулы, которых состоят из ионов водорода и кислотных остатков.
2. Хлорид железа (III) имеет формулу:
А) FeCl3; B) Fe2O3;
Б) FeCl2; Г) FeO.
Слайд 49
Контрольное задание - итоговое
Часть В
Выбери лишнее
вещество и объясни почему?
Игра « Третий лишний»
1.
BaSO4; CaCO3; NaCl. 2. NaCl, Na2SO4, NaOH 3Al2(SO4)3, H2SO4, CaSO4
4. Cu(NO3)2, CuO, CuCl2
5. CaCl2, PbS, BaSO4.
Слайд 50
Контрольное задание - итоговое
Часть А
Г
А
Часть В
объясни почему?
1. NaCl. т.к…
2. NaOH
т.к... 3 H2SO4, т.к…4. CuO, т.к…
5. CaCl2 т.к…





























