Слайд 3
Цефалоспорины (англ. cephalosporins) — это класс β-лактамных антибиотиков,
в основе химической структуры которых лежит 7-аминоцефалоспорановая кислота (7-АЦК)
Основная
особенность
большая резистентность по отношению к β-лактамазам — ферментам, вырабатываемым микроорганизмами.
Слайд 4
Цефалоспорины проявляют бактерицидное действие.
Механизм действия:
повреждение клеточной мембраны бактерий
высвобождение
аутолитических ферментов, что приводит к их гибели.
Слайд 5
История открытия
Цефалоспорины были впервые выделены из культур Cephalosporium
acremonium в 1948 году итальянским ученым Джузеппе Бротзу который
заметил, что культуры продуцировали вещества, эффективно уничтожавшие Salmonella typhi, возбудителя тифа, которая имела активный фермент бета-лактамазу.
Слайд 6
С 1955 по 1962 г. детально изучались культуры
С.acremonium рабочими группами H.Florey и
E.P.Abraham.
Из продуктов обмена веществ
этого гриба удалось выделить
бактерицидную субстанцию - цефалоспорин С, ставшую исходным веществом для
получения 7-аминоцефалоспорановой кислоты - структурной основы
цефалоспоринов.
Слайд 7
В 1962 г. в клиническую практику был введен
первый антибиотик класса
цефалоспоринов - цефалоридин
Слайд 9
Сравнительная характеристика
антимикробной активности
Слайд 10
Из желудочно-кишечного тракта всасывается только цефалексин (90 %
принятой дозы)
Остальные цефалоспорины сильно раздражают слизистые оболочки
В/м: максимальная
концентрация в плазме крови через 30…60 мин, у грудных детей — через 30 мин, иногда раньше.
Цефалоспорины 1-го и 2-го поколений мало проникают через гематоэнцефалический барьер.
Фармакокинетика
Слайд 11
Элиминируют в основном через почки
При повторном введении возможна
их кумуляция, что приводит к увеличению концентрации препарата в
плазме крови и в тканях и повышению его токсичности
Период полувыведения большинства цефалоспоринов колеблется в пределах 1-2 ч.
Слайд 12
Показания
Основным показанием для применения цефазолина в настоящее
время является периоперационная профилактика в хирургии. Он используется также
для лечения инфекций кожи и мягких тканей.
Слайд 13
Бактериальные инфекции верхних и нижних дыхательных путей, уха,
горла и носа, мочевыводящих путей, костей и суставов, органов
малого и брюшной полости, желчных путей и ЖКТ, сепсис, бактериальная септицемия, перитонит, менингит,
Слайд 14
Инфекции нижних отделов дыхательных и мочевыводящих путей; почек;
инфекциях уха, носа, горла ( за исключением энтерококковых); при
септицемии; эндокардите; инфекциях костей и мягких тканей, брюшной полости; при гинекологических инфекционных заболеваниях бактериальный менингит (за исключением листериозного)
Слайд 15
Сидоренко С.В., Козлов С.Н. Практическое руководство по антиинфекционной
химиотерапии: Группа цефалоспоринов. НИИАХ СГМА http://www.antibiotic.ru/ab/023-29.shtml
http://pulmonolog.com/drugs/tsefalosporiny
А.И.Синопальников, О.В.Фесенко (Каф. терапии
Военно-медицинского
факультета при Российской медицинской академии последипломного образования,
Москва). http://works.tarefer.ru/51/100321/index.html
Слайд 17
http://ru.wikipedia.org/wiki/Макролиды
Л.С. Страчунский, С.Н. Козлов. Руководство для врачей http://www.antibiotic.ru/books/mach/mac0111.shtml
Слайд 18
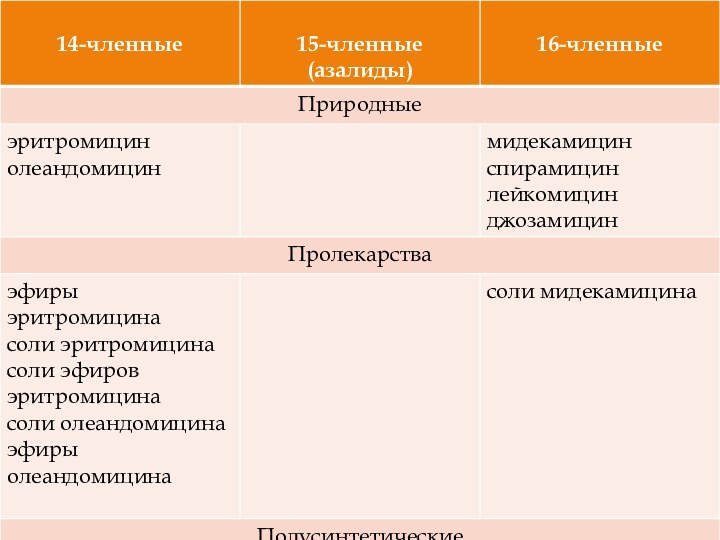
Макролиды — группа лекарственных средств, большей частью антибиотиков,
основой химической структуры которых является макроциклическое 14- или 16-членное
лактонное кольцо, к которому присоединены один или несколько углеводных остатков. Макролиды относятся к классу поликетидов, соединениям естественного происхождения.
Слайд 19
Также к макролидам относят:
азалиды, представляющие собой 15-членную макроциклическую
структуру, получаемую путем включения атома азота в 14-членное лактонное
кольцо между 9 и 10 атомами углерода;
кетолиды — 14-членные макролиды, у которых к лактонному кольцу при 3 атоме углерода присоединена кетогруппа.
Слайд 20
Первый из макролидов — эритромицин — был получен
в 1952 году из почвенного актиномицета Streptomyces erythreus и
использовался для лечения инфекций, вызванных грамположительными бактериями как альтернативный препарат у пациентов с аллергией на пенициллины.
Расширение сферы применения макролидов произошло в 70—80-х годах
Слайд 22
Общие свойства
Преимущественно бактериостатическое действие.
Активность против грамположительных кокков (стрептококки,
стафилококки) и внутриклеточных возбудителей (микоплазмы, хламидии, легионеллы).
Высокие концентрации в
тканях (в 5-10-100 раз выше плазменных).
Слайд 23
Низкая токсичность.
Отсутствие перекрестной аллергии с β-лактамами.
У 14-членных макролидов
взаимодействие с теофиллином, карбамазепином,
циклоспорином, цизапридом и др.
Слайд 24
ЭРИТРОМИЦИН
Первый природный макролид. Один из самых безопасных антибиотиков.
Слайд 25
Фармакокинетика
Всасывается в ЖКТ не полностью.
Биодоступность варьирует от 30
до 65%, причем значительно снижается в присутствии пищи.
Хорошо
проникает в бронхиальный секрет, желчь.
Плохо проходит через ГЭБ, ГОБ.
Выводится преимущественно через ЖКТ.
Т1/2 - 1,5-2,5 ч.
Слайд 26
Показания
Стрептококковые инфекции (БГСА)
Внебольничная пневмония.
Дифтерия.
Коклюш.
Ородентальные инфекции
Кампилобактериоз
Инфекции кожи и мягких
тканей.
Хламидийная инфекция.
Микоплазменная инфекция.
Легионеллез.
Слайд 27
РОКСИТРОМИЦИН
Полусинтетический 14-членный макролид. По спектру активности близок к
эритромицину.
Слайд 28
Отличия от эритромицина:
более стабильная биодоступность (50%), практически не
зависящая от пищи;
более высокие концентрации в крови и тканях;
более
длительный Т1/2 - 10-12 ч;
лучшая переносимость;
менее вероятны лекарственные взаимодействия.
Слайд 29
КЛАРИТРОМИЦИН
Отличия от эритромицина:
повышена активность против H.influenzae;
самый активный из
всех макролидов в отношении H.pylori;
Слайд 30
действует на атипичные микобактерии (M.avium и др.), вызывающие
оппортунистические инфекции при СПИДе;
большая кислотоустойчивость и биодоступность (50-55%), не
зависящая от еды;
более высокие концентрации в тканях;
более длительный Т1/2 (3-7 ч);
лучшая переносимость;
Слайд 32
http://slovari.yandex.ru/нитрофураны/БСЭ/Нитрофураны/
Слайд 33
Нитрофураны - производные фурана, в котором атом водорода
замещен нитрогруппой.
обладают широким спектром антимикробного действия
тормозят дыхание микробной
клетки.
Слайд 34
В хирургии нитрофураны применяют при лечении ран и
для профилактики послеоперационных осложнений (фурацилин);
в акушерстве, гинекологии и
урологии — при лечении инфекционных заболеваний (фурадонин, фуразолидон);
применяют также для лечения лямблиоза и трихомоноза
Слайд 35
Механизм действия
нарушают процесс клеточного дыхания бактерий
ингибируют биосинтез нуклеиновых
кислот.
В зависимости от концентрации оказывают бактериостатический или бактерицидный
эффект.
К нитрофуранам редко развивается лекарственная резистентность микроорганизмов.
Слайд 36
Фармакокинетика
Внутрь: хорошо и быстро всасываются.
Быстро выводятся из организма
(период полувыведения в пределах 1 ч).
Нитрофурантоин и фуразидин накапливаются
в моче в высоких концентрациях, фуразолидон - только в количестве 5% принятой дозы (поскольку в значительной степени метаболизируется).
Слайд 37
Частично экскретируются с желчью и создают высокие концентрации
в просвете кишечника.
При почечной недостаточности выведение нитрофуранов значительно замедляется.
Слайд 38
Показания
Инфекции нижних отделов МВП: острый цистит, супрессивная терапия
хронических инфекций (нитрофурантоин, фуразидин).
Профилактика инфекционных осложнений при урологических операциях,
цистоскопии, катетеризации мочевого пузыря (нитрофурантоин, фуразидин).
Слайд 39
Кишечные инфекции: острая инфекционная диарея, энтероколит (нифуроксазид, нифурател).
Лямблиоз
(фуразолидон, нифурател).
Трихомониаз (нифурател, фуразолидон).
Местно - промывание ран и полостей
(фуразидин).
Слайд 40
Фуразолидон
Более активен в отношении энтеробактерий и некоторых простейших.
Низкие
концентрации в моче.
Применяется при лямблиозе.
Вызывает дисульфирамоподобную реакцию