два цикла имеют одну общую связь (два общих атома)
малые циклы (С3, С4);обычные циклы (С5-С7);
средние циклы (С8-С11);
макроциклы (С12 и больше)
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть


![Циклические углеводороды(цикланы) [5]фуллерен-С20[5,6]фуллерен-С60](/img/tmb/14/1380732/dfe2e14146a213cb32c1b8bcdcbeda19-720x.jpg)
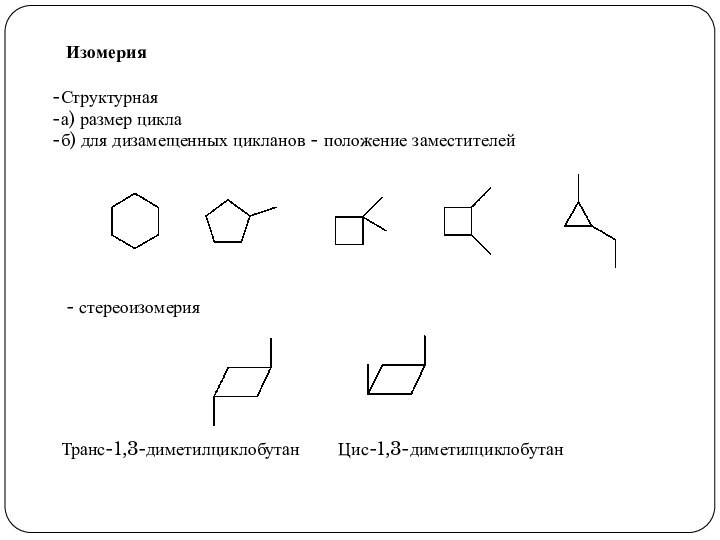

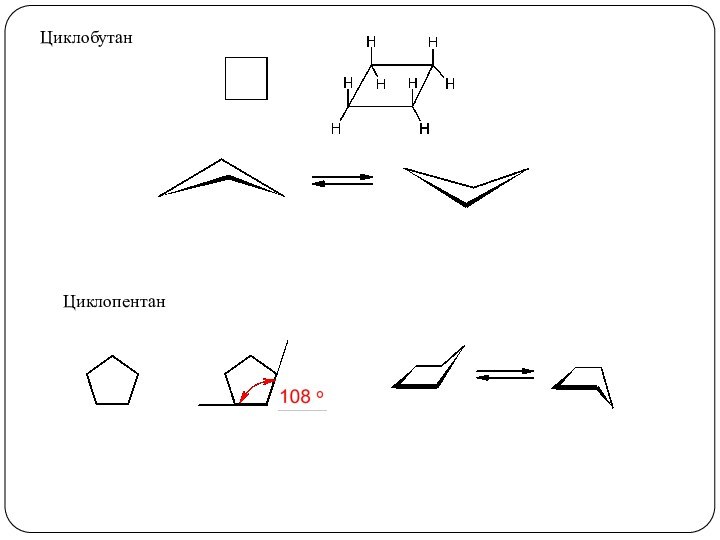
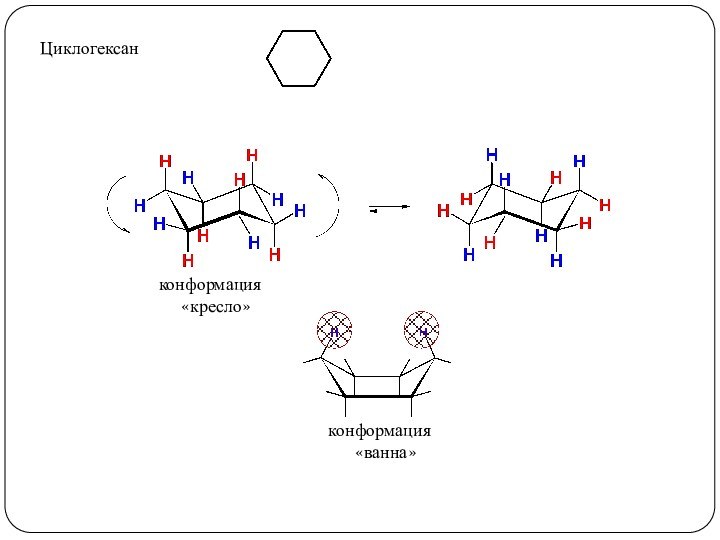
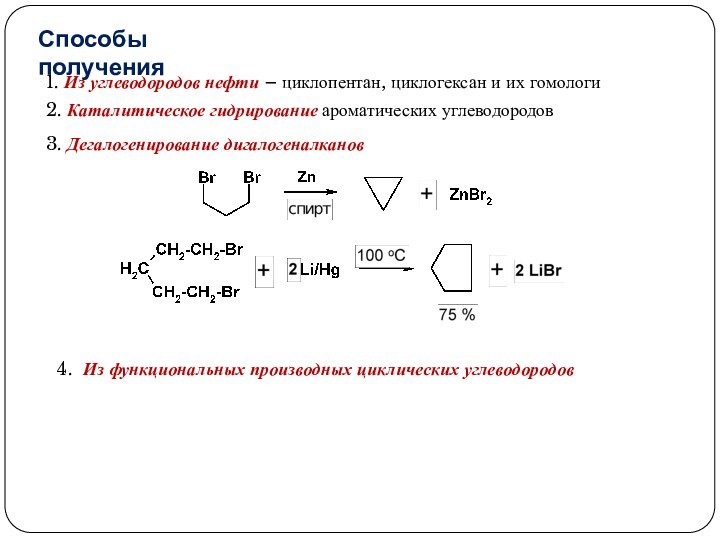
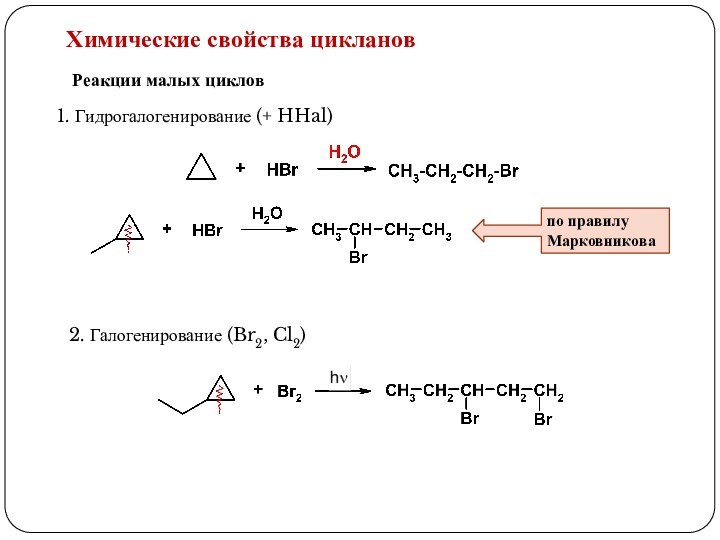
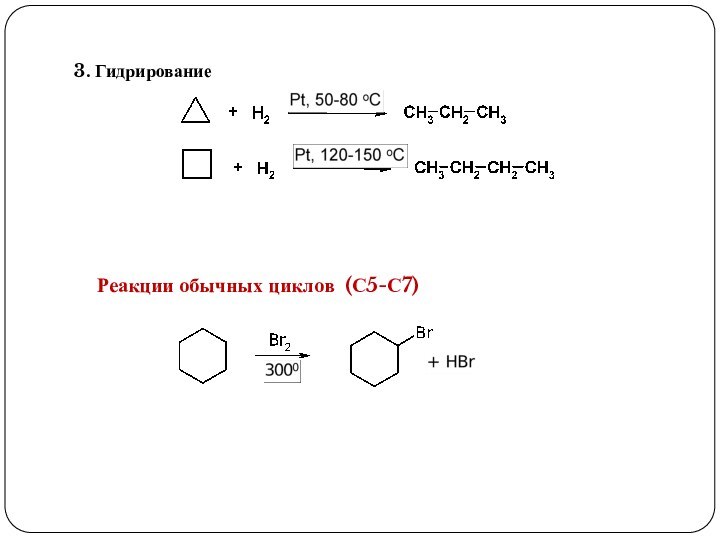
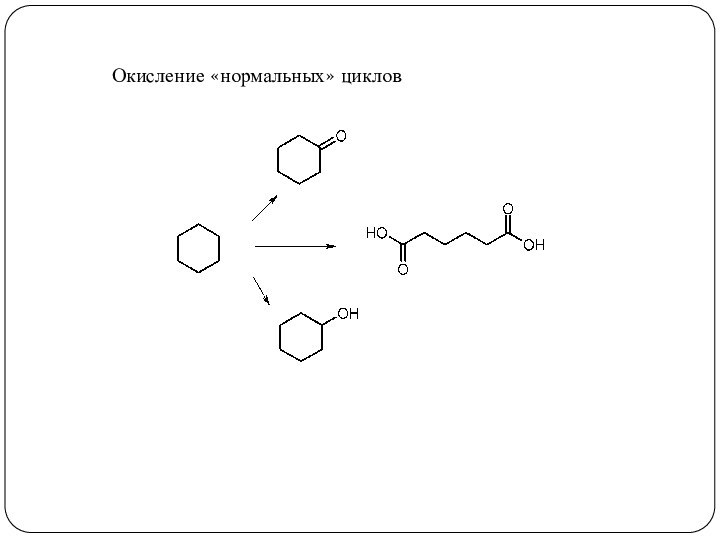

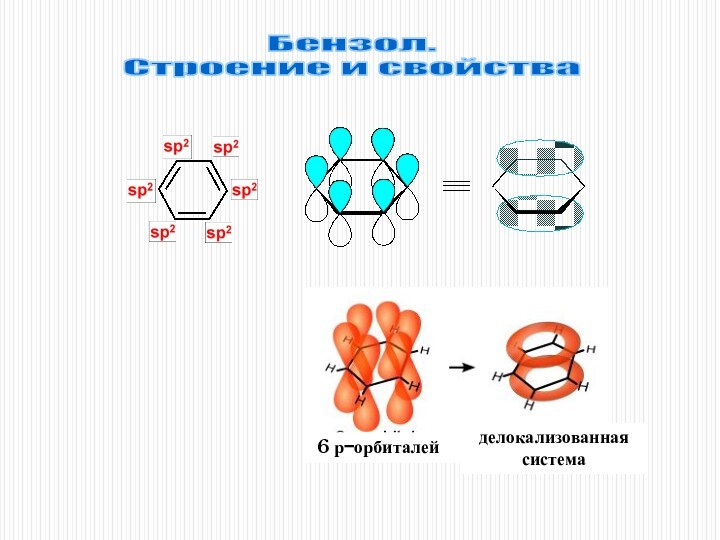

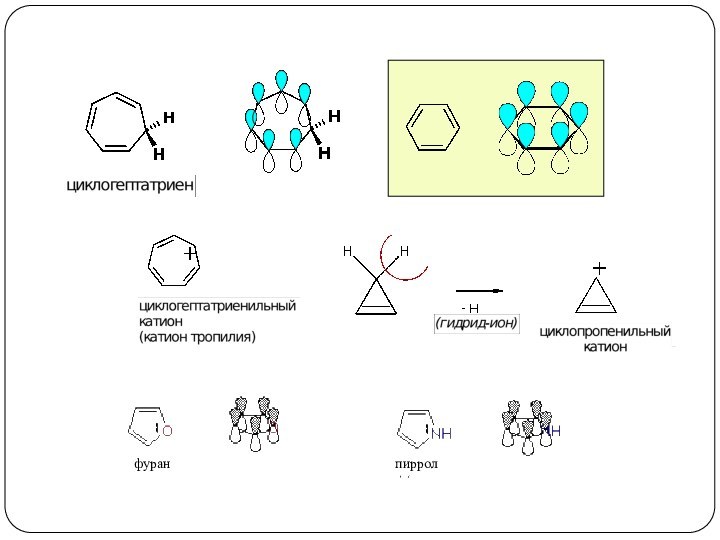
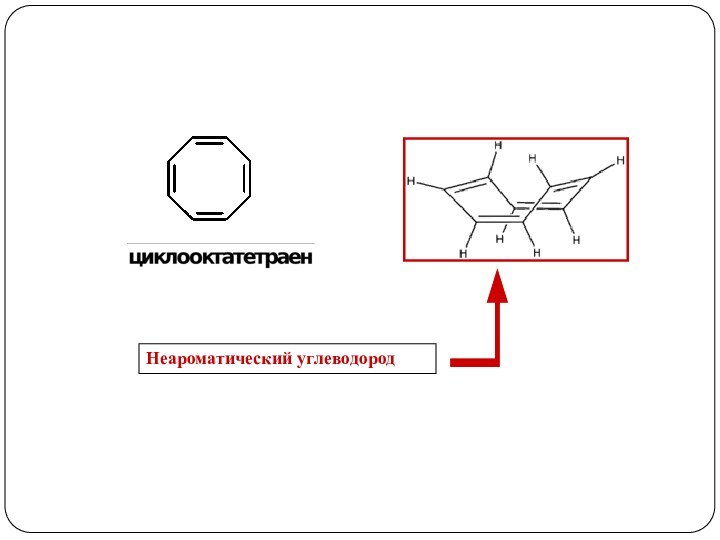



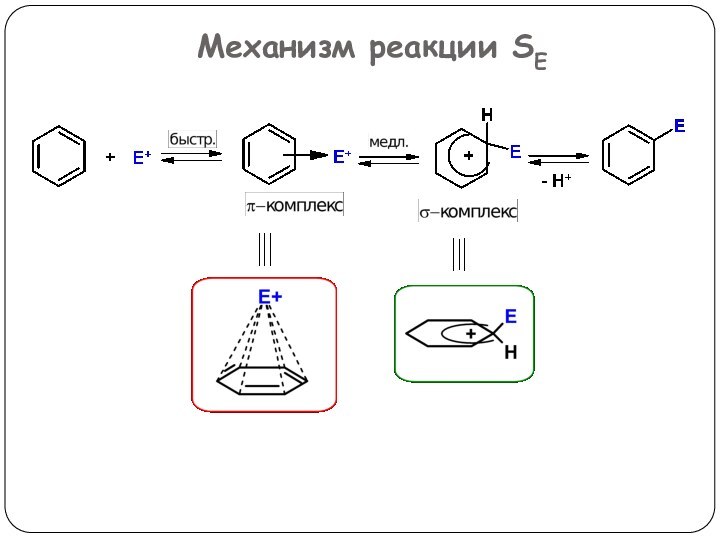

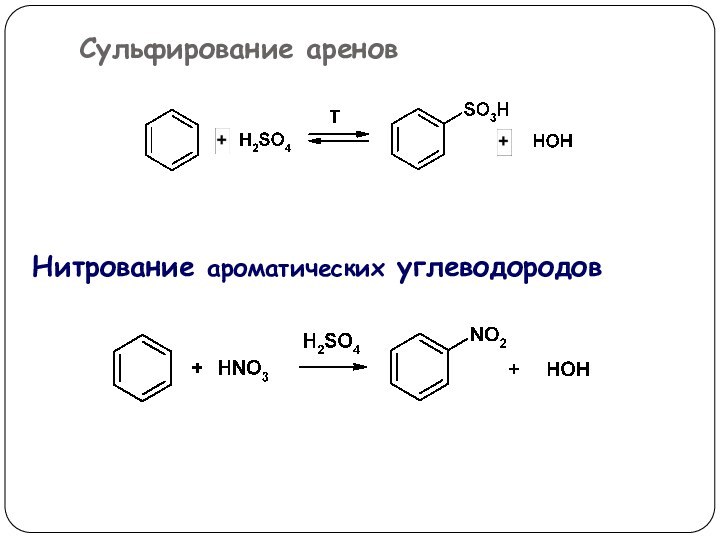
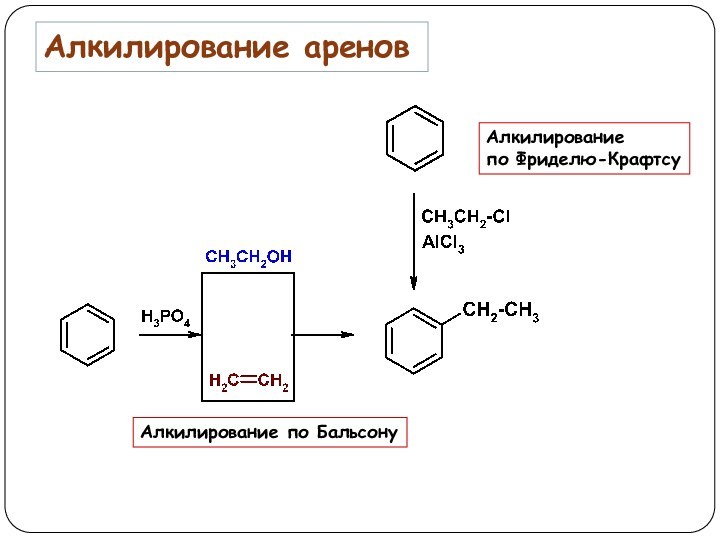
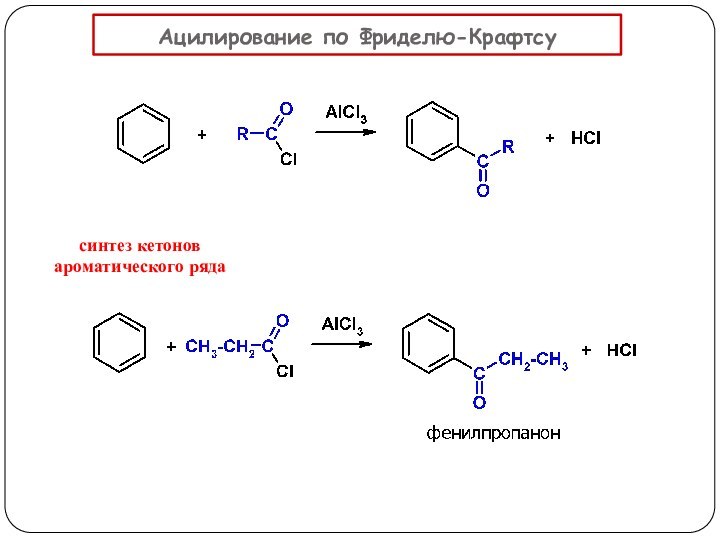




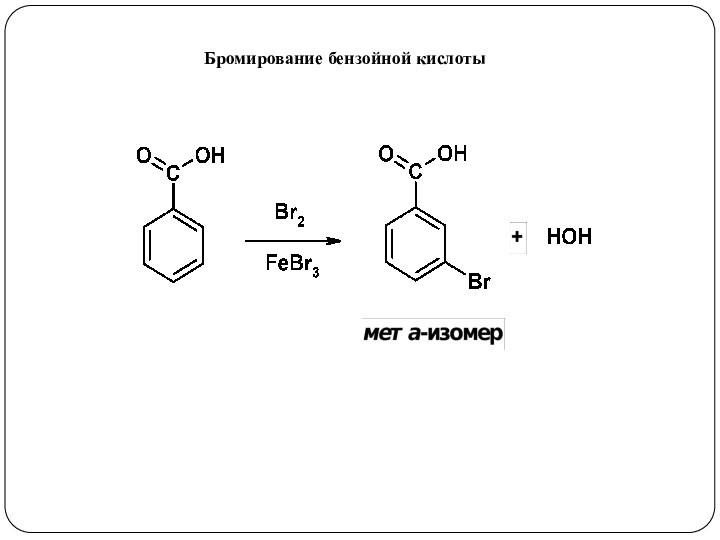


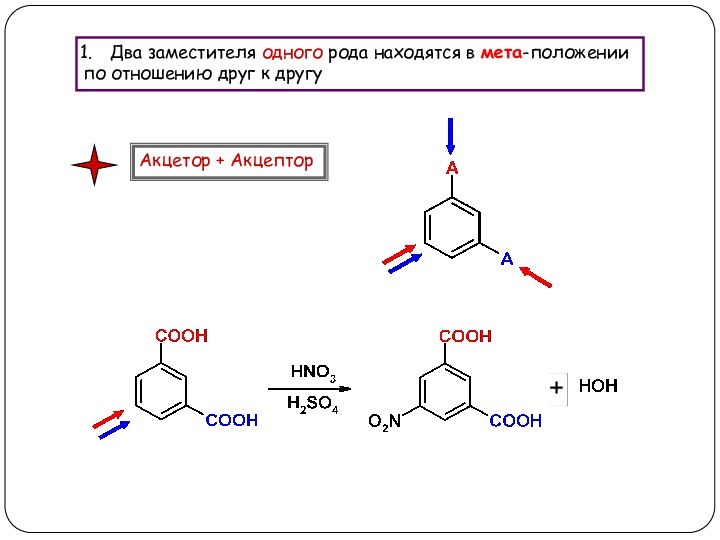

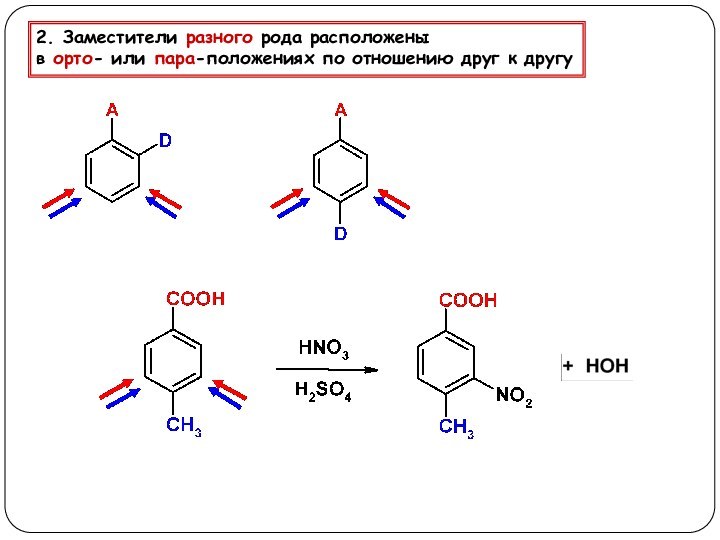
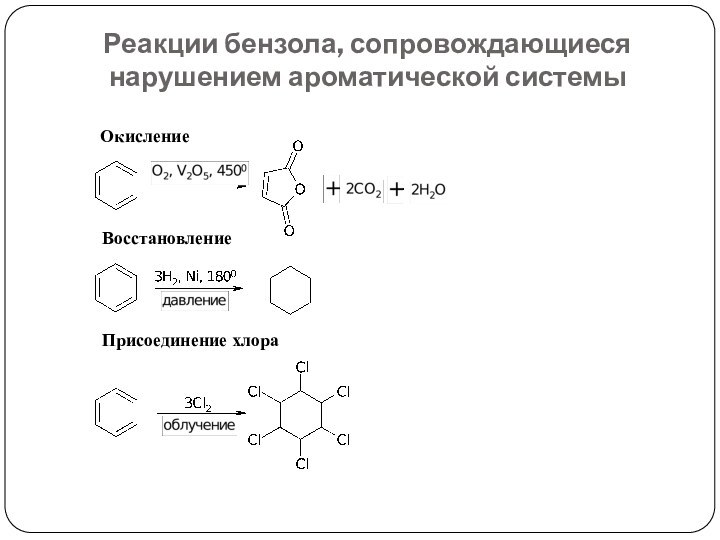
3. Реакции, приводящие к нарушению ароматической системы:
окисление;
восстановление;
галогенирование
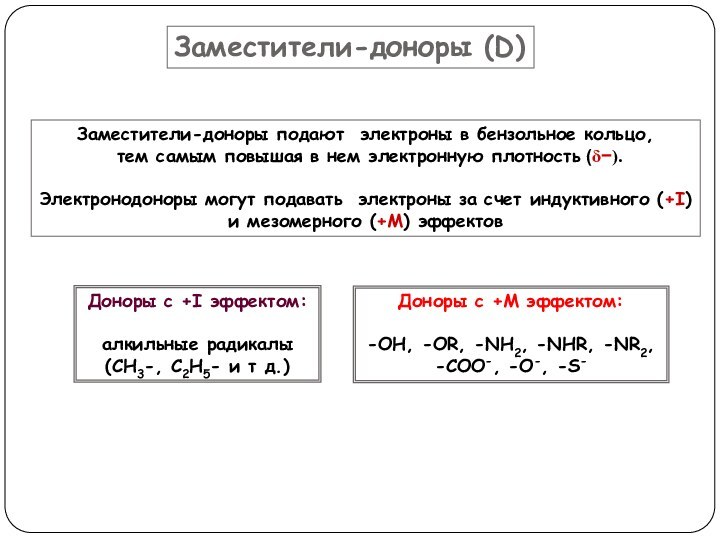
Доноры с +I эффектом:
алкильные радикалы
(CH3-, C2H5- и т д.)
Доноры с +М эффектом:
-OH, -OR, -NH2, -NHR, -NR2,
-COO-, -O-, -S-
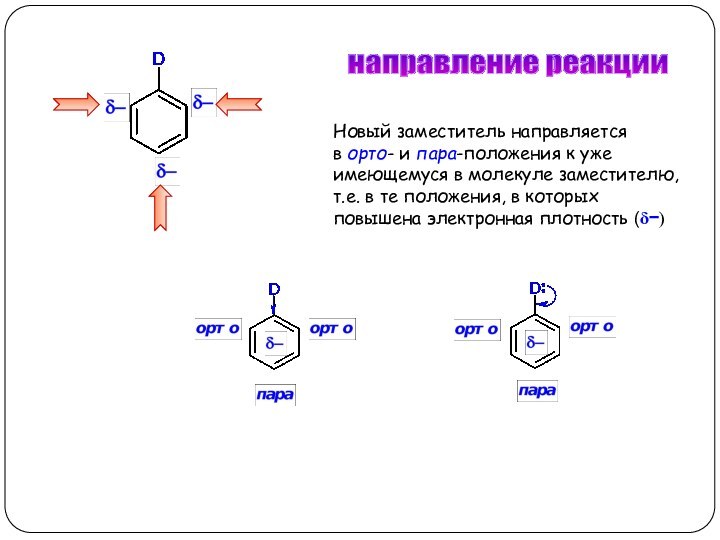
направление реакции
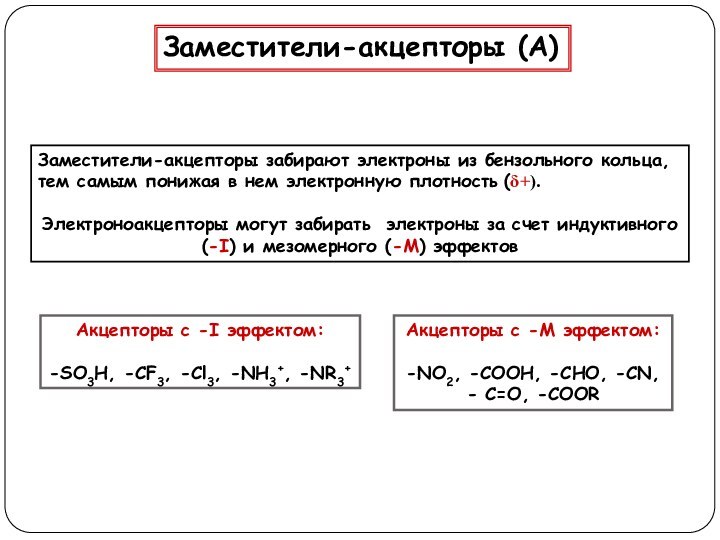
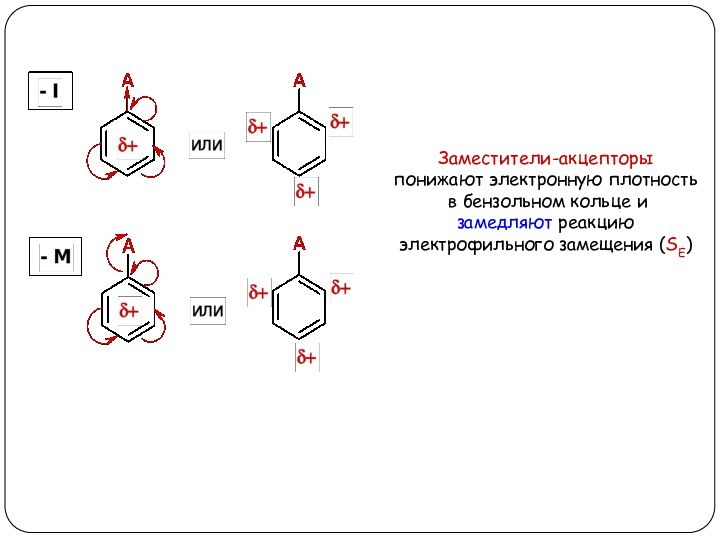
Акцепторы с -I эффектом:
-SO3H, -CF3, -Cl3, -NH3+, -NR3+
Акцепторы с -М эффектом:
-NO2, -COOH, -CHO, -CN,
- C=O, -COOR
направление реакции
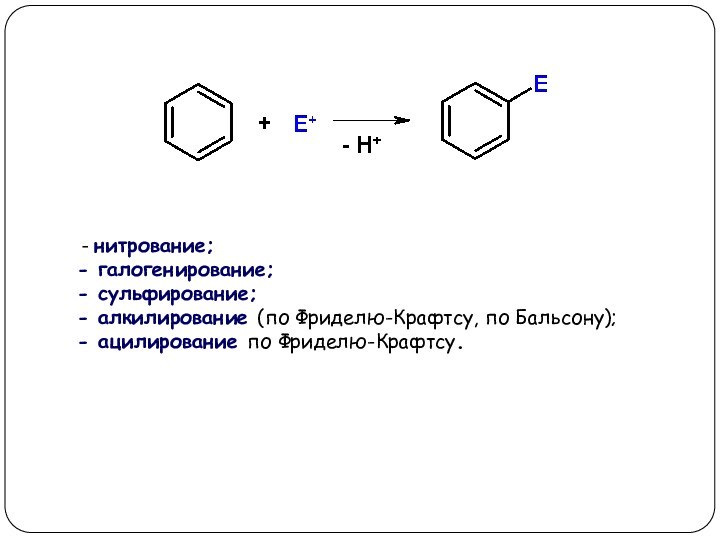
E+
E+
Относят к заместителям 1-го рода,
учитывая, что галогены затрудняют протекание реакции SE!