- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Судың кермектігі (9 класс)
Содержание
- 2. А) Са кальцийдін ПЖ-гі орны.Ә) Қандай кальций қосылыстарды білесіңдер?Б) Са физикалық қасиеттері?
- 3. А) Са атомының электрондық құрылысы? Ә)Табиғаттағы кальций қосылыстарының айналымы? В)Са химиялық қасиеттері?
- 4. Тест 1.Кальций атомының сыртқы энергетикалық деңгейінде неше электрон барА)1В)2С)3Д) 4
- 5. 2.Табиғатта ең көп таралған Са қосылысыА) фосфоритВ) құмС) гипсД) кальций карбонаты
- 6. 3)Кальцийдің қосылыстарындағы тотығу дәрежесіА)+1В)+2С)+3Д)+4
- 7. 4.СаО кальций оксидінің екінші атауыА)мәрмәрВ)гипсС)борД)сөндірілмеген әк
- 8. 5.Құрлыста қолданылатын кальций тұзыА) фосфоритВ) гипсС) апатитД) флюорит
- 9. Жауаптар: 1в; 2д; 3в; 4д; 5в;
- 10. Тапсырма: «Сәйкестік табу» Қосылыстар-------------------------------------Формуласы1Кальций гидроксиді-------------------А. СaCO₃2. Кальций
- 11. Жауаптар:1с; 2в; 3а; 4д; 5б; 6е;
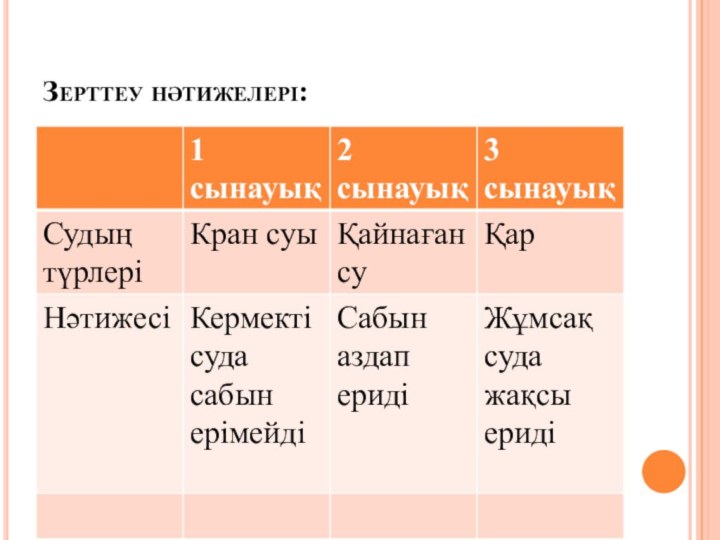
- 12. Зерттеу нәтижелері:
- 13. Табиғатта таза су кездеспейді: оның құрамында қандай
- 14. Кермек суТұрақтыУақытша
- 15. Суда Ca(HCО3)2 және Mg(HCO3)2 гидрокарбонаттары болғанда уақытша
- 16. Судың тұрақты кермектігі кальций мен магнийдің басқа
- 18. Скачать презентацию
- 19. Похожие презентации
А) Са кальцийдін ПЖ-гі орны.Ә) Қандай кальций қосылыстарды білесіңдер?Б) Са физикалық қасиеттері?
















Слайд 3 А) Са атомының электрондық құрылысы? Ә)Табиғаттағы кальций қосылыстарының
айналымы?
В)Са химиялық қасиеттері?
Слайд 10
Тапсырма: «Сәйкестік табу»
Қосылыстар-------------------------------------Формуласы
1Кальций гидроксиді-------------------А. СaCO₃
2. Кальций гипохлориді---------------Б. СаО
3.
Кальций карбонаты.-----------------В. Са(СІО)₂
4. Алебастер--------------------------------С. Са(ОН)₂
5. Кальций оксиді------------------------Д.СаSО₄ • 0,
5Н₂О 6. Ғаныш-------------------------------------Е. СаSО₄ • 2Н₂О