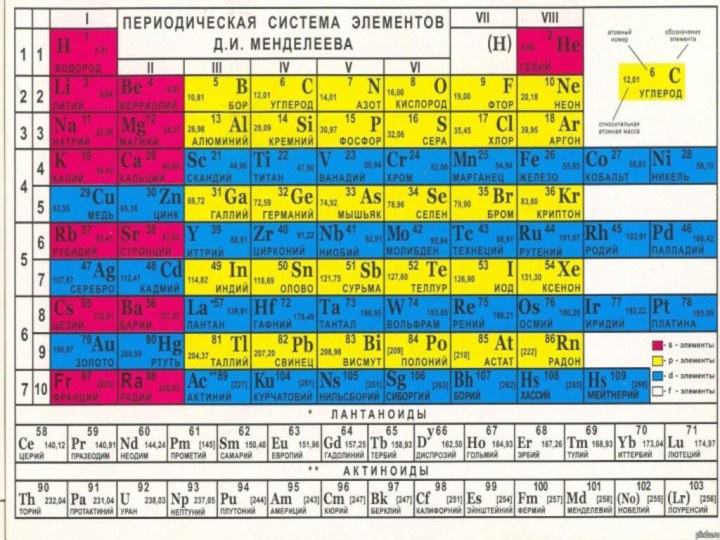
простого вещества (металл или неметалл; окислитель или восстановитель)
Низшая и
высшая степени окисленияСостав и свойства высших оксидов
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть





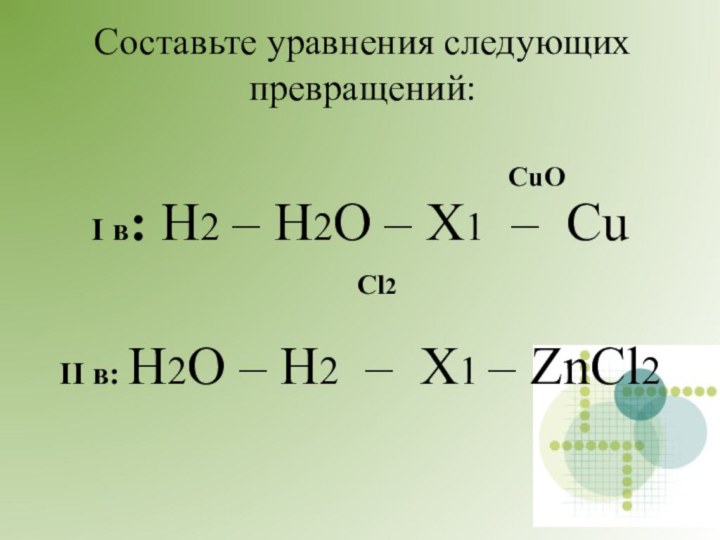






CuO
Cl2