- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии Классификация химических реакций, протекающих с изменением состава веществ
Содержание
- 2. По признаку изменения числа и состава веществ
- 3. Реакции соединения2С + О2 = 2СО2СО + О2 = 2СО2СО2 + Н2О = Н2СО3
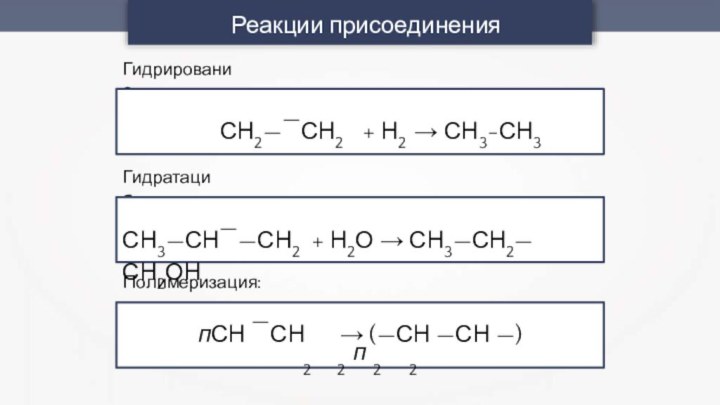
- 4. Реакции присоединенияГидрирование:Гидратация:Полимеризация:пСН —СН → (—СН —СН —)п2 2 2 2СН3—СН——СН2
- 5. Реакции разложенияHgO = Hg + O2Zn(OH)2 = ZnO + H2O2Cu(NO3)2 = 2CuO + 4NO2 + O2
- 6. Реакции замещенияK + H2O = KOH +
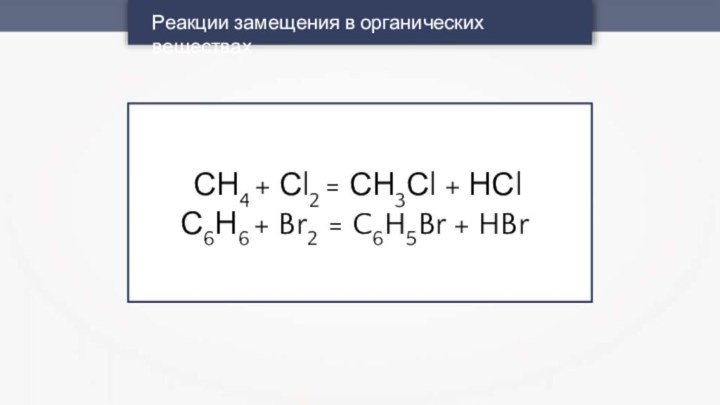
- 7. Реакции замещения в органических веществахСН4 + Сl2
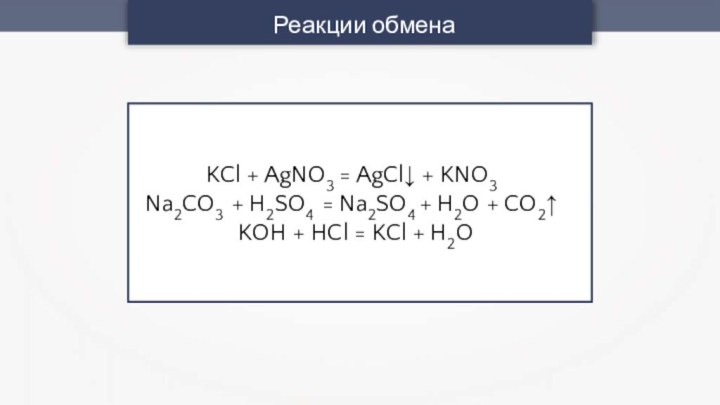
- 8. Реакции обменаKCl + AgNO3 = AgCl↓ +
- 9. По признаку выделения или поглощения теплоты среди химических реакций выделяют экзотермические и эндотермические реакции.
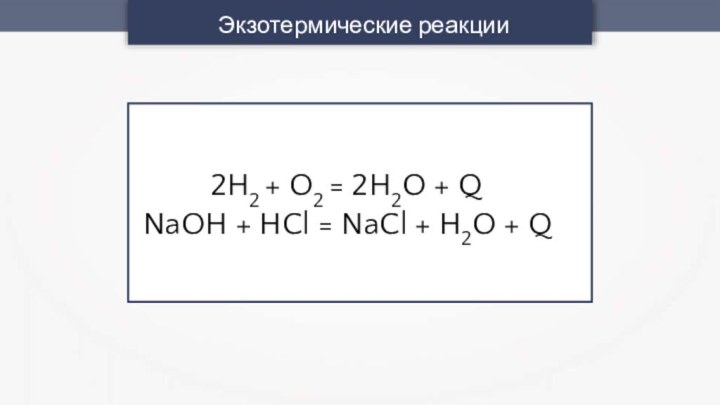
- 10. Экзотермические реакции2H2 + O2 = 2H2O +
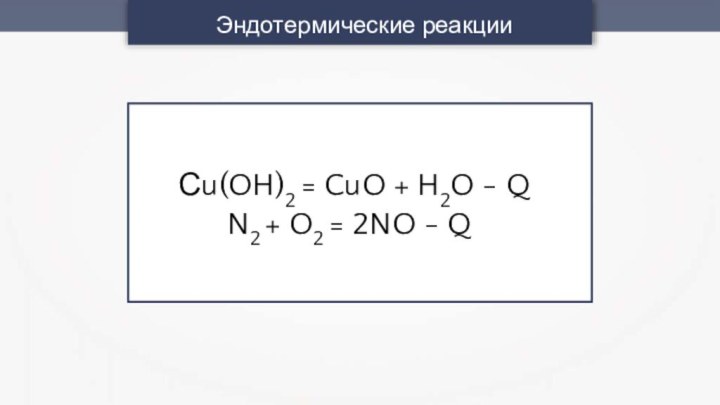
- 11. Эндотермические реакцииСu(OH)2 = CuO + H2O - Q N2 + O2 = 2NO - Q
- 12. Тепловой эффект — количество теплоты, которая выделяется или поглощается в ходе химической реакции.
- 13. Скачать презентацию
- 14. Похожие презентации
По признаку изменения числа и состава веществ среди химических реакций выделяют реакции соединения, разложения, замещения и обмена.