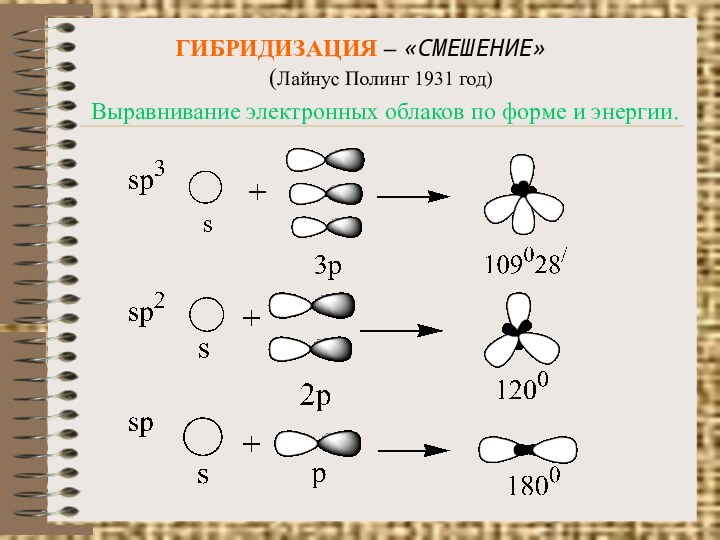
по форме и энергии.
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть

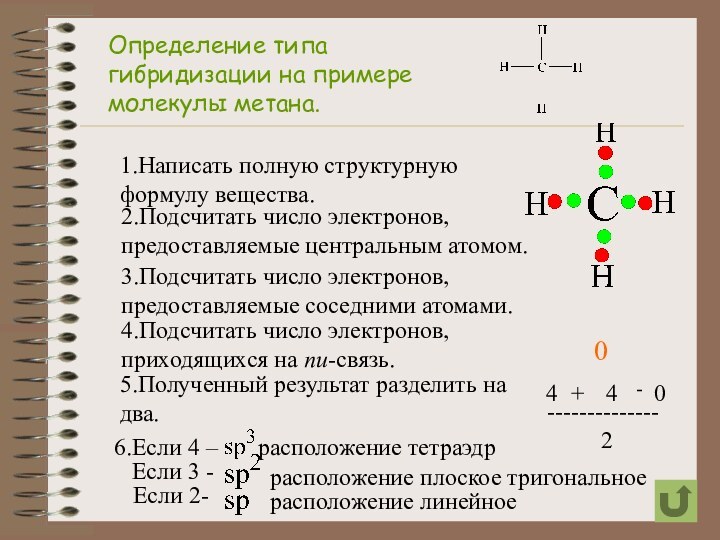
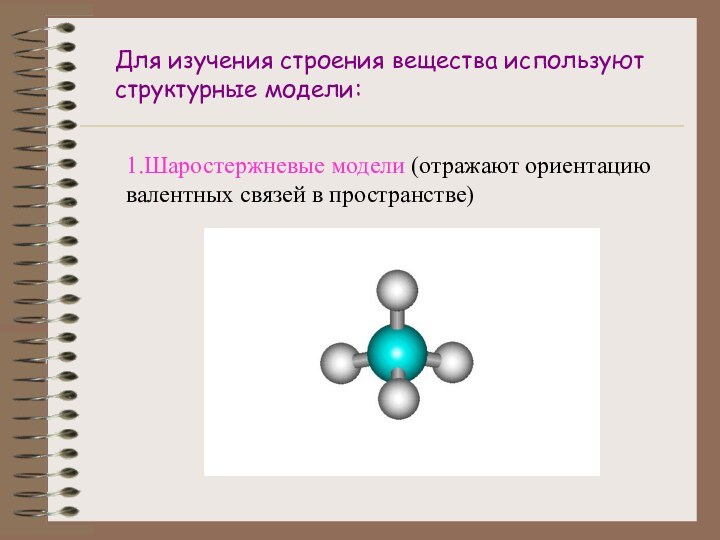

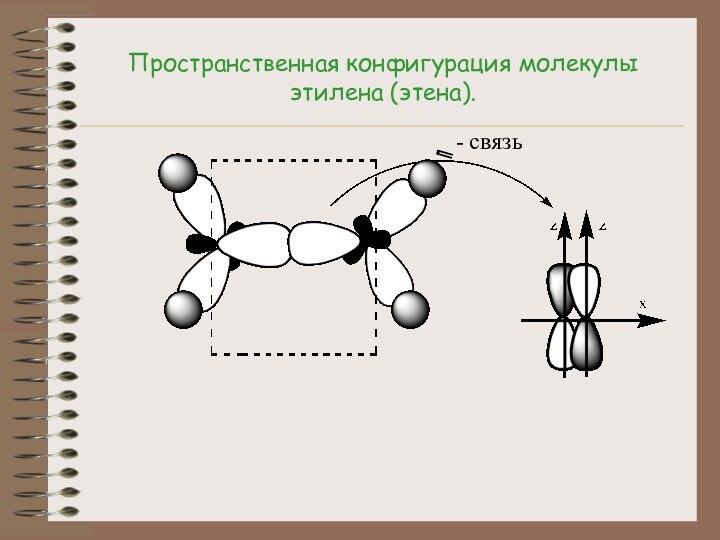
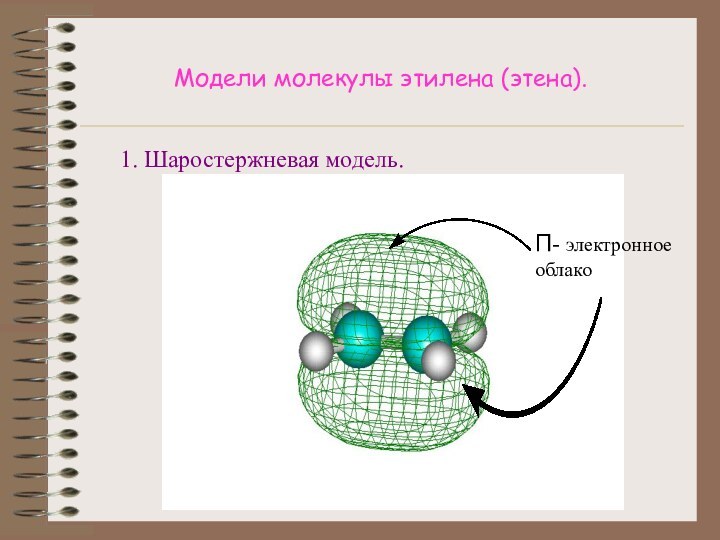
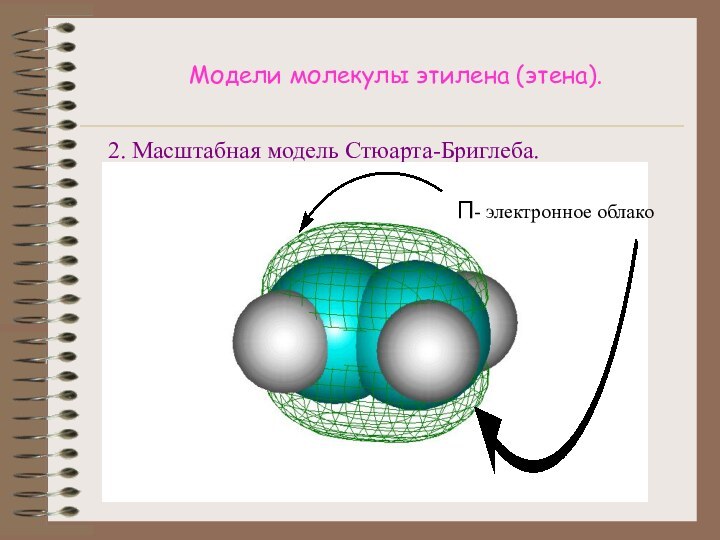
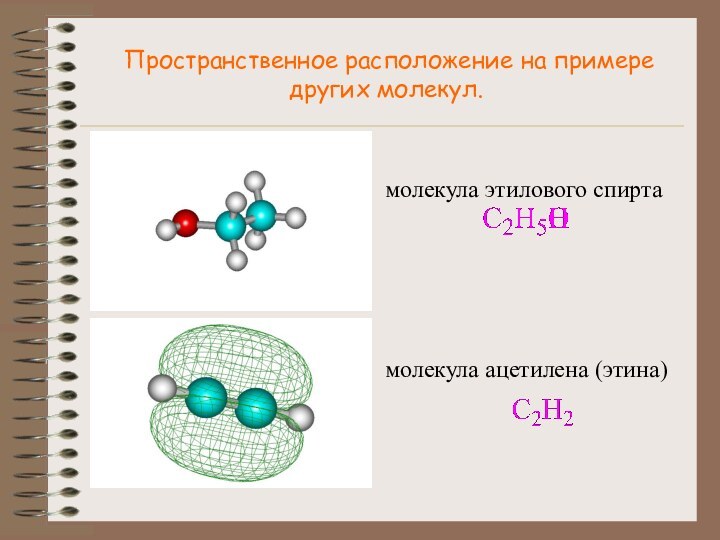
4.Подсчитать число электронов, приходящихся на пи-связь.
0
5.Полученный результат разделить на два.
4
+
4
-
0
--------------
2
6.Если 4 –
расположение тетраэдр
Если 3 -
расположение плоское тригональное
Если 2-
расположение линейное
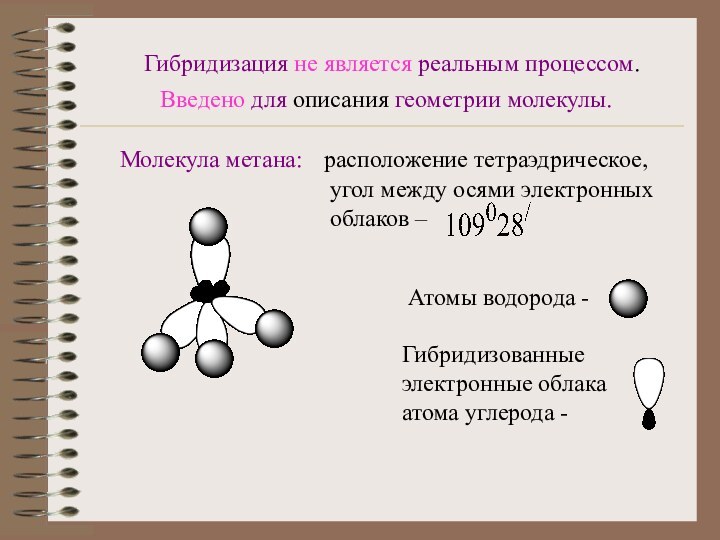
Гибридизованные электронные облака атома углерода -
1
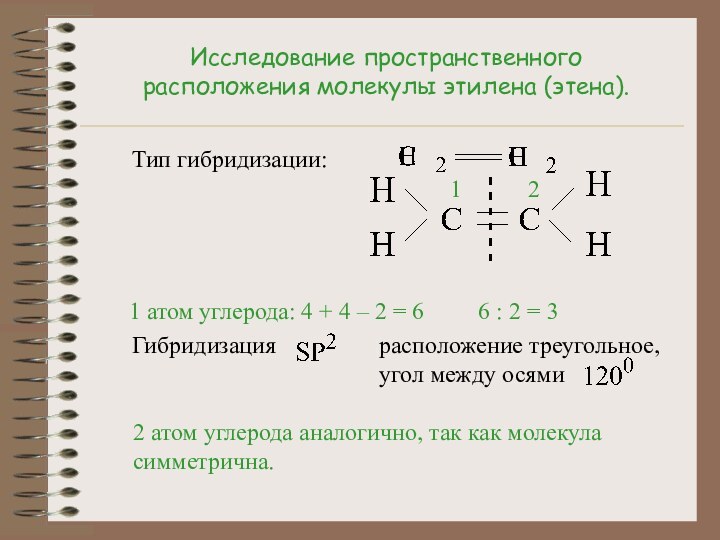
Гибридизация
расположение треугольное, угол между осями
2 атом углерода аналогично, так как молекула симметрична.
2