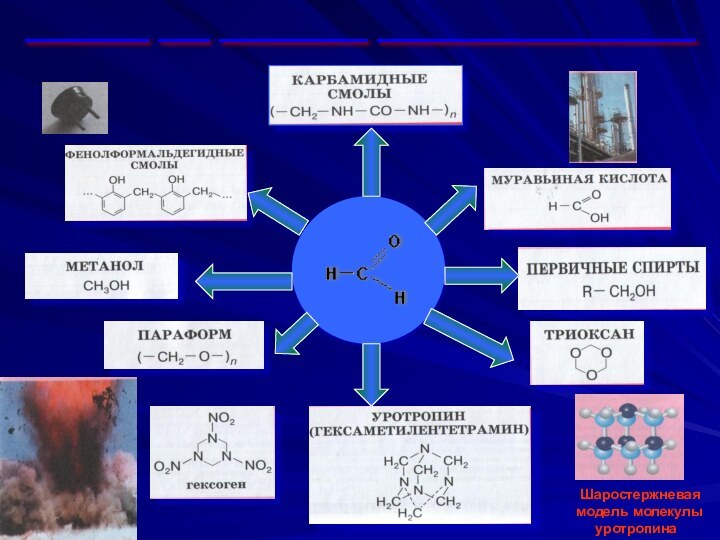
растворимость фенола в холодной и горячей воде?
Как по строению
отличаются фенолы от предельных спиртов?Что общего в химических свойствах предельных спиртов и фенолов?
Чем отличаются химические свойства фенола от свойств предельных спиртов?
Какие типы химических реакций характерны для фенола?
Составьте уравнения реакций:
а) замещения атома водорода в гидроксильной группе
б) замещения атомов водорода в бензольном кольце
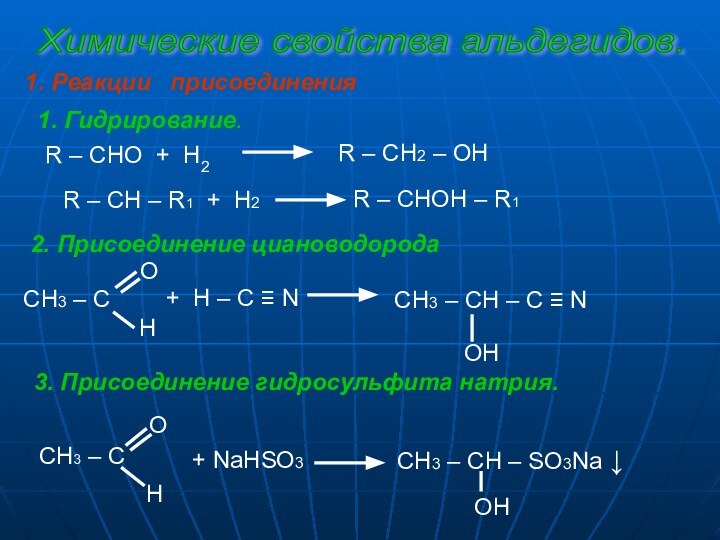
в) присоединения
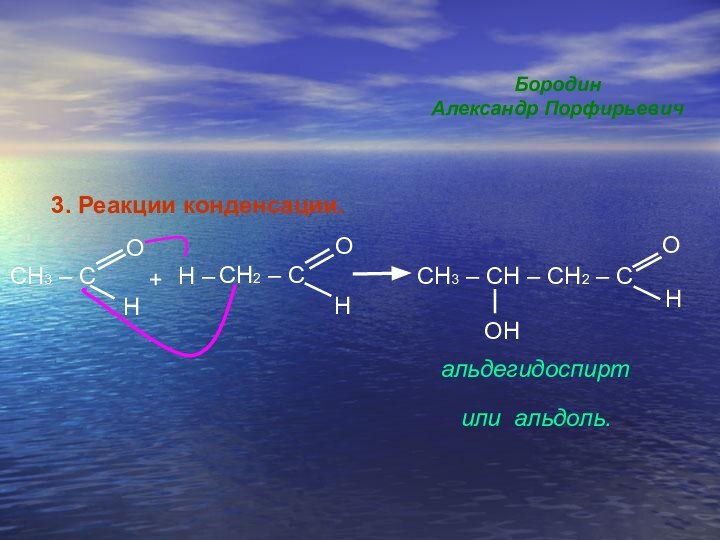
Назовите полученные соединения.
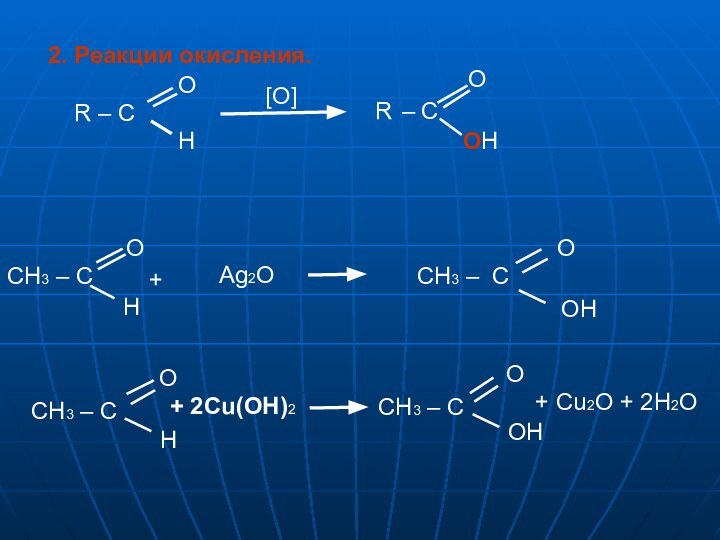
Какие качественные реакции на фенол вам известны?
Назовите основные области применения фенола.








![Альдегиды 10 класс РЕАГЕНТЫ Химические свойства альдегидов. (обобщение) РеакцииприсоединенияРеакцииокисленияРеакцииконденсациигидрированиеПрисоединениециановодородаПрисоединениеNaHSO3Реакция«серебряного зеркала»Окисление с помощью Сu(OH)2самоконденсацияполиконденсацияH2HCNNaHSO3[Ag(NH3)2]OHСu(OH)2С6H5OH](/img/tmb/12/1166493/ecd18f7f0124b2fc2dbd5d7ea39c5307-720x.jpg)