Слайд 3
В 1933г был осуществлен синтез аскорбиновой кислоты, который
подтвердил ее строение. В промышленности синтез аскорбиновой кислоты осуществляется
из D-глюкозы, которая в больших количествах получается при расщеплении крахмала серной кислотой.
ПОЛУЧЕНИЕ:
Слайд 4
Природные источники:
хвоя сосны;
плоды смородины;
плоды рябины;
плоды красного
перца;
плодах цитрусовых;
капуста;
салат;
томат;
картофель;
зелёный лук;
укроп;
петрушка.
Слайд 5
Лекарственное сырьё, содержащее витамин С:
плоды шиповника;
плоды чёрной
смородины;
листья первоцвета;
плоды грецкого ореха (незрелые).
«Витаминный чемпион» - плоды
шиповника.
Слайд 6
Описание:
Белый кристаллический порошок без запаха, кислого вкуса.
Легко
растворим в воде, медленно растворим в 90% спирте, практически
не растворим в эфире и хлороформе.
Проявляет одновременно восстановительные и кислотные свойства.
Восстановительные свойства обусловлены наличием ендиольной группировки
Кислотные свойства - за счет атома водорода гидроксильной группы при углероде в 3 положении.
Слайд 7
Аскорбиновая кислота легко окисляется до дегидроаскорбиновой кислоты (кетонная
форма), способной снова восстанавливаться до аскорбиновой кислоты.
Слайд 8
Аскорбиновая кислота не совместима с:
солями антибиотиков (бензилпенициллина
натриевая
и калиевая соль);
натриевыми солями производных барбитуровой
кислоты и
сульфаниламидных препаратов;
бензоатом натрия и салицилатом натрия.
Слайд 9
Образует отсыревающие и расплавляющиеся смеси с:
бутадионом;
дибазолом;
димедролом;
ацетилсалициловой кислотой;
никотиновой кислотой;
натрия
гидрокарбонатом;
натрия салицилатом;
пахикарпином;
эуфиллином.
с никотиновой кислотой – нарушается обмен кислоты;
с антикоагулянтами – ослабляется эффект антикоагулянтов.
Слайд 10
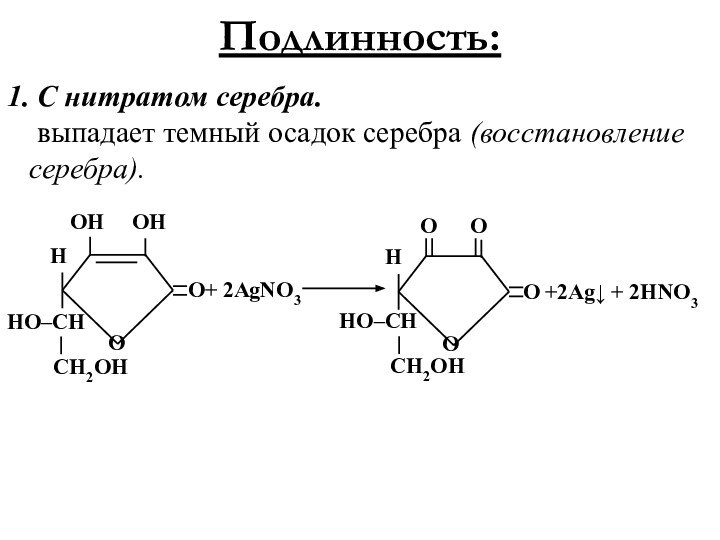
Подлинность:
1. С нитратом серебра.
выпадает темный осадок
серебра (восстановление
серебра).
О О
О
НО–СH
ОН ОН
Н
СН2ОН
О+ 2AgNO3
СН2ОН
НО–СН
О
Н
О
+2Ag↓ + 2HNO3
Слайд 11
2. С 2,6-дихлорфенолиндофенолятом натрия.
синяя окраска
реактива исчезает (восстановление в
бесцветное лейкооснование).
НО–СН
O
СН2ОН
+
Cl
O
Cl
N
ONa
НО–СН
HO
O
СН2ОН
+
Cl
Cl
N
ONa
H
Слайд 12
Чистота:
1. Удельное вращение от + 22 до плюс
24˚С
( 2% водный раствор);
2. Органические примеси,
тяжелые металлы в
пределе эталона;
3. Препарат должен выдерживать требования по
микробиологической чистоте для
нестерильных лекарственных средств.
Слайд 13
Количественное определение:
Йодатометрия (фармакопейный метод).
Метод основан на восстановительных
свойствах аскорбиновой кислоты
KJO3+ 5KI + 6HCl → 3I2 +
6KCl + 3H2O
Слайд 14
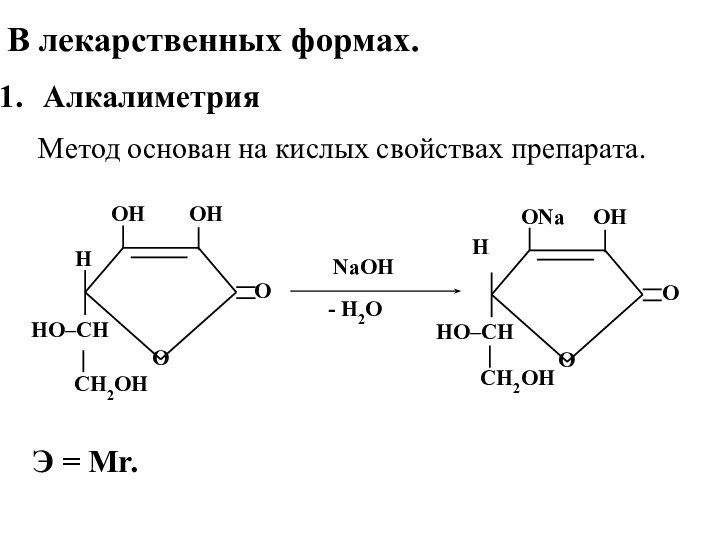
В лекарственных формах.
Алкалиметрия
Метод основан
на кислых свойствах препарата.
Э = Мr.
Слайд 15
2. Йодометрия.
Метод основан на восстановительных свойствах
О
НО–СH
ОН ОН
Н
СН2ОН
О
I2
- 2HI
О
НО–СH
О О
Н
СН2ОН
О
Э = Mr /2
Слайд 16
ГФ XI статья 38 рекомендует определять содержание аскорбиновой
кислоты в плодах шиповника путём титрования 0,001 моль/л раствором
2,6 – дихлорфенолиндофенолятом натрия. Аскорбиновой кислоты должно быть не менее 0,2%.
Слайд 17
Применение:
Суточная потребность аскорбиновой кислоты –
60-70мг.
Назначают:
с целью профилактики
и лечения инфекционных
заболеваний;
при интоксикациях;
кровотечениях различной этиологии.
Слайд 18
Хранение:
В сухом защищенном от света месте.
Срок годности
3 года.
Слайд 19
Аскорбиновая кислота может применяться в качестве антиоксиданта.
радиация;
загрязнённый воздух;
сигаретный дым;
алкоголь;
некоторые лекарственные препараты;
диета;
длительное пребывание на солнце.
могут способствовать
увеличенному образованию свободных радикалов в организме.
Слайд 20
Чрезмерные психические, физические нагрузки и стресс также влияют
на образование свободных радикалов.
Свободные радикалы оказывают пагубное влияние
на здоровье, в том случае, если в организме образуется избыточное количество свободных радикалов.
Собственные защитные системы организма не могут более поддерживать баланс свободных радикалов. Что приводит к поражению клетки.
Слайд 21
Аскорбиновая кислота:
понижает чувствительность кожи к солнечным
лучам;
участвует
в выведении из организма холестерина,
чем помогает в
борьбе с атеросклерозом.
Дефицит аскорбиновой кислоты предрасполагает к некоторым онкологическим заболеваниям.
Суточная доза витамина С – 200мг, по данным зарубежных авторов – 400мг, при воспалительных процессах можно увеличить до 500мг.
Слайд 22
Кислота глютаминовая (ФС 42 – 2722 – 96)
Acidum glutaminicum
2-аминоглутаровая кислота.
Слайд 23
Входит в состав белковых веществ:
казеин;
миозин.
Встречается
в
белке мозга;
в злаковых.
И получали ее при кислотном
гидролизе злаковых.
В настоящее время получают путём синтеза.
Слайд 24
Описание.
Белый кристаллический порошок, с едва ощутимым запахом.
Мало
растворим в холодной воде, растворим в горячей, практически не
растворим в спирте 95% и эфире.
Слайд 25
Подлинность:
1.С нингидрином образуется сине-фиолетовое окрашивание.
Слайд 27
2.Препарат смешивают с резорцином в присутствии концентрированной серной
кислоты, нагревают до появления зелено – коричневого окрашивания. После
охлаждения прибавляют воду и раствор аммиака, появляется красно-фиолетовое окрашивание с зеленой флюоресценцией.
Слайд 28
Чистота.
Удельное вращение. От + 30,5˚ до + 33,5˚;
Хлориды,
тяжелые металлы, мышьяк – недопустимые примеси.
рН водного раствора от
3,1 –3,7.
Определяют микробиологическую чистоту.
Слайд 29
Количественное определение.
1. Метод кислотно-основного титрования.
Основан на
кислой реакции среды (индикатор –
бромтимоловый синий
Э = Mr
T • V • K • 100
X% = ---------------------
А
N*Э
T= ----------
1000
Слайд 30
Применение.
Участвует в обмене азота, связывает аммиак.
Применяется:
при заболеваниях
центральной нервной
системы;
при психических расстройствах
(в виде 1% раствора внутрь в сочетании с
раствором глюкозы, реже внутривенно),
внутрь в виде таблеток, порошков.
Часто применяется в детской практике.
Слайд 31
Хранение.
В сухом, защищенном от света месте.
Срок годности
5 лет.
Слайд 32
Кислота аминокапроновая (ФС 42 – 2720 – 96)
Acidum
aminocapronicum
Описание:
Бесцветные кристаллы или белый кристаллический порошок без запаха. Легко
растворим в воде, очень мало растворим в 95% спирте, практически не растворим в хлороформе и эфире.
Слайд 34
Подлинность:
1.Водный раствор препарата
нейтрализуют раствором едкого натра (индикатор – фенолфталеин), прибавляют раствор
нингидрина и нагревают до кипения; появляется синее окрашивание.
2. К водному раствору прибавляют раствор фенолфталеина 0,1М раствор едкого натра до появления красного окрашивания. После прибавления раствор формалина, нейтрализованного по фенолфталеину (слаборозовое окрашивание), окраска исчезает.
Слайд 35
Чистота:
Раствор препарата должен быть прозрачным в течение 24
часов и бесцветным.
рН раствора от 7,5 до 8,0.
Определяют оптическую
плотность раствора.
Посторонние аминокислоты, определяют хроматографически – не должно быть белого пятна и белого цвета на уровне пятна капролактама.
Хлориды, железо, тяжелые металлы в пределе эталона.
Препарата должен выдерживать требования по микробиологической чистоте для не стерильных лекарственных средств.
Сульфатная зола не должна превышать 0,1%.
Слайд 36
Метод неводного титрования.
Точную навеску препарата растворяют в ледяной
уксусной кислоте, титруют 0,1 М раствором хлорной кислоты, индикатор
– кристаллический фиолетовый до перехода фиолетовой окраски в голубовато – зеленую.
Количественное определение:
Слайд 37
2. Алкалиметрия (аптечный метод).
Точную
навеску препарата растворяют в воде, прибавляют тимолфталеин, ацетон.
Титруют
0,1н раствором едкого натра до синего окрашивания.
O
H2N – CH2 – CH2 – CH2 - CH2 – CH2 – C + NaOH
OH
O
H2N – CH2 – CH2 – CH2 - CH2 – CH2 – C + H2O
ONa
Э= Mr
N*Э
T= ----------
1000
T • V • K • 100
X% = ---------------------
А
Слайд 38
Фибринолитическое средство.
Применяют для остановки кровотечения при хирургических
и различных патологических состояниях, внутривенно и внутрь, 5% раствор
на изотоническом растворе натрия хлорида.
Применение: