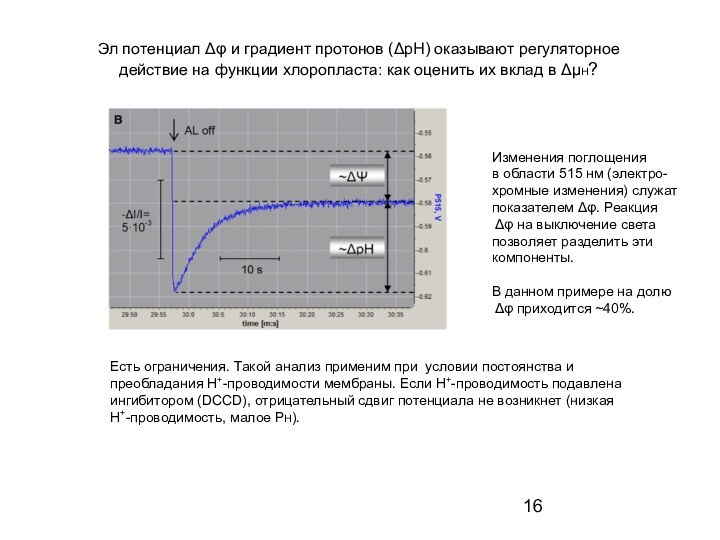
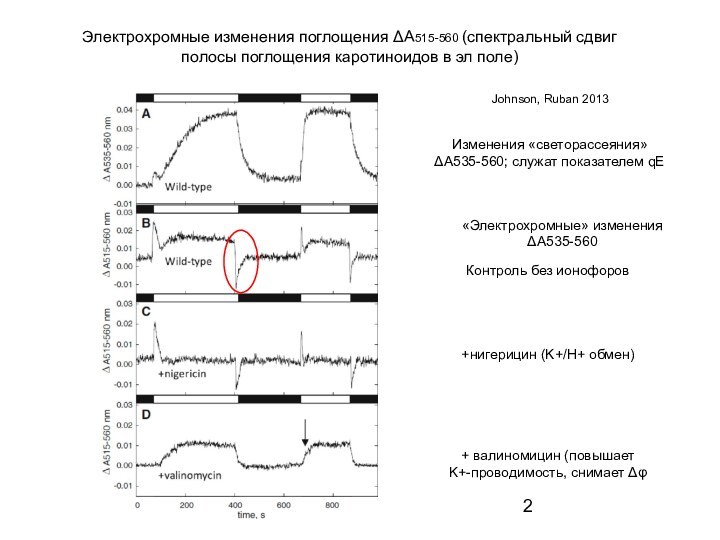
каротиноидов в эл поле)
Изменения «светорассеяния»
ΔА535-560; служат показателем qE
«Электрохромные»
изменения ΔА535-560
Johnson, Ruban 2013
Контроль без ионофоров
+нигерицин (K+/H+ обмен)
+ валиномицин (повышает
K+-проводимость, снимает Δφ
![Электрические поля в фотосинтетических мембранах Координата реакцииQA окисленQA восстановленSchatz et al. 1988[P(Chl)N]*P+I– QA–P+I– QЕсть сходство с динамич.](/img/tmb/15/1453967/27afc119638e8bbfb5f68341a8457e04-720x.jpg)