периодической системы:
гелий He,
неон Ne,
аргон Ar,
криптон Kr, ксенон Xe,радон Rn.
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть



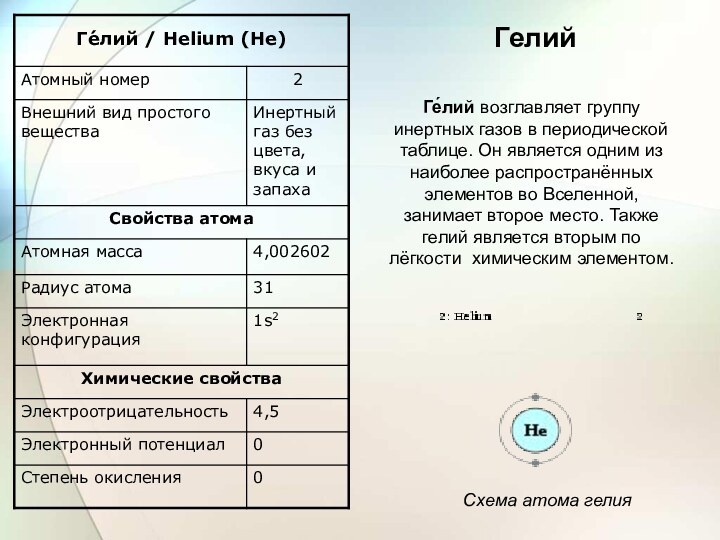


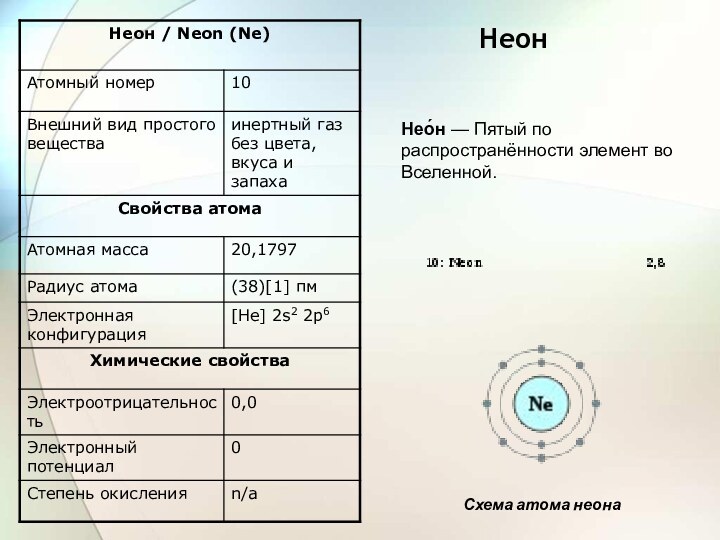

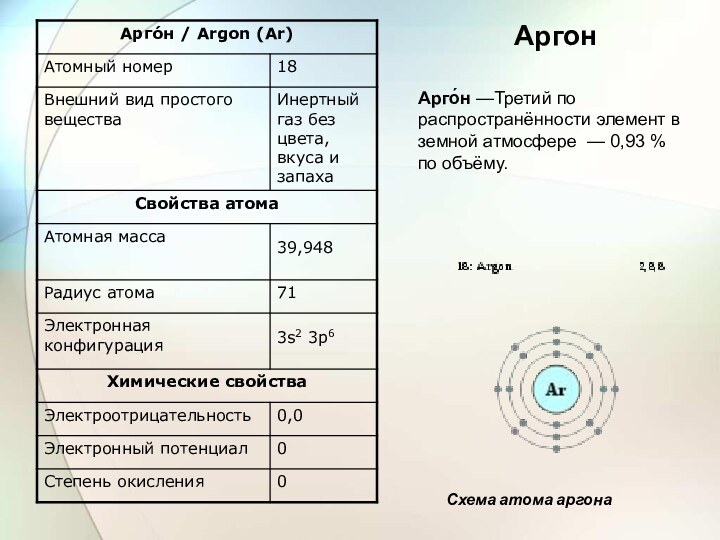

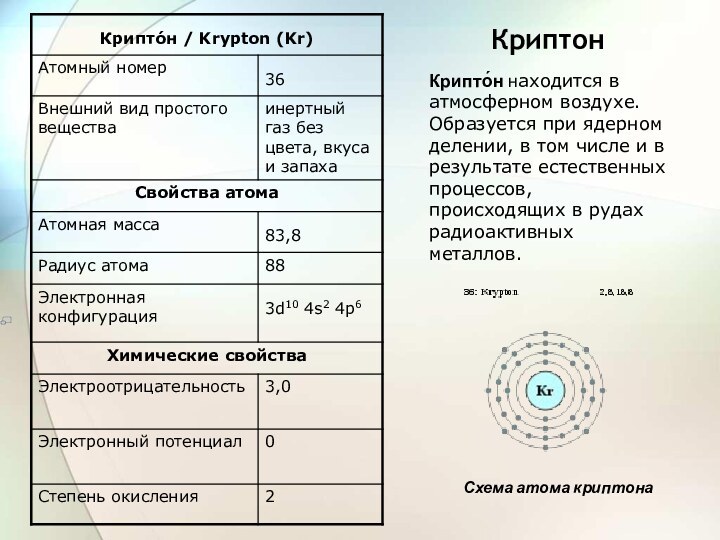

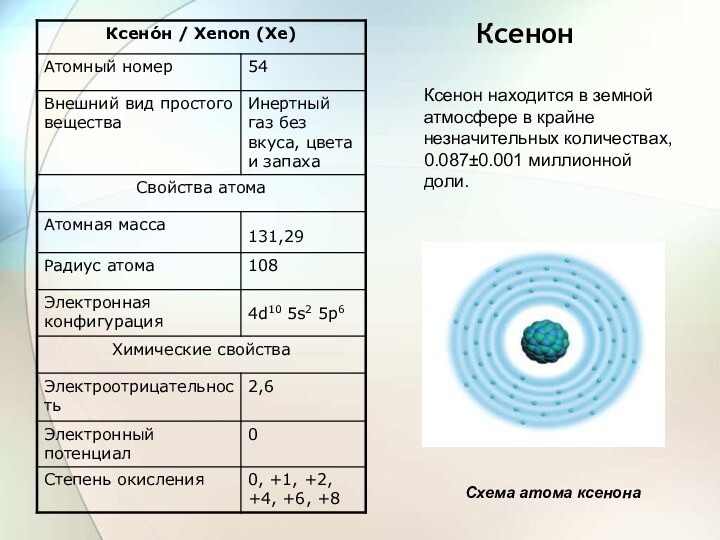


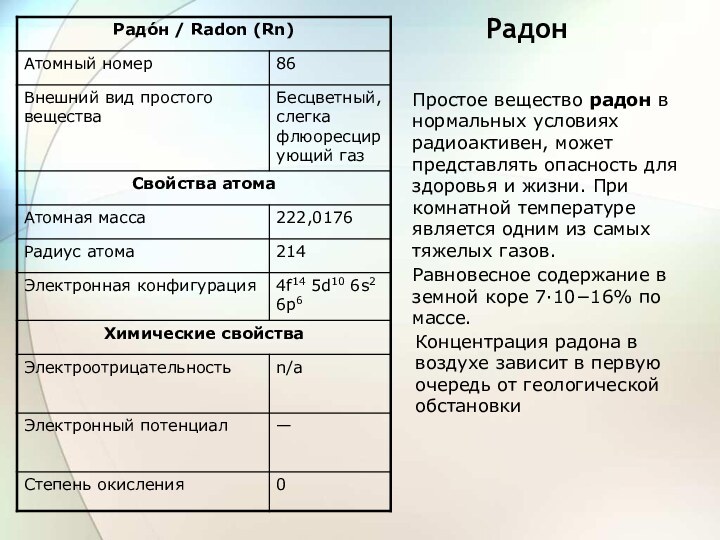

Схема атома гелия
Спектральные линии гелия
Гелий добывается из природного газа процессом низкотемпературного разделения — так называемой фракционной перегонкой
Поскольку гелий обладает низкой плотностью и негорюч, им заполняют метеорологические шары-зонды, аэростаты, дирижабли. Жидкий гелий используется для создания низких температур, близких к абсолютному нулю.
Газоразрядные лампы, заполняемые неоном, раньше применялись в рекламе, но в последнее время на смену им пришли люминесцентные лампы.
Во время исследования в спектре обнаружились новые линии. В момент, когда Рамзай наблюдал спектр только что полученного газа, в лабораторию вошел его двенадцатилетний сын, успевший стать «болельщиком» отцовых работ. Увидев необычное свечение, он воскликнул: «new one!» Так возникло название газа «неон», по-древнегречески значит «новый».
По предложению доктора Медана (председателя заседания, на котором был сделан доклад об открытии) Рэлей и Рамзай дали новому газу имя «аргон» (от греч. αργός — ленивый, медленный, неактивный). Это название подчеркивало важнейшее свойство элемента — его химическую неактивность.
Схема атома криптона
Выделяют ректификацией из жидкого воздуха.
В 1898 году английский учёный Рамзай выделил из жидкого воздуха (предварительно удалив кислород, азот и аргон) смесь, в которой спектральным методом был открыт криптон (От греч. κρυπτός — скрытый, секретный).
Ксенон получают как побочный продукт производства жидкого кислорода на металлургических предприятиях.
В 1898 году учёные У. Рамзай и У. Рэлей открыли новый газ
(тем же способом, которым был обнаружен криптон) и
назвали его ксенон, что в переводе с греческого значит
«чужой»: в спектре он очень отличался по цвету от
ксеноновой фракции воздуха.
Равновесное содержание в земной коре 7·10−16% по массе.
Концентрация радона в воздухе зависит в первую очередь от геологической обстановки
Радон получают способом
продувки воздуха через
раствор любой соли радия,
а затем из этого воздуха
удаляют химически активные
вещества. Остаток конденсируют
жидким азотом, а из него
уже выделяют радон.
Э. Резерфорд в 1899 году отметил, что препараты тория
испускают некое неизвестное ранее вещество. Это вещество
он предложил назвать эмана́цией (от латинского emanatio
— истечение) тория и дать ему символ Em. Первоначально
эманацию тория называли торо́ном, а эманацию
радия — радо́ном. Впервые её выделили в чистом виде
Рамзай и Грей в 1908 году. В 1923 году газ получил
окончательное название радон и символ Em был сменен на Rn.